1、选择题 教材中氨的喷泉实验体现了氨的哪一种性质(?)
A.还原性
B.比空气轻
C.很易液化
D.极易溶于水
参考答案:D
本题解析:略
本题难度:简单
2、实验题 (15分)已知硝酸铜溶液呈蓝色。但在铜与浓硝酸、稀硝酸反应的实验中,同学们发现,除了生成的气体颜色不相同外,最终溶液的颜色也不相同:前者呈绿色,而后者呈蓝色。
甲、乙二位同学为此进行了实验探究。
甲:在I、II两支试管中分别加入等体积的浓HNO3和稀HNO3,再向两支试管中分别投入等质量的铜片,充分反应后铜均无剩余。结果:I中溶液呈绿色,II中溶液呈蓝色。
乙:分别取I中的绿色溶液于两支试管Ⅲ、IV中,对试管Ⅲ进行多次振荡、静置,最终溶液颜色由绿色转变为深蓝色;向试管IV中缓缓加水并不停振荡,观察到溶液由绿色变为深蓝色,最后变为淡蓝色。
请回答下列问题:
(1)分别写出Cu与浓HNO3、稀HNO3反应的化学方程式:__________、__________。
(2)甲的实验_______(“能”或“不能”)说明溶液呈现不同的颜色与其物质的量浓度无关,这是因为充分反应后,I、II两试管中Cu(NO3)2溶液的物质的量浓度_______(填“相等”或“不相等”)。
(3)请你根据乙的实验,推测Cu与浓HNO3反应后溶液呈绿色的原因是________
_______________________________________________________________。
(4)请设计一个方案,验证你所得到的上述结论:____________________________。
参考答案:(1)Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O(2分)
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O(2分)
(2)能(2分)?相等(2分)
(3)反应产生的NO2部分溶解于浓硝酸中呈黄色,与蓝色的硝酸铜溶液混合而使溶液呈绿色(3分)
(4)方案一:取Cu与浓HNO3反应后的绿色溶液,向其中通入足量的空气(或氧气),溶液颜色由绿色逐渐变为蓝绿色,最终变为蓝色。
方案二:取Cu与浓HNO3反应后的绿色溶液,加热,溶液颜色由绿色逐渐变为蓝绿色,最终变为蓝色(可任选其中一个作答)。(4分)
本题解析:略
本题难度:简单
3、计算题 将12.8 g铜跟一定量的浓硝酸反应,待铜耗尽时,共产生气体5.6 L(标准状况下)。计算被还原的HNO3的物质的量是多少?
参考答案:0.25 mol
本题解析:事实上,铜与浓硝酸反应时,浓硝酸的质量分数在不断降低,后来发生的反应,应是铜与稀硝酸的反应,生成的5.6 L气体,也应该是NO2与NO的体积之和。
根据氮原子守恒的方法解此题:
2HNO3 Cu(NO3)2
Cu(NO3)2
1HNO3 1NO
1NO
1HNO3 1NO2
1NO2
被还原的硝酸应该是生成气体的硝酸。
n(NO)+n(NO2)=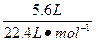 ="0.25" mol。
="0.25" mol。
所以被还原硝酸的物质的量为0.25 mol。
本题难度:简单
4、填空题 在一定条件下,某元素的氢化物X可完全分解为两种单质Y和Z。若已知:
①反应前的X与反应后生成的Z的物质的量之比n(X)∶n(Z)=2∶3。
②单质Y的分子为正四面体构型。
请填写下列空白。
(1)单质Y是______________,单质Z是_________________(填写名称或化学式)。
(2)Y分子中共含________________个共价键。
(3)X分解为Y和Z的化学方程式为:____________________________________。
参考答案:(1)P4? H2(2)6
(3)4PH3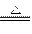 P4+6H2
P4+6H2
本题解析:本题是一道推断题,解题关键是找出“突破口”,该题的突破口是单质Y的分子为正四面体构型。根据Y分子为正四面体构型,假设Y为P4,可推测X为PH3。
4PH3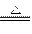 P4+6H2
P4+6H2
即n(X)∶n(Z)=2∶3
本题难度:简单
5、选择题 有关氨气的实验较多,下面对这些实验的实验原理的分析中,正确的是( )
A.氨气极易溶解于水的性质可以解释氨气的喷泉实验 ?
B.氨气的还原性可以解释氨气与氯化氢的反应实验?
C.铵盐的水溶性大是实验室中用NH4Cl和Ca(OH)2的混合物制取氨气的原因?
D.NH3・H2O的热不稳定性可以解释实验室中用加热氨水的方法制取氨气
参考答案:AD
本题解析:由于氨气极易溶解于水从而造成系统内外有较大的压强差,所以A正确;氨气的还原性主要是-3价的氮被氧化的过程。
本题难度:简单