1、选择题 19世纪中叶,俄国化学家门捷列夫的突出贡献是
A.提出原子学说
B.提出分子学说
C.发现元素周期律
D.发现氧气
参考答案:C
本题解析:试题分析:19世纪中叶,俄国化学家门捷列夫的突出贡献是发现元素周期律。提出原子学说的是道尔顿,提
出分子学说的是阿伏加德罗,答案选C。
考点:考查化学式的有关判断
点评:该题是基础性试题的考查,难度不大,记住即可。有利于调动学生的学习兴趣和学习化学的积极性。
本题难度:困难
2、选择题 若原子核外电子排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第二层电子数不超过15个,而且各电子层容纳电子数最多为2n2个,则元素周期表中第3、4、5周期含有的元素分别有
[? ]
A.5种、10种、15种
B.8种、18种、18种
C.8种、10种、15种
D.9种、10种、15种
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列物质能通过化合反应直接制得的是(?)
①FeCl2? ②H2SO4?③NH4NO3?④HCl? ⑤Fe(OH)3
A.只有①②③
B.只有②③
C.只有①③④
D.全部
参考答案:D
本题解析:略
本题难度:一般
4、填空题 下表列出了前20号元素中的某些元素性质的有关数据。
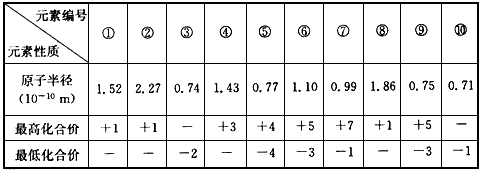
试回答下列问题:
(1)⑤的元素符号是_______,以上10种元素中原子半径最大的是_______(填元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子均满足最外层为8电子稳定结构的物质可能是____________。
(3)写出上述元素中金属性最强的元素所形成的氢氧化物的溶液与④的氧化物反应的离子方程式:___________________________。
参考答案:(1)C;K
(2)CCl4、PCl3
(3)2OH-+Al2O3=2AlO2-+H2O{或Al2O3+2OH-+3H2O=2[Al(OH)4]-)
本题解析:
本题难度:一般
5、选择题 下列各组元素性质的递变错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素的最高正化合价依次升高
C.B、C、N、O、F原子半径依次增大
D.Be、Mg、Ca、Sr、Ba的失电子能力依次增强
参考答案:A、Li、Be、B三种元素原子位于第二周期,电子层数相同,最外层电子数依次增多,故A正确;
B、P、S、Cl三种元素位于第三周期,最高化合价分别为+5、+6、+7,化合价升高,故B正确;
C、同周期从左到右原子半径依次减小,B、C、N、O、F原子半径应依次减小,故C错误;
D、Be、Mg、Ca、Sr、Ba元素位于第ⅡA主族,从上到下失电子能力依次增强,故D正确;
故选C.
本题解析:
本题难度:简单