1��ѡ���� 3.2gCu�������8mol/L30mLHNO3��Ӧ������Ļ�ԭ����ΪNO2��NO����Ӧ����������Һ��n(H+)Ϊamol������Һ������n(NO3-)Ϊ


A��amol
B��(0.1+a)mol
C��(0.05+a)mol
D��(0.2+a)mol
�ο��𰸣�B
�����������
�����Ѷȣ���
2��ѡ���� ����������������ȷ���ǣ�?��
A�������о綾������û�ж�
B�������ڿ����м��ȵ�260 ��Ϳ���ת��ɲ���ȼ�յĺ��
C���������������찲ȫ���
D�������İ���Ӧ�ñ�����ˮ��
�ο��𰸣�D
������������ڰ���������ȼ������ڿ����н���ֱ�Ӽ��ȵ�260 �棬��������Ѿ�ȼ���ˣ�����ѡD��
�����Ѷȣ���
3��ѡ���� ����ʳƷ���Ӽ�������Ӧ����ȷ���ǣ�?��
A�����������������
B��������������������
C�����ɼ�����̼������
D����ɫ������Ҷ����
�ο��𰸣�A
���������A���������ƾ��ж��ԣ�����������ζƷ����AӦ�ô���
B���������ƾ��з����ԣ�������������������BӦ����ȷ��
C��̼�����������ֽܷ����ɶ�����̼������ʹʳƷ������ɣ����������ɼ�����CӦ����ȷ��
D��Ҷ������ʾ��ɫ����������ɫ������DӦ����ȷ��
��ѡA��
�����Ѷȣ���
4������� ��12�֣�X��Y��Z��WΪ����������ͬ�����������ӻ���ӣ�����X��5��ԭ�Ӻˣ���Щ����һ��������������ת����ϵ��ͼ�в��ַ�Ӧ����P��Ӧ��������ȥ����
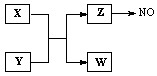
��1��Z ��NO��Ӧ�Ļ�ѧ����ʽ�ǣ�?
Һ̬ Z��ˮ�ĵ������ƣ����д��ڵĵ�������ͬ����������?��
��2��ʵ�����м���Z�Ļ�ѧ�Լ��������ǣ�
?
| ?��ѧ�Լ�
| ?����
|
����һ
| ?
| ?
|
������
| ?
| ?
|
��3���ɹ���X��Y������Ԫ������ɵ�һ�����ӻ����������Ԫ��ԭ����֮��Ϊ2��4��3�������ӻ�������?����д��ѧʽ����
��4��һ�������£�Z��һ�����������������Ӧ�����������ֺ��ȶ��IJ�����ж���������Z�Ļ������20 mL�ڸ������·�Ӧ��ʵ�ʲμӷ�Ӧ�Ķ���������Z��2 mL����ԭ���������Z������������������?��
�ο��𰸣���12�֣�
��1�� ? NH2����NH4+
? NH2����NH4+
��2��
?
?��ѧ�Լ�
?����
����һ
��ʪ��ĺ�ɫʯ����ֽ���飨1�֣�
��ֽ��Ϊ��ɫ��1�֣�
������
պ��Ũ����IJ��������飨1�֣�
�а������ɣ�1�֣�
��3��NH4NO3��
��4��2�s3��7:3
���������������Ҫ���������ṹ�����������ʼ����飻������ԭ��Ӧ�����֪ʶ��
��1�����볣����10���������������������֪����XΪNH4+��YΪOH����ZΪNH3��WΪH2O��
��4��4NH3 + 3NO2 =2N2 + 6H2O
��μӷ�Ӧ��NH3Ϊa ml����μӷ�Ӧ��NO2Ϊ3a/4����a-3a/4=2��a=8��
���Բμӷ�Ӧ��NH3Ϊ8 ml��NO2Ϊ6ml�����ڶ��߹�20 ml�����������
NH3������NH3Ϊ14 ml��NO2Ϊ6 ml�����������Ϊ7:3
NO2������NH3Ϊ8 ml��NO2Ϊ12 ml�����������Ϊ2:3
�����Ѷȣ�һ��
5��ѡ���� �����£��� ��Һ�еμ�����
��Һ�еμ�����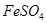 ��Һ���ɷ�������������Ӧ��
��Һ���ɷ�������������Ӧ��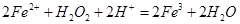 ��
�� ����˵����ȷ����
����˵����ȷ����
A���� �ֽ�����У�
�ֽ�����У�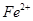 ��
��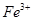 ���������ֲ���
���������ֲ���
B�� �������Ա�
�������Ա�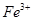 ǿ���仹ԭ�Ա�
ǿ���仹ԭ�Ա�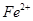 ��
��
C���� �ֽ�����У���Һ��
�ֽ�����У���Һ��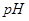 ���½�
���½�
D�� ���������������
���������м�������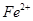 ������߲���
������߲���
�ο��𰸣�A
���������A�����������Ӧ֪��Fe3+��Fe2+��H2O2�ֽ�Ĵ����������������䣬��ȷ��B����2Fe2++H2O2+2H+=2Fe3++2H2O��2Fe3++H2O2=2Fe2++O2��+2H+��֪��H2O2�������ԣ�Fe3+�������ԣ�H2O2�Ļ�ԭ�ԣ�Fe2+�Ļ�ԭ�ԣ�����C����������Ӧ��ӿɵ�2H2O2=2H2O+O2�������Էֽ�����У�Fe2+����������ҺpHֵ���䣬����D����ΪFe2+�ɵ���H2O2�ֽ⣬����H2O2��������Ҫ�������Fe2+������
�����Ѷȣ�һ��