1、填空题 (9分)将250mLH2SO4的质量分数为98%,密度为1.84g/cm3的浓硫酸稀释到1000mL。
(1)浓硫酸的物质的量浓度是多少?
(2)此时溶液中H2SO4的物质的量是多少?
(3)稀释后溶液中H+的物质的量浓度是多少?
参考答案:(1)18.4 mol/L(2)4.6mol?(3)9.2mol/L
本题解析:略
本题难度:简单
2、选择题 在硫酸、明矾和硫酸铝组成的混合溶液中,c(Al3+)="0.3" mol・L-1,c(SO42-)=0.7mol・L-1, 由水电离的c(H+)=10-13 mol・L-1,则c(K+)为
A.0.15mol・L-1
B.0.2mol・L-1
C.0.3mol・L-1
D.0.4mol・L-1
参考答案:B
本题解析:由水电离的c(H+)=10-13 mol・L-1,所以由水电离的c(OH―)=10-13 mol・L-1,说明水的电离主要受到硫酸电离的抑制。所以溶液中的c(H+) =10-1 mol・L-1,c(OH―)=10-13 mol・L-1,根据电荷守恒可得正确答案为B。
本题难度:一般
3、选择题 VL浓度为0.5mol?L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
A.通入标准状况下的HCl气体11.2VL
B.加入10mol?L-1的盐酸0.1VL,再稀释至1.5VL
C.将溶液加热浓缩到0.5VL
D.加入VL1.5mol?L-1的盐酸混合均匀
参考答案:A、标准状况下的HCl气体11.2VL物质的量是0.5mol,VL浓度为0.5mol?L-1的盐酸中HCl的物质的量不能计算其具体的数值,所以无法计算通入氯化氢后溶液的物质的量浓度,故A错误.
B、VL浓度为0.5mol?L-1的盐酸的物质的量是0.5Vmol,10mol?L-1的盐酸0.1VL的物质的量是Vmol,再稀释至1.5VL,所以C=C1V1+C2V2V=0.5Vmol+Vmol1.5L=1mol/L,故B正确.
C、加热浓缩盐酸时,导致盐酸挥发增强,故C错误.
D、浓稀盐酸混合后,溶液的体积不是直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,故D错误.
故选B.
本题解析:
本题难度:一般
4、实验题 某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:
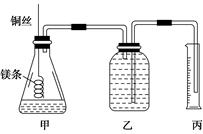
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol/L的盐酸溶液;
②用________(填仪器名称并注明规格)量取10.0 mL 1.0 mol/L的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)用文字表述实验步骤④中检查装置气密性的方法:
___________________________________________________
(2)实验步骤⑤中应选用________(填序号)的量筒。
A.100 mol ? B.200 mL ? C.500 mL
读数时除恢复到室温外,还要注意_________________________________________。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=________,若未除去镁条表面的氧化膜,则测量结果________(填“偏大”、“偏小”或“无影响”)。
参考答案:②10 mL量筒 ③0.12
(1)两手掌紧贴锥形瓶外壁一会儿,如果观察到广口瓶中长导管内有一段水柱高出液面,表明装置气密性良好
(2)B 量筒内的液面与集气瓶内的液面相平
(3)0.2 V L/mol 偏小
本题解析:②量筒的精确度是0.1 mL,故应用10 mL量筒;③因HCl的物质的量为0.01 mol,由反应Mg+2HCl=MgCl2+H2↑知,HCl可与0.005 mol Mg完全反应,为保证HCl完全反应,故镁应不少于0.005 mol×24 g/mol=0.12 g。
(1)本装置可与初中化学制氢气的装置相联系,用微热的方法检查装置的气密性。
(2)实验中产生的气体在标准状况下的体积为0.005 mol×22.4 L/mol=0.112 L=112 mL,考虑到室温时气体的体积稍大些,再考虑通常仪器规格应略大且越接近,误差越小,故选B。读数时注意量筒内的液面与集气瓶中液面相平,保证气压相等。
(3)Vm是气体的体积(排出水的体积)与气体的物质的量之比。若未除去表面的氧化膜,导致氧化膜耗酸,从而放出H2的体积变小,则Vm偏小。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的数值,下列叙述中正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
C.在常温常压下,11.2L Cl2含有的分子数为0.5NA
D.标准状况下,11.2LH2O含有的分子数为0.5NA