1、选择题 下列化学反应中,属于氧化还原反应的是
[? ]
A.NaOH+HCl=NaCl+H2O
B.H2CO3=H2O+CO2↑
C.NH3+HCl=NH4Cl
D.2FeCl2+Cl2=2FeCl3
参考答案:D
本题解析:
试题分析:
A.有元素化合价变化的反应属于氧化还原反应,A选项没有元素化合价变化,故A错;
B.有元素化合价变化的反应属于氧化还原反应,B选项没有元素化合价变化,故B错;
C.有元素化合价变化的反应属于氧化还原反应,C选项没有元素化合价变化,故C错;
D.有元素化合价变化的反应属于氧化还原反应,D选项铁元素化合价由+2价升高到+3价,氯化亚铁作还原剂,氯元素由0价降到-1价,氯气作氧化剂,故D正确;
故选:D
本题难度:简单
2、选择题 下列过程没有发生氧化还原反应的是(?)
A.工业制备硅单质
B.漂白粉的失效过程
C.水玻璃的变质过程
D.雷雨发庄稼
参考答案:C
本题解析:凡是有化合价升降的反应都是氧化还原反应,据此可知,选项A、B、D都是和氧化还原反应有关系的。C中水玻璃是硅酸钠的水溶液,吸收CO2生成硅酸而变质,属于复分解反应,不是氧化还原反应,答案选C。
点评:该题是高考中的常见题型,属于基础性试题的考查,试题基础性强,侧重对学生基础知识的巩固和训练,该题的关键是明确氧化还原反应的判断依据,然后记住常见的化学过程,灵活运用即可。
本题难度:简单
3、填空题 用电子转移的观点分析下列氧化还原反应。
2Na+2H2O=2NaOH+H2↑____________________
4Fe(OH)2+O2+2H2O=4Fe(OH)3 _____________________
参考答案: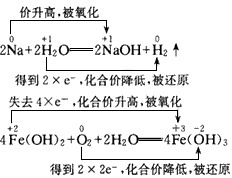
本题解析:
本题难度:一般
4、填空题 根据事实完成下列反应的化学方程式:
(1)AsH3是一种很强的还原剂,室温下,它能在空气中自燃,其氧化产物为As2O3,该反应的化学方程式为________________________________________;
(2)NaNO3与氢碘酸作用,放出NO气体并有单质I2生成__________________;
(3)砷为氮族元素,其氧化物As2O3俗称砒霜,可用马氏试砷法来检验,其原理是将Zn、盐酸和试样混合,若含有砒霜,则生成AsH3气体,这一反应的离子方程式为_______________。
参考答案:(1)2AsH3+3O2====As2O3+3H2O
(2)2NaNO3+8HI====3I2+2NO↑+2NaI+4H2O
(3)6Zn+As2O3+12H+====6Zn2++2AsH3↑+3H2O
本题解析:此题为知识迁移题,书写时应由已知条件确定主要反应物与生成物,然后通过对比已确定的物质写出其他反应物和生成物,最后通过化合价升降法进行配平。
本题难度:简单
5、选择题 在一定条件下有下列反应:X2+Y2+H2O → HXO3+HY(方程式未配平)。则X2、Y2可能的组合是
A.Br2 F2
B.I2 Cl2
C.Cl2 O2
D.N2 Br2
参考答案:B
本题解析:
反应中Y2作氧化剂,X2作还原剂,由于反应在水溶液中进行,因此Y2不可能是F2,A错。由于Y2的还原产物是HY,因此Y2不可能是O2,C错。若选项d成立,据题意N2的氧化产物HXO3是HNO3,Br2的还原产物HY是HBr,很显然HNO3和HBr在溶液中不能大量共存,因此D错。
本题难度:一般