1、选择题 定容容器A与定压容器B的体积开始时相同,内皆装有同质量,同物质的量之比的SO2与O2混合气体,经一定时间在相同温度下达到平衡。有关叙述正确的是
[? ]
A.A、B中SO2的转化率相同
B.B中的反应速率比A中快
C.B中SO2的转化率比A中高
D.若A、B中皆再加入同量的氩气,平衡不移动
参考答案:BC
本题解析:
本题难度:一般
2、选择题 反应Cl2+H2O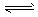 HCl+HClO达平衡时,欲使HClO浓度增大,应加入
HCl+HClO达平衡时,欲使HClO浓度增大,应加入
[? ]
A.CaCO3
B.HCl
C.NaOH
D.H2O
参考答案:A
本题解析:
本题难度:简单
3、选择题 如图所示,把NO2和N2O4的混合气体盛在两个连通的烧瓶里,调节左、右两边注射器内活塞,使其高度相等,关闭弹簧夹;同时把一个烧瓶放在热水里,另一个放在冰水里。下列对实验现象的描述错误的是?
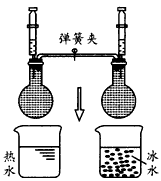
[? ]
A.左边注射器内的活塞高度比右边注射器内的活塞高度要高
B.左边注射器内的活塞与右边注射器内的活塞移动的方向和高度都相同
C.左边烧瓶内的颜色比右边烧瓶内的颜色深
D.两烧瓶内的化学平衡都发生了移动
参考答案:B
本题解析:
本题难度:一般
4、选择题 一定条件下,在一容积固定的密闭容器中充入2 molNO和1 mol O2,发生反应:2NO +O2=2NO2、
2NO2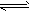 N2O4,下列推测中,正确的是
N2O4,下列推测中,正确的是
[? ]
A.平衡时体系中含NO、O2、NO2、N2O4
B.平衡后容器中压强为开始时的2/3
C.达到平衡后,压缩容器容积,混合气体颜色变浅
D.达到平衡后,再充入少量O2混合气体颜色不变
参考答案:D
本题解析:
本题难度:一般
5、填空题 80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:
N2O4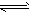 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据
2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据
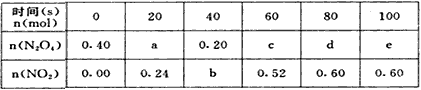
(1)计算20s-40s内用N2O4表示的平均反应速率为_______mol/L.
(2)计算在80℃时该反应的平衡常数K=_______;
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色_______(填“变浅”、“变深”或“不变”) ;
(4)要增大该反应的K值,可采取的措施有(填序号)______________
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
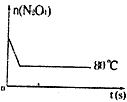
参考答案:(1)0.002
(2)1.8
(3)变浅
(4)D
(5)“略”
本题解析:
本题难度:一般