1、实验题 氯气和氨气在常温下混合即可发生反应。某兴趣小组同学为探究纯净、干燥的氯气与氨气的反应,设计了如下装置

请回答:
(1)装置F中发生反应的离子方程式是___,
(2)装置D中盛放的试剂是____,其作用是____,
(3)装置C中有白烟产生,试写出反应的化学方程式__,
(4)若从装置C的G处逸出的尾气中含有少量Cl2,为防止其污染环境,可将尾气通过盛有 ____的洗气瓶。
参考答案:(1) MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)浓硫酸 ;干燥氯气
(3)8NH3+3Cl2 ==N2+6NH4Cl (或2NH3+3Cl2==N2+6HCl?,?NH3+HCl=NH4Cl)
(4)氢氧化钠溶液
本题解析:
本题难度:一般
2、实验题 实验室用浓盐酸和二氧化锰反应制取纯净、干燥的氯气(氯化氢极易溶于水),装置如下图所示:
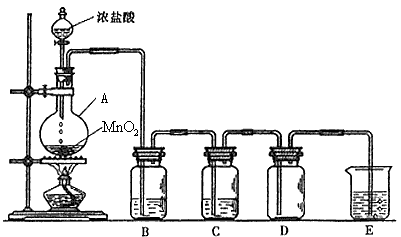
根据装置图回答下列问题:
(1)写出A中反应的化学方程式,并标出反应中电子转移的情况: __________________ 该反应中氧化剂和还原剂的物质的量之比是____________;
(2)分别指出B、C、E装置中试剂的名称及其作用:试剂名称:B中____________,C中____________,E中____________;装置作用:B____________,C____________,E____________;
(3)写出E中发生反应的离子方程式:_______________。
参考答案:(1)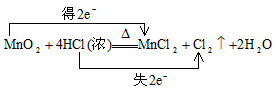 ;1:2
;1:2
(2)水(饱和食盐水) ;浓硫酸 ;氢氧化钠溶液;除去Cl2中混有的气体 ;除去氯气中的水(干燥氯气) ;吸收多余的氯气,防止污染空气
(3)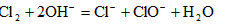
本题解析:
本题难度:一般
3、选择题 下列有关实验原理、装置、操作或结论的描述中,不正确的是
[? ]
A.实验室用大理石与稀盐酸制CO2
B.萃取碘水中的碘
C.制取SO2、检验SO2的漂白性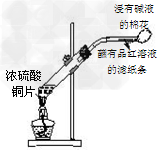
D.实验室用乙醇和浓硫酸制乙烯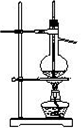
参考答案:B
本题解析:
本题难度:一般
4、填空题 (1)在实验室中用MnO2和浓盐酸反应制备氯气,其反应的化学方程式为:______;
(2)某同学欲制取2.24L(标况)氯气,其做法是称取8.7g?二氧化锰与40mL10mol?L-1?的浓盐酸反应,其做法能否达到目的______(填“能”、“或“不能”).通过计算和文字叙述说明之.
参考答案:(1)浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水.
故答案为:MnO2+4HCl(浓)?△?.?MnCl2+Cl2 ↑+2H2O.
(2)MnO2 +4HCl(浓)? ?△?.?? MnCl2+Cl2↑+2H2O
? 87g? 4mol? 22.4l
? 8.7g?0.4mol?2.24L
理论上二氧化锰和浓盐酸恰好反应生成?2.24L氯气,但实际上随着反应的进行,浓盐酸变成稀盐酸,稀盐酸和二氧化锰不反应,所以得不到?2.24L氯气.
故答案为:不能.
本题解析:
本题难度:一般
5、实验题 用下图中的装置进行实验,将A逐滴加入B中;
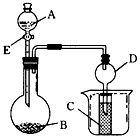
(1)若A为浓硫酸,B为第三周期金属元素的片状单质,其在常温下难与水反应;C为品红溶液,实验中观察到溶液褪色,则B是_______(填化学式),B与浓H2SO4反应的化学方程式为__________________;反应后向烧杯中加入沸水, 又可观察到试管C中的现象为________________________。
(2)若B为Na2CO3,C为C6H5ONa溶液,实验中可观察到小试管内溶液变浑浊,则酸A应具有的性质是
_________________。然后向烧杯中加入沸水,可观察到试管C中的现象是_______________________。
(3)若B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后向烧杯中加入沸水,静置片刻,观察到试管壁出现光亮的银镜,则A是______(填名称),C是_______(填
化学式)与葡萄糖的混合液。该反应的离子方程式为_____________________________,仪器D在此实验中的作用是______________。
参考答案:(l)Mg;Mg+2H2SO4==MgSO4+SO2↑+ 2H2O;C中溶液变红
(2)酸性比碳酸的酸性强;溶液由浑浊变澄清
(3)浓氨水(或铵盐的浓溶液);AgNO3;
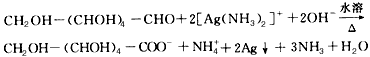 ;防止倒吸
;防止倒吸
本题解析:
本题难度:一般