1、选择题 下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A.该硫酸的物质的量浓度为9.2 mol・L-1
B.1 mol 铁加入到足量的该硫酸中,可产生2 g H2
C.该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol・L-1
D.配制200 mL,4.6 mol・L-1的硫酸溶液需取该硫酸50 mL
参考答案:D
本题解析:A错,根据物质的量浓度与质量分数的关系: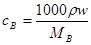 可得该硫酸的物质的量浓度为18.4 mol・L-1;B错,铁常温在浓硫酸中发生钝化,在加热的条件下生成二氧化硫气体;C错,该硫酸与等质量的水混合所得溶液的物质的量浓度等于9.2 mol・L-1
可得该硫酸的物质的量浓度为18.4 mol・L-1;B错,铁常温在浓硫酸中发生钝化,在加热的条件下生成二氧化硫气体;C错,该硫酸与等质量的水混合所得溶液的物质的量浓度等于9.2 mol・L-1
本题难度:简单
2、选择题 下列物质中含原子总数最多的是(?)
A.0.5mol NH3
B.9.03×1023个HCl分子
C.8g CH4
D.44.8L氧气(标准状况下)
参考答案:D
本题解析:根据构成物质的原子可知,A中原子是0.5mol×4=2.0mol;B中是9.03×1023÷6.02×1023/mol=1.5mol;C中甲烷是0.5mol,则原子的物质的量是0.5mol×5=2.5mol;D中氧气的物质的量是44.8L÷22.4L/mol=2mol,则原子的物质的量是4mol,所以答案选D。
点评:该题是中等难度的试题,试题基础性强,难易适中。该题的关键是准确判断出构成分子的原子个数以及气体分子的物质的量,然后灵活运用即可。有利于培养学生的逻辑推理能力,提高学生分析问题、解决问题的能力。
本题难度:一般
3、填空题 (9分)
(1)3.6g H2O的物质的量是________,含有________mol H。
(2)在标准状况下,4g H2、11.2 L O2、1mol H2O中,所含分子数最多的是________,质量最大的是________。(填化学式)
(3)等质量的二氧化硫和三氧化硫,它们的物质的量之比为________,所含的硫原子数之比为________,所含的氧原子数之比为________。
(4)下列物质:①H2O ②石墨 ③NH4NO3 ④硫酸 ⑤CH3COOH ⑥蔗糖属于弱电解质的是 ;属于非电解质的是 (用编号填写)。
参考答案:(1)0.2mol 0.4 (2)H2 H2O (3)5∶4 5∶4 5∶6(4)①⑤ ⑥
本题解析:(1)3.6gH2O的物质的量为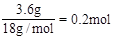 ,含有0.4molH。
,含有0.4molH。
(2)标准状况下,4gH2的物质的量为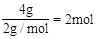 ,11.2LO2的物质的量为
,11.2LO2的物质的量为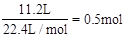 ,质量为16g,1molH2O的质量为18g。因此含分子数最多的是H2。质量最大的是H2O。
,质量为16g,1molH2O的质量为18g。因此含分子数最多的是H2。质量最大的是H2O。
(3)等质量的二氧化硫和三氧化硫,它们的物质的量之比为5∶4;所含的硫原子数之比为5∶4;所含的氧原子数之比为5∶6。
(4)弱电解质为:水、醋酸。非电解质为:蔗糖。
考点:物质的量与电解质综合
点评:电解质和非电解质都属于化合物,单质或混合物既不是电解质也不是非电解质。电解质主要包含酸碱盐和金属氧化物,非电解质主要包含有机物和大部分的非金属氧化物。强电解质包含强酸、强碱和大部分的盐类,弱电解质包含弱酸、弱碱和水。
本题难度:一般
4、选择题 配制一定物质的量浓度的某溶液,下列情况会使配制结果偏低的是( )
A.未冷却即转移、定容
B.未洗涤烧杯及玻璃棒
C.定容时俯视刻度线
D.容量瓶中原有少量蒸馏水
参考答案:A.未冷却即转移、定容,导致溶液体积偏小,则配制溶液浓度偏高,故A错误;
B.未洗涤烧杯及玻璃棒,导致溶质的物质的量偏小,则配制溶液浓度偏低,故B正确;
C.定容时俯视刻度线,溶液的体积偏小,配制溶液浓度偏高,故C错误;
D.容量瓶中原有少量蒸馏水,溶质的物质的量和溶液的体积不变,配制溶液浓度不变,故D错误;
故选:B.
本题解析:
本题难度:简单
5、实验题 (8分)用18mol/L的浓硫酸配制100mL 1mol/L硫酸:
(1)用量筒量取浓硫酸的体积应为?mL,将浓硫酸缓缓倒入盛水的烧杯中后__? __?(填“应该”或“不应”)用少量蒸馏水洗涤量筒2~3次并将洗涤溶液也倒入烧杯中。
(2)若实验仪器有: A.100mL量筒? B.托盘天平? C.玻璃棒? D.50mL容量瓶 E.10mL量筒? F. 胶头滴管? G. 50mL烧杯? H. 100mL容量瓶
验时应选用的仪器有(填入编号)?。
(3)定容时,若俯视液面,则所配溶液浓度? ____?(填“偏高”、“偏低”或“无影响”);若不小心加水超过了容量瓶刻度线,应?。
A.用胶头滴管将多余溶液吸出? B.加热容量瓶使水挥发? C.重新配制
参考答案:(8分)①5.6(2分),不应(1分)
②C E F G H(2分,漏选得1分,有错选不得分)? ③偏高(1分),C(2分)
本题解析:(1)18mol/L的浓硫酸配制100mL 1mol/L硫酸需要浓硫酸的体积是
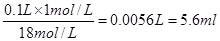 ;量取浓硫酸的量筒是不能洗涤的,否则浓度偏大。
;量取浓硫酸的量筒是不能洗涤的,否则浓度偏大。
(2)量取5.6ml浓硫酸需要10ml量筒,另外还需要稀释浓硫酸额烧杯和玻璃棒,以及100ml容量瓶和定容时需要的胶头滴管,即答案选C、E、F、G、H。
(3)根据c=n/V可知,如果定容时,俯视液面,则容量瓶中溶液的体积减少,所配溶液浓度偏高。若不小心加水超过了容量瓶刻度线,则只能是重新配制,答案选C。
配制一定物质的量浓度溶液的实验是中学化学中一个重要的定量实验,实验过程中引起溶液浓度存在误差的因素有很多。从大的方面讲,一是由实验过程中的不规范操作引起的;二是由仪器或药品等系统原因引起的。由于引起误差的原因复杂,所以误差分析就成为高考化学实验中的一个难点。
本题难度:简单