| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《键参数――键能、键长与键角》高频考点预测(2020年最新版)(二)
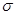 键? G. 键? G.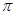 键 键(4)碳铂中C原子的杂化方式有?。 (5)铂(Pt)单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。  晶胞中铂(Pt)原子的配位数为?。若已知铂(Pt)的摩尔质量为M g/mol,阿伏加德罗常数为NA,Pt原子半径为b pm,则该晶胞的密度为 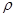 =?g/cm3。(用含M、NA、b的计算式表示,不用化简)。 =?g/cm3。(用含M、NA、b的计算式表示,不用化简)。Ⅱ.原子序数小于36的元素A和B,在周期表中既处于同一周期又位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子,B元素在周期表中的位置为?,A2+在基态时外围电子(价电子)占据的能层符号为?,外围电子(价电子)排布式?。 参考答案:(15分)(1)C、O(1分) N>O>C(1分)? C<N<O(1分) 本题解析:(1)与氮元素处于同一周期且相邻的两种元素分别是C、O,第一电离能随核电荷数的增加而增大,但N原子的2p轨道为半充满状态,是稳定状态,所以第一电离能最大,因此这三种元素的第一电离能从大到小的顺序是N>O>C,电负性随核电荷数的增加而增大,所以这三种元素的电负性由小到大的顺序是C<N<O; 本题难度:一般 3、选择题 下列各组化合物中,化学键类型相同的是(? ) 参考答案:AC 本题解析:B项,Na2O中只有中离子键,Na2O2中除离子键外还有共价键。D项,HCl中只有共价键,NaOH中除共价键外还有离子键。 本题难度:简单 4、选择题 下列分子中,具有极性键的非极性分子的组合是 参考答案:B 本题解析: 本题难度:简单 5、选择题 下列各组物质发生变化时,所克服的粒子间作用属于同种类型的是 参考答案:D 本题解析: 本题难度:简单 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《无机非金属.. | |