1、选择题 下列措施中不能起到节能降耗和保护环境目的的是
A.加大太阳能、水能、风能、地热能等能源开发力度,减少化石燃料的使用
B.研制乙醇汽油技术,降低机动车辆尾气中有害气体排放
C.生产、生活中,努力实现资源的循环利用
D.利用高新技术,提高石油、煤、天然气产量,以满足工业生产快速发展的需求
2、填空题 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。工业上常采用NaClO氧化法生产,其生产工艺如下:
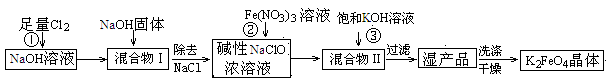
主要反应为:3NaClO+2Fe(NO3)3+10NaOH = 2Na2FeO4↓+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH。
(1)写出反应①的离子方程式:?。
(2)从“混合物II”中分离出K2FeO4后,会有副产品,它们都是重要的化工产品,其中一种在工业上用作氯碱工业原料的物质是?。
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图Ⅰ为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图Ⅱ为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。
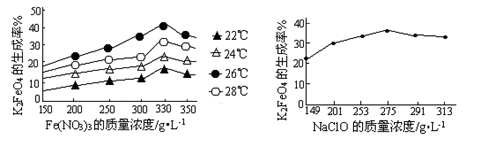
图Ⅰ?图Ⅱ
根据上图分析:工业生产中最佳温度为?℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为?。
3、选择题 镁橄榄石(2MgO?SiO2)中阴离子是( )
A.SiO44-
B.SiO64-
C.SiO32-
D.SiO54-
4、选择题 在熔融状态下,Na与KCl存在可逆反应:Na+KCl NaCl+K,通过调整温度,可利用金属Na来制取K。
NaCl+K,通过调整温度,可利用金属Na来制取K。
物质
| K
| Na
| KCl
| NaCl
|
熔点(℃)
| 63.6
| 97.8
| 770
| 801
|
沸点(℃)
| 774
| 883
| 1 500
| 1 413
|
?
根据上表的熔点和沸点,确定由Na与KCl反应制取K的合适温度为(?)
A.770℃?B.801℃
C.850℃?D.770℃~801℃
5、填空题 工业上生产高氯酸(沸点:90oC)时还同时生产了亚氯酸钠,其工艺流程如下:
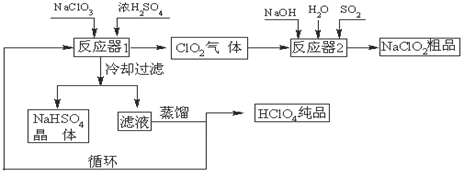
(1)冷却过滤的目的是降低NaHSO4的?,并分离出NaHSO4晶体。
(2)反应器2中发生反应的离子方程式为?,SO2的
作用是作?剂。
(3)上述工业生产高氯酸的化学反应为:3NaClO3+3H2SO4(浓)=3NaHSO4+HClO4+2ClO2+H2O,氧化产物与还原产物的物质的量之比为?。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是高氯酸的沸点比较?(填“高”或“低”),容易从溶液中逸出,循环使用的物质是?。