1��ѡ���� �����£���pH=1��ij����Һ��pH=13������������Һ�У�������������Ƭ���ų�H2�����ʵ���֮�ȴ���1��3����ԭ�������
A.����Һ�������ͬ�����Ƕ�Ԫǿ��
B.����Һ����������Ǽ���Һ�����3��
C.����Һ�������ͬ����������
D.����ǿ�ᣬ������Һ��Ũ�ȱ�NaOH��ҺŨ�ȴ�
�ο��𰸣�BC
�����������������ͼ�ֱ������Ӧ�ķ���ʽΪ��2Al+6H+=2Al3++3H2����2Al+2OH-+2H2O=2NaAlO2+3H2���������������ֱ�����ͼӦʱ����ͼ���ȫ��Ӧ�����������������Ƭ���ų�H2�����ʵ���֮�ȴ���1��3����μӷ�Ӧ��n��H+����n��OH-����1��������ͼ�����ʵ����жϣ�
�����ͼ�ֱ������Ӧ�ķ���ʽΪ��2Al+6H+=2Al3++3H2����2Al+2OH-+2H2O=2NaAlO2+3H2���������������ֱ�����ͼӦʱ����ͼ���ȫ��Ӧ�����������������Ƭ���ų�H2�����ʵ���֮�ȴ���1��3����μӷ�Ӧ��n��H+����n��OH-����1��
A��������Ƕ�Ԫǿ�ᣬ������Һ�������ͬ��������Һ��n��H+�����ڼ���Һ��n��OH-�������������������������1��3����A����
B���������Һ������Ǽ���Һ�����3��ʱ���������ǿ������μӷ�Ӧ��n��H+����С�ڲμӷ�Ӧ��n��OH-�������Էų�H2�����ʵ���֮�ȴ���1��3����B��ȷ��
C���������Һ�������ͬ�����������ᣬ��μӷ�Ӧ��n��H+�����ڲμӷ�Ӧ��n��OH-�������Էų�H2�����ʵ���֮�ȴ���1��3����C��ȷ��
D���������ǿ�ᣬ�����Ũ��C���ᣩ��C��NaOH������D����
��ѡBC��
���������⿼���������������ƺ����ᷴӦ���йؼ��㣬���ݻ�ѧ����ʽ�ҳ������������ᡢ��֮��Ĺ�ϵʽ����ȷ�����Ĺؼ���ͬʱ��Ҫ�������ǿ������Ŀ�Ѷ��еȣ�
�����Ѷȣ���
2��ѡ���� ��30 g�����64 g�Ҵ���Ӧ�����ʵ�ʲ��������۲��ʵ�85������ɵ�����������������
A.37.4 g
B.44 g
C.74.8 g
D.88 g
�ο��𰸣�A
���������
�����Ѷȣ�����
3��ѡ���� ���ۼ������Ӽ������Ӽ��������ȶ��ǹ�����������IJ�ͬ���ã�����������˵���������õ�������
A.��
B.ʯӢ
C.�ռ�
D.ʳ��
�ο��𰸣�C
���������
�����Ѷȣ�����
4��ѡ���� ���з�Ӧ�У����ܱ��ֳ���������ԣ����ܱ��ֳ��������Ե���
A.Fe2O3+HNO3
B.NaOH+HNO3
C.C+HNO3��Ũ��
D.Cu+HNO3
�ο��𰸣�D
���������������������������ԣ���Ӧ������Ԫ��N�Ļ��ϼ۽��ͣ����ֳ����ԣ���Ӧ���������������ɣ�
���A��Fe2O3+HNO3��Ӧ������������ˮ�����ϼ�û�б仯������������ԭ��Ӧ������ֻ���ֳ����ԣ���A����
B��NaOH+HNO3��Ӧ���������ƺ�ˮ�����ϼ�û�б仯������������ԭ��Ӧ������ֻ���ֳ����ԣ���B����
C��C��HNO3��Ӧ���ɶ�����̼������������ˮ������ֻ���ֳ�ǿ�����ԣ���C����
D��Cu��HNO3��Ӧ��������ͭ��NO��ˮ��NԪ�ػ��ϼ۽��ͣ�������ֳ������ԣ���������ͭ�����ỹ���ֳ����ԣ���D��ȷ��
��ѡD��
���������⿼����������ʣ���Ŀ�ѶȲ�����ע�����������������Ե��жϣ�ע��������ʵ����ʷ�����
�����Ѷȣ�һ��
5��ѡ���� 1.7�˻�����H2A����3.01��1022��H2A���ӣ���H2A����Է�������Ϊ
A.17
B.34
C.16
D.32
�ο��𰸣�B
�����������������ͨ���������������ʵ������ٸ������������ʵ����Ĺ�ϵ����Ħ��������Ħ����������ֵ��������Է���������ȣ��Ӷ��ó���Է���������
��𣺸���N=n��NA ��n�T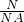 �T=
�T=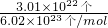 =0.05mol��
=0.05mol��
����m=n��M��M=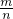 =
=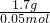 =34g/mol��
=34g/mol��
Ħ����������ֵ��������Է���������ȣ���������Է���������34��
��ѡB
���������⿼������й����ʵ����ļ��㣬����Ҫ��ס������ʽ��Ҫ���Ƶ����������ʵ�������������������Ħ������֮��Ĺ�ϵ�ǽ���Ĺؼ�������ʱҪϸ�ģ�ע�����и������Ƿ���������ԭ������������ȷ���
�����Ѷȣ�����