1������� ��6�֣���1�������£���pH=12��ij����Һ�У���ˮ�����c��OH-��Ϊ?��
��2���������������Һ�У������ӵ������ʵ���������?��
��0.2 mol��L-1��CuSO4��Һ?��0.1 mol��L-1��Na2CO3
��0.2 mol��L-1��KCl?��0.1 mol��L-1��Na2SO4
��3��Ũ��Ϊ0.100 mol��L-1�����и����ʵ���Һ�У�c��NH4+���ɴ�С��˳����?��
��NH4Cl?��NH4HSO4?��NH3��H2O?��CH3COONH4
�ο��𰸣���6�֣�
��1��__10-12 mol��L-1��10-2 mol��L-1_?��2��___��__?��3��__��������������
�����������
�����Ѷȣ�һ��
2������� ��12�֣��ڳ����£�����������Һ����0.1mol/L NH4Cl?��0.1mol/L CH3COONH4?��0.1mol/L NH4HSO4?
�����Ҫ����д���пհף�
��1����Һ�ٳ�??�ԣ���ᡱ��������С�������ԭ���ǣ�
?�������ӷ���ʽ��ʾ��
��2��������������Һ�У�pH��С����?��c(NH4+)��С����??�z����ũ{
��3�������£������Һ�ڵ�pH=7����˵��CH3COO����ˮ��̶�________���������������������NH4+��ˮ��̶ȣ�CH3COO����NH4+Ũ�ȵĴ�С��ϵ�ǣ�
c(CH3COO��) ??c��NH4+)���������������������
�ο��𰸣���12�֣���ÿ��2�֣�
��1��?��? NH4++H2O NH3��H2O+H+��
NH3��H2O+H+��
��2��?��?��
��3��? ="?" =
�����������
�����Ѷȣ�һ��
3��ѡ���� Fe(NO3)2��Һ��dz��ɫ�����д�������ƽ�⣺Fe2+ +2H2O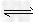 Fe(OH)2+2H+��������Һ����μ������ᣬ�����ı仯��?
Fe(OH)2+2H+��������Һ����μ������ᣬ�����ı仯��?
[? ]
A����Ϊ������H+��Ũ�ȣ�����ƽ�����ƣ�����Fe2+��Ũ������ ?
B��ƽ�������ƶ�?
C����Һ��ɫ��dz��ɫ���ɫ?
D�����ɺ��ɫ����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ������Һ���й����ʵ���Ũ�ȹ�ϵ��ȷ����
A��pH=2�Ĵ�����Һ��pH=12��NaOH��Һ�������ϣ�
c (Na��)��c (CH3COO��)��c(H��)��c(OH��)
B����NH4HSO4��Һ�еμӵ����ʵ�����NaOH�γɵ���Һ�У�
c(Na��) ��c(SO42��) ��c(NH4��) ��c(H��) ��c(OH��)
C��0.1 mol��L��1Na2CO3��Һ��0.1mol��L��1NaHCO3,��Һ��������������Һ��
c(CO32-)+2c(OH-)=c(HCO3- )+c(H2CO3)+2c(H+)
D����ͬ�¶��£�pH��ȵ�Na2CO3��Һ��C6H5ONa(������)��Һ��NaOH��Һ��c(C6H5ONa)>c(Na2CO3)>c(NaOH)
�ο��𰸣�BD
���������pH=2�Ĵ�����Һ��pH=12��NaOH��Һ�����������������Һ�����ԣ�c (CH3COO��)��c (Na��)��c(H��)��c(OH��)��A������NH4HSO4��Һ�еμӵ����ʵ�����NaOH�γɵ���Һ��笠�ˮ�������ԣ� c(Na��) ��c(SO42��) ��c(NH4��) ��c(H��) ��c(OH��)��B��ȷ��
0.1 mol��L��1Na2CO3��Һ��0.1mol��L��1NaHCO3��Һ��������������Һ��Һ�Լ��ԣ�c(CO32-)+2c(OH-)=c(HCO3- )+3c(H2CO3)+2c(H+)��C������ͬ�¶��£�pH��ȵ�Na2CO3��Һ��C6H5ONa(������)��Һ��NaOH��Һ��ˮ��̶�Խ���Ӧ��Ũ��Խ��D��ȷ��
�����Ѷȣ���
5��ѡ���� ����˵����ȷ����
A��������Һ��ˮ�ĵ���̶�һ���ȴ�ˮ�ĵ���̶�С
B�������£�pH=3�Ĵ����pH=11��NaOH��Һ�������Ϻ�pH>7
C��HA�����Ա�HB��ǿ����Na A��Һ��pHһ����NaB��Һ��С
D��0.1mol/L Na2CO3��Һ��0.1mol/L NaHSO4��Һ�������ϣ���Һ��c(Na+)> c(SO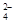 ) >c(HCO
) >c(HCO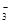 )> c(OH-)> c(H+)
)> c(OH-)> c(H+)
�ο��𰸣�D
���������������Һ����������Һ��Ҳ����������ˮ����ɵ�������Һ��������Һ�е���ˮ�ĵ��룬������ˮ����ɵ�������Һˮ�ĵ���̶ȱȴ�ˮ�ĵ���̶�С��A����pH=3�Ĵ����pH=11��NaOH��Һ�������Ϻ���Һ�����ʵijɷ�Ϊ���ᡢ�����ƣ���Һ�����ԣ�B����HA�����Ա�HB��ǿ����ͬŨ�ȵ�Na A��Һ��pHһ����NaB��Һ��С������뿪��ͬŨ�ȵ�ǰ����һ����C����0.1mol/L Na2CO3��Һ��0.1mol/L NaHSO4��Һ�������Ϻ���Һ�����ʳɷ�ΪNaHCO3��Na2SO4,����D��ȷ��
�����Ѷȣ�һ��