1、选择题 常温下,将NH4NO3溶于水得到无色溶液,为使溶液中的c(NH4+):c(NO3-)=l:l,可采取的下列措施是( )
A.加入适量的HNO3,抑制NH4+水解
B.加入适量的氨水,使溶液的pH=7
C.加入适量的水稀释溶液
D.加入适量的NaOH,使溶液的pH=7
参考答案:A、加入硝酸,氢离子的浓度增大能抑制铵根离子的水解,但硝酸中有硝酸根离子导致硝酸根离子的浓度增大,铵根离子与硝酸根离子的浓度不是1:1,故A错误.
B、加入氨水使溶液的PH=7,溶液中氢离子浓度等于氢氧根离子浓度,溶液呈中性,溶液中阴阳离子所带的电荷相等,所以c(NH4+):c(NO3-)=l:l,故B正确.
C、加水稀释溶液,溶液越稀,铵根离子的水解程度越大,所以c(NH4+):c(NO3-)小于l:l,故C错误.
D、加入适量的NaOH,使溶液的pH=7,溶液中氢离子浓度等于氢氧根离子浓度,溶液呈中性,溶液中阴阳离子所带的电荷相等,[c(NH4+)+C(Na+)]:c(NO3-)=l:l,所以c(NH4+):c(NO3-)小于l:l,故D错误.
故选B.
本题解析:
本题难度:简单
2、填空题 土壤是人类从事农业、林业生产的一项重要资源。保护土壤防止污染、合理利用土壤是我们每个人的职责。请回答问题。
(1)有人说,电动自行车的发展,可能是环保背后的更大污染。这一说法的原因是
?。
(2)农作物的生长对于土壤的酸碱性有一定的要求,有的喜酸性,有的喜碱性。适于一般农作物生长的PH在6.5-7.5之间,酸性或碱性过强都不利于作物的生长。土壤的碱性主要是由于土壤中的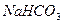 、
、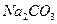 等盐类的水解而产生,请用离子方程式表示
等盐类的水解而产生,请用离子方程式表示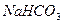 、
、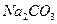 的水解 ??;??。指出土壤显酸性的可能原因(填出一条合理方案即可)??。
的水解 ??;??。指出土壤显酸性的可能原因(填出一条合理方案即可)??。
(3)土壤里发生着大量的氧化还原反应,许多氧化还原反应是在微生物存在的条件下进行的。如当土壤通气性良好时,土壤团粒的空隙里含有氧气,这时,在好气性微生物的作用下氧化反应得以顺利进行,土壤里的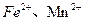 等被氧化为
等被氧化为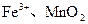 等。从能量的转化角度来说,微生物的活动所需的能量来自?。从化学反应的角度来说,这些微生物在氧化还原反应过程中所起的作用是??。
等。从能量的转化角度来说,微生物的活动所需的能量来自?。从化学反应的角度来说,这些微生物在氧化还原反应过程中所起的作用是??。
参考答案:
(1)废旧电池的随意丢弃对土壤的污染(2分)。
(2)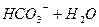

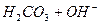 (1分);
(1分);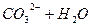

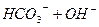 (1分)(不写可逆号的不给分);植物根部呼吸时放出二氧化碳,与水反应生成碳酸(土壤有机质分解产生有机酸等其他合理答案都可)(2分)
(1分)(不写可逆号的不给分);植物根部呼吸时放出二氧化碳,与水反应生成碳酸(土壤有机质分解产生有机酸等其他合理答案都可)(2分)
(3)氧化还原反应所释放的(2分);催化剂(2分)。
本题解析:本题以合理利用土壤为命题的切入点,涉及环境保护、水解、氧化还原反应、化学反应的能量转化等,学科内综合性较强。土壤中微生物的活动所需能量均来自氧化还原反应,而这些氧化还原反应又都是在微生物的作用下才反应的,故微生物在这些氧化还原反应中起催化剂的作用。
本题难度:一般
3、选择题 向1 L 0.3 mol・L-1的NaOH溶液中缓慢通入CO2气体至溶液增重8.8 g(忽略体积变化),下列说法中不正确的是
A.所得溶液呈碱性
B.取20mL所得溶液,甲基橙做指示剂,用0.2 mol・L-1的HCl 进行滴定,消耗HCl的体积为10mL
C.c(Na+) + c(H+) =" 2" c(CO32-) + c(HCO3-) + c(OH?-)
D.2c(Na+) = 3[c(CO32-) + c(HCO3-) + c(H2CO3)]
参考答案:B
本题解析:略
本题难度:一般
4、填空题 写出NaHCO3在水溶液中所发生的电离与水解反应的离子方程式,
?
?
?
并写出溶液中的电荷守恒的表达式?
溶液中的物料守恒(即原子守恒)的表达式?
参考答案:NaHCO3 = Na+ + HCO3-?HCO3- ?H+ + CO32-? HCO3- + H2O
?H+ + CO32-? HCO3- + H2O  ?OH- + H2CO3
?OH- + H2CO3
c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-) + c(OH-)? c(Na+)? = c(CO32-) + c(HCO3-) + c(H2CO3)
本题解析:碳酸氢钠在溶液中既存在电离平衡,也存在水解平衡,所以NaHCO3在水溶液中所发生的电离与水解反应的离子方程式有NaHCO3 = Na+ + HCO3-?、HCO3- ?H+ + CO32-、HCO3- + H2O
?H+ + CO32-、HCO3- + H2O  ?OH- + H2CO3;其电荷守恒和物料守恒的表达式分别是是c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-) + c(OH-)?、c(Na+)? = c(CO32-) + c(HCO3-) + c(H2CO3)。
?OH- + H2CO3;其电荷守恒和物料守恒的表达式分别是是c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-) + c(OH-)?、c(Na+)? = c(CO32-) + c(HCO3-) + c(H2CO3)。
点评:该题是基础性试题的考查,难度不大。试题紧扣教材,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于调动学生的学习兴趣,提高学习效率。
本题难度:一般
5、选择题 向10.00 mL 0.01 mol/L某一元酸HA溶液中逐滴加入0.01 mol/L NaOH 溶液,溶液pH变化曲线如图所示。下列说法不正确的是
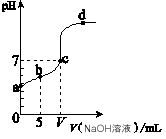
[? ]
A.HA是弱酸
B.b点表示的溶液中:2c(Na+) = c(A-) + c(HA)
C.c点时:V= 10.00 mL
D.b、c、d点表示的溶液中:c(Na+) + c(H+) = c(A-) + c(OH-)
参考答案:C
本题解析:
本题难度:一般