1������� д�����л�ѧ����ʽ�����ӷ���ʽ(6��)
��̼��Ũ���Ṳ�ȵĻ�ѧ����ʽ:?.
��ʵ������ȡ�����Ļ�ѧ����ʽ:?.
�۹����Ķ�����̼������������Һ��Ӧ�����ӷ���ʽ:?.
�ο��𰸣���1��C��2H2SO4(Ũ) CO2����2SO2����2H2O
CO2����2SO2����2H2O
��2��Ca(OH)2��2NH4Cl CaCl2��2H2O��2NH3��
CaCl2��2H2O��2NH3��
��3��CO2��OH��=HCO3��
���������Ũ�����ڼ��ȵ��������ܰ�̼��������CO2�������ᱻ��ԭ����SO2��ˮ��ʵ������ȡ�������õ�����ʯ�Һ��Ȼ�識������ɡ�������CO2���������Ʒ�Ӧ���ɵ�̼�����ơ�
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ��д��ȷ����
A��̼�������Һ����������������Һ��Ӧ + OH��NH3��H2O
B��AlCl3��Һ�м��������İ�ˮ��Al3++ 4NH3?H2O�T�TAlO2��+4NH4++2H2O
C����������Һ����μ���Ba(OH)2��Һ��SO42-ǡ�ó�����ȫ
2Al3��+ 3SO42-+ 3Ba2��+ 6OH��2Al(OH)3��+ 3BaSO4��
D��FeCl2��Һ��Cl2��Ӧ��2Fe2++Cl2=2Fe3++2Cl��
�ο��𰸣�D
�����������
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ������ȷ����
A�������ǽ����������в������ݣ�CO32��+2H+��CO2��+H2O
B�����������������ܽ���ϡ������Һ�У�Fe3O4+8H+=2Fe3++Fe2++4H2O
C��������ͨ��������Һ�У�NH3 + H+ = NH4+
D����̼�������Һ�м���������NaOH��Һ��NH4+ +OH��= NH3��H2O
�ο��𰸣�C
���������A��̼��Ʋ�����ˮ�����ܲ�Ϊ���ӣ�CaCO32��+2H+��Ca2��+CO2��+H2O
B��ϡ�������ǿ�����ԣ�Fe2+��������������ȷ
C����ȷ
D��̼���������Ҳ��μӷ�Ӧ��NH4+ +HCO3��+2OH��= NH3��H2O+CO32��+H2O
��ΪC
�����Ѷȣ���
4��ѡ���� ���л�ѧ���̼��������ȷ����?��?��
A����NaHSO4��Һ�е���Ba(OH)2��Һ������H+��SO42-��Ba2+��OH-��BaSO4����H2O
B����ˮ�����c(H+)Ϊ10-3 mol��L-1����Һ�У�Na+��NO3-��SO32-��Cl-һ���ܴ�������
C������1molKAl(SO4)2����Һ�м���Ba(OH)2��Һ�������������ʱ���������ܵ����ʵ���Ϊ2mol
D��������Ũ�����ữ��KMnO4��Һ��H2O2��ϣ���֤��H2O2���л�ԭ��2MnO4-��6H+��5H2O2��2Mn2+��5O2����8H2O
�ο��𰸣�C
���������
���⿼��������������������ӹ��漰�����йص����ӷ���ʽ��д��A.Ҫʹ����Һ�����ԣ���ô
H+��OH-��������1:1��1molNaHSO4�����1molH+��1molBa(OH)2�����2molOH-������n(NaHSO4):n[Ba(OH)2]=2:1���������ӷ���ʽӦΪ��2H+��SO42-��Ba2+��2OH-��BaSO4����2H2O��B����ˮ�����c(H+)Ϊ10-3 mol��L-1��˵������Һ�Ǵٽ���ˮ�ĵ��롣ˮ��c(H+)=10-7mol��L-1�����Ը���Һ�бغ������������ӣ�Fe3+��Cu2+ ��Al3+�ȣ�����������ӣ�CO32-��CH3COO-�ȣ��������Һ�д���Fe3+��Cu2+�Ļ�����ô��Ȼ��SO32-���ܴ������档D��KMnO4��Һ������Ũ�����ữ������������KMnO4��Һ����Ũ���ᷢ����Ӧ��Ҳ������ŨHNO3�ữ����ŨHNO3��������ǿ�����ԣ���C��Al3++2SO42-+ 2Ba2+��4OH-= 2BaSO4��+AlO2-+2H2O�����������ʵ���Ϊ2mol������Ϊ466g��Al3++ SO42-+
SO42-+ Ba2+��3OH-=
Ba2+��3OH-= BaSO4��+Al(OH)3������������£����������ʵ���Ϊ2.5mol��������Ϊ427.5g������C��ȷ��
BaSO4��+Al(OH)3������������£����������ʵ���Ϊ2.5mol��������Ϊ427.5g������C��ȷ��
�����Ѷȣ���
5��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����?��?��
A����������Һ�м���ͭ�ۣ�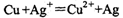
B��AlCl3��Һ�еμӰ�ˮ��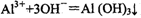
C��ϡH2SO4��Ba��OH��2��Һ��Ӧ��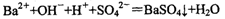
D�����Ȼ�������Һ�м���ϡ���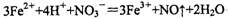
�ο��𰸣�D
���������A����ɲ��غ㡣
B����ˮ�������д��������ʽ��
C�������Ϸ�Ӧ��ʵ����Ӧ���е����������ӣ������ӣ��Լ�������ɵ�ˮ��ϵ����Ӧ��Ϊ2��
D��ȷ��
�����Ѷȣ�һ��