1������� (10��)A��B��C��D��E����ѧ������5�ֻ����A��B�������Ԫ��X��Y���ĵ����������г����� ������������ʼ�Ĺ�ϵ����ͼ��ʾ��
������������ʼ�Ĺ�ϵ����ͼ��ʾ��
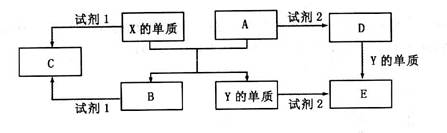
�ش��������⣺
(1)X�ĵ�����A��Ӧ�Ļ�ѧ����ʽ��___________________________________________��
(2)��C��Һ�Լ��ԣ����Լ�1��___________________________________��Һ(д��ѧʽ)��
��C��Һ�����ԣ��������Ե�ԭ����(�����ӷ���ʽ��ʾ)
____________________________________________________��
(3)���Լ�1���Լ�2����ϡ���ᡣ
�ټ�������D����Һ�н������ӵķ�����_______________________________________��
��д��D��E��Ӧ�����ӷ���ʽ______________________________________________ __��
__��
��ij��Ч��ˮ������Y(OH)SO4�ۺϵõ��ġ���ҵ����E��ϡ�������������Ϊԭ�����Ʊ�Y(OH)SO4����Ӧ����NO���ɣ��÷�Ӧ�Ļ�ѧ����ʽ��(������ƽ)��
___________________________________________________________________________��
�ο��𰸣���1��
 ��2��NaOH(��KOH)(1��)��
��2��NaOH(��KOH)(1��)��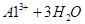 ?
?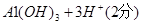
��3����ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ�� ��ɫ����֤��ԭ��Һ�к���Fe3+��2�֣�
��ɫ����֤��ԭ��Һ�к���Fe3+��2�֣�
�� ��1�֣�
��1�֣�
��
�����������
�����Ѷȣ�һ��
2������� ����A��B��C��D���ֻ��������ɫ��Ӧ���ʻ�ɫ��A��B��C�ֱ�����������ᷴӦ��������D����������C���Ⱥ������A����ɫ��ζ������E������A��Һ��ͨ������E��������C����B��C����Һ��Ͽ�����A����ش��������⣺
��1���ƶ�A��B��C��D�Ļ�ѧʽ��A______��B______��C______��D______
��2��A��Һ��ͨ������E��Ӧ�����ӷ���ʽΪ______
��3��B��Һ��C��Һ��Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�A��B��C��D���ֻ��������ɫ��Ӧ���ʻ�ɫ��Ӧ������NaԪ�أ�A��B��C�ֱ�����������ᷴӦ��������D��
DӦΪNaCl��������C���Ⱥ������A����ɫ��ζ������E��CӦΪ�ֽ�����Σ�ΪNaHCO3����AΪNa2CO3��EΪCO2��
��Na2CO3��Һ��ͨ������CO2��������NaHCO3��B��NaHCO3����Һ��Ͽ�����Na2CO3����BӦΪNaOH����
��1�������Ϸ�����֪AΪNa2CO3��BΪNaOH��CΪNaHCO3��DΪNaCl���ʴ�Ϊ��Na2CO3��NaOH��NaHCO3��NaCl��
��2����Na2CO3��Һ��ͨ������CO2��������NaHCO3����Ӧ�����ӷ���ʽΪH2O+CO2+CO32-�T2HCO3-��
�ʴ�Ϊ��H2O+CO2+CO32-�T2HCO3-��
��3��NaOH��NaHCO3����Һ��Ͽ�����Na2CO3����Ӧ�����ӷ���ʽΪHCO3-+OH-�TCO32-+H2O��
�ʴ�Ϊ��HCO3-+OH-�TCO32-+H2O��
���������
�����Ѷȣ�һ��
3���ƶ��� A��B��C�ǵ��ʣ�x��Y��Z��H��?J��?L�ǻ����B�ڿ�����ȼ��Ҳ�ɵ�X��J��x��J���ǹ��塣���ʵ��������£������֮������ͼ��ʾ��ת����ϵ��

(1) ����C��_______��������L��________?(�ѧʽ)
(2) д����Ӧ�١��ݵĻ�ѧ����ʽ��? ��Ӧ�٣�_______________ ��Ӧ�ݣ�________________
�ο��𰸣���1��H2? ��NO?
��2����Ӧ�٣�N2��3Mg Mg3N2
Mg3N2
��Ӧ�ݣ�4NH3��5O2 4NO��6H2O
4NO��6H2O
���������
�����Ѷȣ�һ��
4������� ��֪ͼ��H����ɫҺ�壬�ų�����֮Դ��B�ǿ����к����������ʣ�E�Ǻ���ɫ���壮
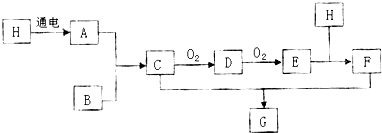
��1��C�Ļ�ѧʽ��______��
��2��D��E���Ǵ�����Ⱦ����������ת���Ļ�ѧ����ʽ�ֱ��ǣ�
��D��E______��
��E��D______��
��3��E��H�ķ�Ӧ�У��������ͻ�ԭ������������______��
��4��C��F��Ӧ����G�Ļ�ѧ����ʽ��______��
�ο��𰸣�H����ɫҺ�壬�ų�����֮Դ���ƶ�ΪH2O��B�ǿ����к�����������ΪN2��E�Ǻ���ɫ���壬�������������õ��ж�ΪNO2���������ͼ������֪��HΪH2O��AΪH2��BΪ�����е�N2��CΪNH3��DΪNO��EΪNO2��E��ˮ��Ӧ���������һ��������C+F=G����NH3+HNO3=NH4NO3��
��1��C�Ļ�ѧʽΪNH3��
�ʴ�Ϊ��NH3��
��2��D��E���Ǵ�����Ⱦ����������ת���Ļ�ѧ����ʽ�ֱ��ǣ���2NO+O2=2NO2����3NO2+H2O=2HNO3+NO��
�ʴ�Ϊ��2NO+O2=2NO2 3NO2+H2O=2HNO3+NO��
��3��E��H��ӦΪ3NO2+H2O=2HNO3+NO������Ԫ�ػ��ϼ۱仯������֪���������ͻ�ԭ������������1��2��
�ʴ�Ϊ��1��2��
��4��C��F��Ӧ����G�ķ�Ӧ�ǰ���������ķ�Ӧ����Ӧ��ѧ����ʽΪ��HNO3+NH3=NH4NO3��
�ʴ�Ϊ��HNO3+NH3=NH4NO3
���������
�����Ѷȣ�һ��
5���ƶ��� ��֪����M��ͬһ�����ڵ�X��Y����Ԫ����ɣ�X ԭ�ӵ������������������ڲ��������һ�룬YԪ�ص����������������۵Ĵ�����Ϊ6��M���������ʵ�ת����ϵ������ʾ�����ֲ�������ȥ��
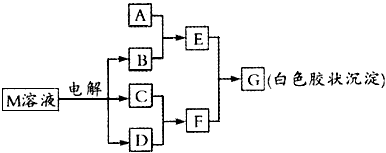
(1)��ҵ���M��Һ�Ļ�ѧ����ʽΪ____________________
(2)��A����X��Yͬ���ڵ�һ�ֳ�����������AԪ�������ڱ��е�λ���ǵ�____���ڵ�____�壬д��A��B��Һ��Ӧ�Ļ�ѧ����ʽ____________________��
(3)��A��ijԪ�ص�һ�ֳ������������������������ά�����Ԫ�ص�ԭ�ӽṹʾ��ͼΪ
________��д��E��F��Ӧ�����ӷ���ʽ____________________��
(4)B�ĵ���ʽΪ____________�����к��еĻ�ѧ��Ϊ____________��
(5)д��M���ʵ�һ����;��________________��
�ο��𰸣�(1)2NaCl+2H2O 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
(2)������A��2Al+2NaOH+2H2O=2NaAlO2+3H2��
(3)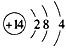 ��2H++SiO32-=H2SiO3��
��2H++SiO32-=H2SiO3��
(4)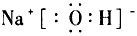 �����Ӽ����ۼ�
�����Ӽ����ۼ�
(5)�ȼҵ���𰸺������ɣ�
���������
�����Ѷȣ�һ��