|
|
|
高中化学知识点归纳《原电池原理》高频试题强化练习(2020年最新版)(十)
2021-06-11 05:53:34
【 大 中 小】
|
1、填空题 (10分)下图是一个化学过程的示意图。
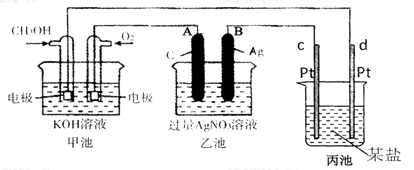
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH的电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
A.MgSO4
B.CuSO4
C.NaCl
D.CuCl2
|
参考答案:(10分)
(1)电解池 (2) 阳极 (3)CH3OH+8OH--6 e- CO32-+6H2O
(4)4Ag++2H2O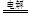 4Ag+O2↑+4H+ (5)280 B、D 4Ag+O2↑+4H+ (5)280 B、D
本题解析:(1)该装置甲池是甲醇燃料电池,属于原电池,则装置乙和丙为电解池。
(2)“串联各池,阴阳交替”,d电极与原电池的负极相连,d电极为阴极,则c(Pt)电极的名称是阳极。
(3)在甲醇燃料电池中,甲醇在负极失电子,在碱性溶液中生成碳酸钾,电极反应式是CH3OH+8OH--6 e- CO32-+6H2O
(4)在乙池中,银电极作阴极,则乙池是用惰性电极电解硝酸银溶液,乙池中反应的离子方程式为4Ag++2H2O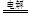 4Ag+O2↑+4H+。 4Ag+O2↑+4H+。
(5)根据电极反应:乙池B电极:Ag++e-=Ag 甲池正极:O2+4e-+2H2O = 4OH-,根据各电极放电量相等,得关系式:4Ag―O2,5.40g银的物质的量为0.05mol,转移电子0.05mol,则消耗氧气0.0125mol,体积为0.0125×22.4×1000=280mL。丙池析出金属0.64g,丙池转移电子的物质的量也是0.05mol,则1.6/0.05=32若该金属是+1价,则该金属的相对原子质量是32×1=32,若该金属是+2价金属,则该金属的相对原子质量是32×2=64,若该金属是+3价金属,则该金属的相对原子质量是32×3=96,选B、D。
考点:考查电解池、原电池的工作原理。
本题难度:一般
2、选择题 下列事实不能用电化学理论解释的是
[? ]
A.铝片不用特殊方法保存
B.生铁比纯铁易生锈
C.制氢气时用粗锌而不用纯锌
D.工程施工队在铁制水管外刷一层“银粉”
参考答案:A
本题解析:
本题难度:一般
3、填空题 如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极.若A、B中充满KOH溶液后倒立于KOH溶液的水槽中.切断K1,合闭K2、K3通直流电,回答下列问题:

①判断电源的正、负极:a为______极,b为______极.
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象______.
③写出电极反应式:A极______,C极______.
④若电解一段时间后,A、B中均有气体包围电极.此时切断K2、K3,合闭K1,则电流表的指针是否移动(填是或否)______.说明理由______.
参考答案:①切断K1,合闭K2、K3通直流电,电极A、B及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为2:1,通过图象知,B极上气体体积是A极上气体体积的2倍,所以B极上得氢气,A极上得到氧气,所以B极是阴极,A极是阳极,故a是负极,b是正极.
故答案为:负;正;
②浸有硫酸钠的滤纸和电极C、D与电源也构成了电解池,因为a是负极,b是正极,所以C是阴极,D是阳极,电解质溶液中的阳离子钾离子向阴极移动,阴离子高锰酸根离子向阳极移动,所以D极呈紫色;电解质溶液中氢离子和氢氧根离子放电,所以在两极上都得到气体.
故答案为:紫色向D方向移动,两极有气体产生;
③A极上氢氧根离子失电子生成氧气和水,电极反应式为4OH--4e=2H2O+O2↑;C极上氢离子得电子生成氢气,电极反应式为4H++4e=2H2↑.
故答案为:4OH--4e=2H2O+O2↑;4H++4e=2H2↑;
④切断K2、K3,合闭K1,电解一段时间后,A、B中均有气体包围电极.此装置构成氢氧燃料原电池,所以有电流通过,电流表的指针移动.
故答案为:是;组成氢氧燃料电池.
本题解析:
本题难度:一般
4、选择题 如图所示,X、Y、Q、W?都是惰性电极,将电源接通后,W极附近颜色逐渐加深.下列说法中错误的是( )
A.电源的M极为正极
B.甲装置中溶液的pH减小
C.甲装置的两个电极上都有单质生成且物质的量之比为1:1
D.欲用乙装置给铜镀银,U极应该是Ag,电镀液选择AgNO3溶液
|
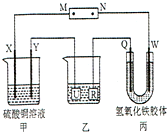
参考答案:A.氢氧化铁胶粒带正电,通电时,W极附近颜色逐渐加深,说明W连接电源的负极,则M为正极,N为负极,故A正确;
B.通电时,甲中X为阳极,电极反应为2H2O-4e-=O2↑+4H+,Y为阴极,电极反应为2Cu2++4e-=2Cu,总反应为:2CuSO4+2H2O?电解?.?2Cu+2H2SO4+O2↑,甲装置中溶液的pH减小,故B正确;
C.通电时,甲中X为阳极,电极反应为2H2O-4e-=O2↑+4H+,Y为阴极,电极反应为2Cu2++4e-=2Cu,甲装置的两个电极上都有单质生成且物质的量之比为n(O2):n(Cu)=1:2,故C错误;
D.欲用乙装置给铜镀银,Ag应连接电源的正极,即U极应该是Ag,电镀液为AgNO3溶液,故D正确.
故选C.
本题解析:
本题难度:简单
5、选择题 下列关于铜电极的叙述,正确的是
[? ]
A.铜锌原电池中铜是负极 ?
B.用电解法精炼粗铜时粗铜作阴极
C.在镀件上电镀铜时可用金属铜作阳极?
D.电解稀硫酸制H2、O2时铜作阳极
参考答案:C
本题解析:
本题难度:一般
