1、选择题 下列说法中,正确的是
[?]
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.燃烧热是指1mol物质燃烧所放出的热量
C.反应产物的总能量大于反应物的总能量时,反应吸热,ΔH>0
D.ΔH的大小与热化学方程式的计量系数无关
参考答案:C
本题解析:
本题难度:简单
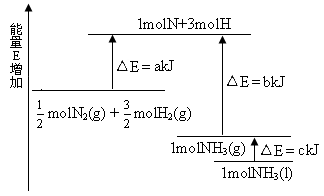
2、选择题 化学反应N2+3H2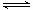 2NH3的能量变化如下图所示,该反应的热化学方程式是
2NH3的能量变化如下图所示,该反应的热化学方程式是
 ?
?
A.N2(g)+3H2(g)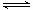 2NH3(1) △H=2(a-b-c)kJ・mol-1
2NH3(1) △H=2(a-b-c)kJ・mol-1
B.N2(g)+3H2(g)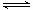 2NH3(g) △H=2(b-a)kJ・mol-1
2NH3(g) △H=2(b-a)kJ・mol-1
C.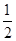 N2(g)+
N2(g)+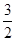 H2(g)
H2(g) 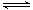 NH3(1) △H=(b+c-a)kJ・mol-1
NH3(1) △H=(b+c-a)kJ・mol-1
D.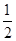 N2(g)+
N2(g)+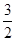 H2(g)
H2(g)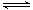 NH3(g) △H=(a+b)kJ・mol-1
NH3(g) △H=(a+b)kJ・mol-1
参考答案:A
本题解析:
本题较新,也很有特色;重在看清图中标识,找准分子,原子变化过程中相应的能量变化。
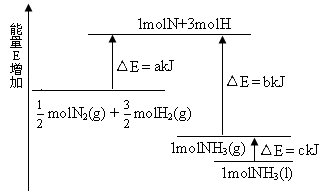
图中a 为反应物键能之和;
图中b 为生成物键能之和;
图中c 为1 mol NH3液化时放出的能量。
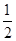 N2(g)+
N2(g)+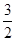 H2(g)
H2(g) 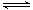 ?NH3(1)? △H=(a-b-c)kJ・mol-1各项同时乘2得
?NH3(1)? △H=(a-b-c)kJ・mol-1各项同时乘2得
N2(g)+3H2(g)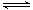 ?2NH3(1)? △H=2(a-b-c)kJ・mol-1
?2NH3(1)? △H=2(a-b-c)kJ・mol-1
本题难度:一般
3、选择题 已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
参考答案:A.由吸热反应,则X、Y的总能量小于M、N的总能量,但无法确定X与M、Y与N的能量高低,故A错误;
B.该反应为吸热反应,与反应条件无关,该反应可能需要加热,也可能不需要加热,故B错误;
C.该反应为吸热反应,则断裂化学键吸收的热量大于生成键释放的能量,故C错误;
D.反应X+Y=M+N为吸热反应,则X、Y的总能量小于M、N的总能量,故D正确;
故选D.
本题解析:
本题难度:简单
4、选择题 已知25 ℃、101 k Pa下,石墨、金刚石燃烧的化学方程式分别为:C(石墨) + O2(g) = CO2(g),1 moL C(石墨) 完全燃烧放热393.51 kJ;C(金刚石) + O2(g) = CO2(g),1 moL C(金刚石) 完全燃烧放热 395.41 kJ。据此推理所得到的下列结论中,正确的是(?)。
Pa下,石墨、金刚石燃烧的化学方程式分别为:C(石墨) + O2(g) = CO2(g),1 moL C(石墨) 完全燃烧放热393.51 kJ;C(金刚石) + O2(g) = CO2(g),1 moL C(金刚石) 完全燃烧放热 395.41 kJ。据此推理所得到的下列结论中,正确的是(?)。
A.金刚石比石墨稳定
B.由石墨制备金刚石一定是吸热反应
C.石墨的能量比金刚石的能量高
D.石墨转化为金刚石是物理变化
参考答案:B
本题解析:略
本题难度:简单
5、选择题 下列说法正确的是(? )
A.需要加热方能发生的反应一定是吸热反应
B.若反应为放热反应,则该反应不必加热就可发生
C.放热反应比吸热反应容易发生
D.化学反应都伴随着能量的变化
参考答案:D
本题解析:反应开始时需要加热的反应可能是吸热反应,也可能是放热反应,选项A、B错误;反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小,而反应发生的难易程度与反应吸热还是放热无关。选项C错误;任何化学反应都伴随着能量的变化。
本题难度:一般