1��ѡ���� �����ڵ�����Ԫ�طֱ�ΪX��Y��Z����֪XԪ�ص�ԭ�������ֻ��һ�����ӣ�YԪ��ԭ�ӵ�M���Ӳ��ϵĵ�����������K���L�����������һ�룬ZԪ��ԭ�ӵ�L���Ӳ��ϵĵ�������YԪ��ԭ�ӵ�L���Ӳ��ϵĵ�������2������������Ԫ������ɵĻ�����ķ���ʽ��������(����)
A�� X2YZ4
B�� XYZ3
C�� X3YZ4
D��X4Y2Z7
�ο��𰸣�C
���������XԪ�ص�ԭ�������ֻ��һ�����ӿ�֪XԪ��ΪH��YԪ��ԭ�ӵ�M���Ӳ��ϵĵ�����������K���L�����������һ��ɣ�K���L���������Ϊ10����M�������Ϊ5��Yԭ���ܹ���15�����ӣ�YΪP��ZԪ��ԭ��L�������Ϊ8-2=6������ZԪ��ΪO��
����P��ߵĻ��ϼ�Ϊ+5�ۣ����ж�A����A��P�Ļ��ϼ�Ϊ+6�ۣ�����ѡ���������B��C��D��P�Ļ��ϼ�Ϊ+5�ۣ����Դ�ӦѡA�������ο�������
�����Ѷȣ���
2��ѡ���� ������Ԫ��X��Y��W��Q��Ԫ�����ڱ��е����λ������ͼ��ʾ�������£�Al������W �����{���������ˮ�����ϡ��Һ��ȴ��������Ũ��Һ������˵����ȷ����
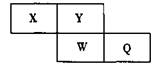
A��Y�����{���ϼ�Ϊ+6
B�����Ӱ뾶��W>Q>Y>X
C���⻯��ķе㣺Y>Q
D�����{���������ˮ��������ԣ�W>Q
�ο��𰸣�C
���������Ũ������ʹ���ۻ���ϡ��������ܽ�������W�����ݱ���Ԫ�ص�λ���ƶ�X��Y��W��Q�ֱ�Ϊ�����������ȣ�A����Ԫ�صķǽ����Ժ�ǿ����+6�ۣ�����B�����Ӱ뾶��S2��>Cl��>N3��>O2������W>Q>X>Y������C���е㣺H2O>HCl��ˮ���Ӽ������������Ȼ�����Ӽ����������ȷ��D���ǽ����ԣ�S<Cl�������ԣ�H2SO4<HClO4������
�����Ѷȣ�һ��
3��ѡ���� ����Ԫ�ص�����������Ӧˮ�����������ǿ���ǣ�?��
A��Si
B�� P
C�� S
D��Cl
�ο��𰸣�D
����������ǽ�����Խǿ������������Ӧˮ��������Ծ�Խǿ������Ԫ�ؾ����ڵ������ڣ��������ҷǽ���������ǿ����Cl�ķǽ�������ǿ�����Դ���D��
�����Ѷȣ���
4��ѡ���� ���л�̬ԭ�ӻ����ӵĵ����Ų�ʽ������� ?
A��Ca�� 1s22s22p63s23p64s2
B��Mg2+�� 1s22s22p6
C��F���� 1s22s22p5
D��Br�� 1s22s22p63s23p63d104s24p5
�ο��𰸣�C
������������ݹ���ԭ����֪ ��ѡ��C�Ǵ���ģ�Ӧ����1s22s22p6������ѡ�����ȷ�ģ���ѡC��
�����������Ǹ߿��еij�����������ͣ����ڻ���������Ŀ��飬���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ��Ǽ�ס����ԭ����Ȼ��������ü��ɡ�
�����Ѷȣ�һ��
5��ѡ���� ��A��B��C��D��������Ԫ�أ�A��BԪ�ص������Ӻ�C��DԪ�ص������Ӷ������� ͬ�ĵ��Ӳ�ṹ����A�������������Ա�B������������������C����������������ɱ�D����������������ɶ࣬��A��B��C��D��ԭ��������С��ϵ�ǣ�?��D
ͬ�ĵ��Ӳ�ṹ����A�������������Ա�B������������������C����������������ɱ�D����������������ɶ࣬��A��B��C��D��ԭ��������С��ϵ�ǣ�?��D
A��B>A>C>D?B��C>B>A>D? C��A>B>C>D? D��B>A>D>C
�ο��𰸣�D
�����������
�����Ѷȣ���