| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ̽����ʵ�����������ۡ�����̣�2020�����°棩(��)
?�����۲쵽?����ʱ�ŵ�ȼ�ƾ��ơ��˲�������Ŀ����?�� ��5����Ӧ������CO2���������練Ӧ����������������������ֱ�д���������������CO2��Ӧ�Ļ�ѧ����ʽ�� ��װ�â�PdCl2��Һ�й۲쵽�к�ɫ������װ�â��й���ɷ�ֻ��һ�֣���������м���ϡ���������ʹ����ʯ��ˮ����ǵ����塣?�� ��װ�â����Ƶ�����Ϊ0.46g����ַ�Ӧ��װ�â��еĹ�����뵽����ϡ�����в���224mL����״����CO2���壬����Һ�л��й��������?�� �ο��𰸣���1��c��f��g��d��e��a��b����b��a����h��3�֣� ����������� �����Ѷȣ�һ�� 3��ѡ���� ����ʵ��ɴﵽʵ��Ŀ�ĵ���: �ο��𰸣�A �����������NaHCO3���-COOH��Ӧ���ʴ�����CH3CH2Br��AgNO3����Ӧ���ʴ�������ˮ����������-CHO���ʴ�����ѡA�� �����Ѷȣ��� 4��ʵ���� ��9�֣������йػ�ѧʵ��IJ�����˵���У���ȷ���ǣ�����ĸ��ţ�?�� |
�ο��𰸣�BDF
�����������
�����Ѷȣ���
5��ʵ���� ��15�֣�ij����С���Ե���Ϊԭ�Ͻ�������ʵ�飺
I���ⶨ�����нᾧˮ�ĺ�����
�ⶨ����ͭ���壨CuSO4��5H2O����ᾧˮ�ĺ�����ʵ�鲽��Ϊ������ĥ?�ڳ�����������װ������������������?�ۼ���?����ȴ?�ݳ���?���ظ������ݵIJ���?�߸���ʵ�����ݼ�������ͭ�ᾧˮ�ĺ�����
��1���ڢܲ���Ҫʹ�õ�������?��
��2���жϾ����Ƿ���ȫʧˮ�ķ����ǣ�?��
��3������ʵ�����ݼ���ó�����ͭ�ᾧˮ�ĺ���Ϊ5.3 �������������ԭ�������?
?�����������ܵ�ԭ��
II���õ����Ƶ�����ͭ������̽������ͭ������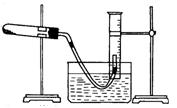
��1��ȡһ������������ͭ�����һ������������ع��壬��Ͼ��Ⱥ�����ͼ��ʾ��װ�ü�����ȡ������Ϊ֤������ͭ������صķֽⷴӦ������������ã�������ʵ���Ӧ�ý��е�ʵ������ǣ���ʵ���Ⱥ���д��ĸ˳��?��Ȼ���һ��֤���ù���Ϊ����ͭ��
a������? b�����? c���ܽ�? d��ϴ��? e������
��2������ͬѧ��Ϊ�����������������һ��ʵ�����֤������ͭ����������ȷֽ��ʵ����������á���ͬ������ͬ�⣬Ҫ���е���һ��ʵ����?������ͬ�⣬˵������?��
�ο��𰸣���15�֣�I.��1������������2�֣�?
��2���������γ��������������0.1g��3�֣�
��3������ǰ��������δ��ȫ����; ����ʱ���������CuSO4�ֽ�. ��4�֣�
II.��1��cadbe����3�֣���2����ȡ��ͬ����������ع��壬��������ֱͭ�Ӽ��ȣ��Աȷų����������ʡ���3�֣�
�����������
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ�ؿ�֪ʶ�㡶��ѧ��Ӧ��.. | |
| �����Ŀ |