| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ��ѧƽ�⡷����Ԥ�⣨2020�����°棩(��)
�ο��𰸣� ��������� �����Ѷȣ�һ�� 2������� ��12�֣���1����֪��Ӧ��4NH3(g)+3O2(g)==2N2(g)+6H2O(g) ��H=��1266.8kJ/mol |
�ο��𰸣�(12��)
��1����4NH3(g)+5O2(g)==4NO(g)+6H2O(g) ��=��905.8kJ/mol (2��) �� K1��K22 (2��)
��2NH3��6e-+6OH- ==N2+6H2O (2��) ����(2��)
��2����AD (2��) ��40%(2��)
�����������1���ٸ��ݸ�˹���ɣ���ӦI+2����ӦII���ɵõ������´���������NO���Ȼ�ѧ����ʽ��Ϊ4NH3(g)+5O2(g)==4NO(g)+6H2O(g) ��=��905.8kJ/mol����Ϊ�÷�Ӧ=��ӦI+2����ӦII�����Ը÷�Ӧ��ƽ�ⳣ��K=K1��K22��
�ڷ�ӦI���Ϊԭ��أ����������������������������Ը����İ���ʧȥ���ӣ������������ӽ�ϣ����ɵ�����ˮ���缫��Ӧʽ��2NH3��6e-+6OH- ==N2+6H2O�������������õ����ӣ���ˮ����������������ӣ�������������pH���ߣ�
��2�������������ת���ʣ�����Լ�ʱ�Ƴ������������Ũ�ȼ�С��ƽ�������ƶ����������¶ȣ�ƽ�������ƶ���������ת���ʽ��ͣ�ʹ�ô�������ƽ����ƶ���Ӱ�죬������ת���ʲ��䣻ѭ�����úͲ��ϲ��䵪������ʹƽ�������ƶ���������ת�����������Դ�ѡAD��
�ڵ����������������25%ʱ�������ĵ����������x�������������������3x�����ɰ����������2x������2x/(1-x+3-3x+2x)=25%�����x=0.4����������ת������3��0.4/3��100%=40%��
���㣺�����˹���ɵ�Ӧ�ã���ѧƽ���ƶ����жϣ�ת���ʵļ��㣬�绯ѧ��Ӧԭ����Ӧ��
�����Ѷȣ�һ��
3��ѡ���� ��ӦA+2B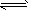 2C��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���ͬʱ�����¶Ⱥͼ�Сѹǿ�ﵽ�µ�ƽ�⣬����ƽ��ʱ�����C�ĺ�����ԭƽ����ͬ���������ƶ���ȷ����
2C��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���ͬʱ�����¶Ⱥͼ�Сѹǿ�ﵽ�µ�ƽ�⣬����ƽ��ʱ�����C�ĺ�����ԭƽ����ͬ���������ƶ���ȷ����
[? ]
A��Bһ��������̬����
B��Aһ��������̬����
C���ﵽ��ƽ��������¶ȣ�����Ӧ���ʼ������淴Ӧ���ʼӿ�
D���ﵽ��ƽ������B��ƽ��������Ӧ�����ƶ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� ��14�֣���ҵ������CO��ˮ������һ�������·�����Ӧ��ȡ������
��CO(g)��H2O(g)  CO2(g)��H2(g) ��H����41 kJ/mol
CO2(g)��H2(g) ��H����41 kJ/mol
ijС���о�����ͬ�¶��¸÷�Ӧ�����е������仯�����Ƿֱ��������ΪV L���������º����ܱ������м���һ�����ķ�Ӧ�ʹ������ͬ�¶��·�����Ӧ������������£�
| ������� | ��ʼʱ���������ʵ���/mol | �ﵽƽ���ʱ��/min | ��ƽ��ʱ��ϵ�����ı仯/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| �� | 1 | 4 | 0 | 0 | t1 | �ų�������32.8 kJ | |
| �� | 2 | 8 | 0 | 0 | t2 | �ų�������Q | |
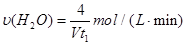
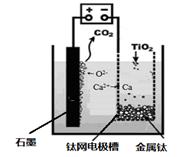
�ο��𰸣���1��С�ڣ���2��80%������3��1 ��4��A����5��2CO(g) + O2(g) ="==" 2CO2(g) ��H =" -566" kJ/mol
��6��3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O
��7���� 2O2- - 4e- ="=" O2���� C + 2O2- - 4e- ="=" CO2��
���Ʊ�TiO2ʱ���ڵ��۷������·�Ӧ��2CaO  2Ca + O2���� 2Ca + TiO2
2Ca + O2���� 2Ca + TiO2 Ti + 2CaO��
Ti + 2CaO��
�ɴ˿ɼ���CaO�������䡣
�� �Ʊ�TiO2ʱ���ڵ��۷������·�Ӧ��������2Ca2+ + 4e- ="=" 2Ca ��������2O2- - 4e- ="=" O2��
2Ca + TiO2 Ti + 2CaO�����ɴ˿ɼ���CaO�������䡣
Ti + 2CaO�����ɴ˿ɼ���CaO�������䡣
�����������1���÷�Ӧ�����У���Ӧ����ӻ�ѧ������ʱ�����յ�������С����������ӻ�ѧ���γ�ʱ���ͷŵ������������Է�����ѧ��Ӧʱ�ų���������2���������з�Ӧ��ƽ��ʱ��32.8 kJ ��41 kJ =0.8������CO��ת����Ϊ80%����3�����������١��������е��¶Ȳ��䣬���Է�Ӧ��ƽ�ⳣ����ͬ��K=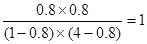 ����4��A. ���ڸ������ڵķ�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ�����������ڷ�Ӧ������ʵ����ı���ȣ����Դﵽƽ��ʱ����������Ϊ��Чƽ�⣬��H2�����������ȣ���ȷ��B���������������١����ǵ�Чƽ�⣬�������ʵ����Ǣٵ�2�����ų�������Ҳ�Ǣٵ�2�������Ԣ��з�Ӧ��ƽ��״̬ʱ��Q ="32.8" kJ��2=" 65.6" kJ������C����Ӧ��ʼʱ�����ڢڵ����ʵ����Ǣٵ�2����Ũ��Խ��Ӧ���ʾ�Խ�죬����D����ѧ��Ӧ�����ǵ�λʱ�������ʵ���Ũ�ȵĸı���ֵ���÷�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ������ȫ��Ӧ���ʸ�ѡ����١�2+�������ɵã�2CO(g) + O2(g) ="==" 2CO2(g) ��H =" -566" kJ/mol����6��n(CO2)="0.6" mol ;n(NaOH)=" 0.200L" ��5 mol/L=1mol,��n(CO2)��n(NaOH)=3��5�����Ի�ѧ����ʽ�ǣ�3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O����7����������O2-ʧȥ���ӣ�����������Ӧ����������Ӧ�ĵ缫��Ӧʽ�ǣ�2O2- - 4e- ="=" O2����дΪC + 2O2- - 4e- ="=" CO2���������Ʊ�������ǰ��CaO���������䣬��ԭ�����Ʊ�TiO2ʱ���ڵ��۷������·�Ӧ��������2Ca2+ + 4e- ="=" 2Ca ��������2O2- - 4e- ="=" O2����2Ca + TiO2
����4��A. ���ڸ������ڵķ�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ�����������ڷ�Ӧ������ʵ����ı���ȣ����Դﵽƽ��ʱ����������Ϊ��Чƽ�⣬��H2�����������ȣ���ȷ��B���������������١����ǵ�Чƽ�⣬�������ʵ����Ǣٵ�2�����ų�������Ҳ�Ǣٵ�2�������Ԣ��з�Ӧ��ƽ��״̬ʱ��Q ="32.8" kJ��2=" 65.6" kJ������C����Ӧ��ʼʱ�����ڢڵ����ʵ����Ǣٵ�2����Ũ��Խ��Ӧ���ʾ�Խ�죬����D����ѧ��Ӧ�����ǵ�λʱ�������ʵ���Ũ�ȵĸı���ֵ���÷�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ������ȫ��Ӧ���ʸ�ѡ����١�2+�������ɵã�2CO(g) + O2(g) ="==" 2CO2(g) ��H =" -566" kJ/mol����6��n(CO2)="0.6" mol ;n(NaOH)=" 0.200L" ��5 mol/L=1mol,��n(CO2)��n(NaOH)=3��5�����Ի�ѧ����ʽ�ǣ�3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O����7����������O2-ʧȥ���ӣ�����������Ӧ����������Ӧ�ĵ缫��Ӧʽ�ǣ�2O2- - 4e- ="=" O2����дΪC + 2O2- - 4e- ="=" CO2���������Ʊ�������ǰ��CaO���������䣬��ԭ�����Ʊ�TiO2ʱ���ڵ��۷������·�Ӧ��������2Ca2+ + 4e- ="=" 2Ca ��������2O2- - 4e- ="=" O2����2Ca + TiO2 Ti + 2CaO�����ɴ˿ɼ���CaO�������䡣
Ti + 2CaO�����ɴ˿ɼ���CaO�������䡣
���㣺���黯ѧ���ļ����뷴Ӧ�ȵĹ�ϵ�����ʵ�ƽ��ת���ʡ�ƽ��״̬���жϡ����ӷ���ʽ����д�����ԭ����Ӧ�õ�֪ʶ��
�����Ѷȣ�����
5��ѡ���� ij�¶��£��ڹ̶��ݻ��������У����淴ӦA��g��+3B��g���T2C��g���ﵽƽ�⣬��ʱ���n��A����n��B����n��C��=2��2��1���������¶Ȳ��䣬��n��A����n��B����n��C��=2��2��1�ı�������������ٳ���A��B��C��������
A��ƽ��������Ӧ�����ƶ�
B��ƽ�����淴�����ƶ�
C��ƽ�ⲻ�����ƶ�
D��n��C����С
�ο��𰸣��ﵽƽ�⣬��ʱ���n��A����n��B����n��C��=2��2��1���������¶Ȳ��䣬��n��A����n��B����n��C��=2��2��1�ı�������������ٳ���A��B��C���൱����ԭ���Ļ�������С���������ѹǿ����Ӧǰ����Ļ�ѧ������֮�ʹ�������������廯ѧ������֮�ͣ�������ѹǿ��ƽ��������Ӧ�����ƶ�����A��ȷ��B��C����
����C�����ʵ�����ƽ����Ȼ������Ӧ�����ƶ���������ɳ����ԭ����֪��ֻ�ܼ����������ܸı䣬��C�����ʵ�������D����
��ѡA��
���������
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ̽����ʵ��.. | |
| �����Ŀ |