|
|
|
�߿���ѧ֪ʶ���ܽᡶ��ѧƽ�⡷����Ԥ�⣨2020�����°棩(��)
2021-06-11 05:56:32
�� �� �� ��
|
1��ѡ���� �ܱ������н������·�Ӧ��X2��g��+3Y2��g�� 2Z��g����X2��Y2��Z��ʼŨ�ȷֱ�Ϊ0.2 mol��L-1��0.6 mol��L-1��0.4 mol��L-1����ƽ��ʱ���������ݿ϶����Ե��ǣ� �� 2Z��g����X2��Y2��Z��ʼŨ�ȷֱ�Ϊ0.2 mol��L-1��0.6 mol��L-1��0.4 mol��L-1����ƽ��ʱ���������ݿ϶����Ե��ǣ� ��
A��X2Ϊ0.4 mol��L-1��Y2Ϊ1.2 mol��L-1
|
2������� ��12�֣���1����֪��Ӧ��4NH3(g)+3O2(g)==2N2(g)+6H2O(g) ��H=��1266.8kJ/mol
��Ӧ��N2(g) + O2(g)="=" 2NO(g) ��=��180.5kJ/mol
���ǵ�ƽ�ⳣ������ΪK1��K2
��д�������´���������NO���Ȼ�ѧ����ʽ ���÷�Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽK= (�ú�K1��K2�Ĵ���ʽ��ʾ)��
�ڷ�Ӧ�����Ƴ�ȼ�ϵ�أ����õ����KOH��Һ���������Һ�����ĵ缫��ӦʽΪ�� ���õ��ʹ�ù����У�����������Һ��pH�� ������ߡ��������͡����䡱����
��2����֪��N2(g) +3H2(g)  2NH3(g) ��H=��92kJ/mol�� 2NH3(g) ��H=��92kJ/mol��
��Ϊ���H2��ת���ʣ��˲�ȡ�Ĵ�ʩ�� ������ĸ��
A����ʱ�Ƴ���
B�������¶�
C��ʹ�ô���
D��ѭ�����úͲ��ϲ���N2
|
����һ���¶ȡ�ѹǿ�£���N2��H2�������1:3���ܱ������л�ϣ�����Ӧ��ƽ��ʱ�����ƽ����������NH3���������Ϊ25%����ʱH2��ת����Ϊ
��
3��ѡ���� ��ӦA+2B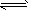 2C��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���ͬʱ�����¶Ⱥͼ�Сѹǿ�ﵽ�µ�ƽ�⣬����ƽ��ʱ�����C�ĺ�����ԭƽ����ͬ���������ƶ���ȷ����
2C��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���ͬʱ�����¶Ⱥͼ�Сѹǿ�ﵽ�µ�ƽ�⣬����ƽ��ʱ�����C�ĺ�����ԭƽ����ͬ���������ƶ���ȷ����
[? ]
A��Bһ��������̬����
B��Aһ��������̬����
C���ﵽ��ƽ��������¶ȣ�����Ӧ���ʼ������淴Ӧ���ʼӿ�
D���ﵽ��ƽ������B��ƽ��������Ӧ�����ƶ�
4������� ��14�֣���ҵ������CO��ˮ������һ�������·�����Ӧ��ȡ������
��CO(g)��H2O(g)  CO2(g)��H2(g) ��H����41 kJ/mol
CO2(g)��H2(g) ��H����41 kJ/mol
ijС���о�����ͬ�¶��¸÷�Ӧ�����е������仯�����Ƿֱ��������ΪV L���������º����ܱ������м���һ�����ķ�Ӧ�ʹ������ͬ�¶��·�����Ӧ������������£�
�������
| ��ʼʱ���������ʵ���/mol
| �ﵽƽ���ʱ��/min
| ��ƽ��ʱ��ϵ�����ı仯/kJ
|
CO
| H2O
| CO2
| H2
|
��
| 1
| 4
| 0
| 0
| t1
| �ų�������32.8 kJ
|
��
| 2
| 8
| 0
| 0
| t2
| �ų�������Q
|
| | | | | | |
|
��1���÷�Ӧ�����У���Ӧ����ӻ�ѧ������ʱ�����յ�������
������ڡ�����С�ڡ����ڡ�����������ӻ�ѧ���γ�ʱ���ͷŵ���������
��2���������з�Ӧ��ƽ��ʱ��CO��ת����Ϊ
%��
��3�������������з�Ӧ��ƽ�ⳣ��K=
��
��4������������ȷ����
������ĸ��ţ���
A��ƽ��ʱ����������H2������������
B���������з�Ӧ��ƽ��״̬ʱ��Q > 65.6 kJ
C����Ӧ��ʼʱ���������з�Ӧ�Ļ�ѧ��Ӧ�������
D���������У���ѧ��Ӧ����Ϊ��
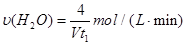
��5����֪����2H2 (g) + O2 (g) = 2H2O (g) ��H����484 kJ/mol��д��CO��ȫȼ������CO2���Ȼ�ѧ����ʽ��
��
��6���������з�Ӧ���е�t minʱ����û��������CO2�����ʵ���Ϊ0.6 mol������200 mL 5 mol/L��NaOH��Һ������ȫ���գ���Ӧ�����ӷ���ʽΪ����һ�����ӷ���ʽ��ʾ��
��
��7���о����֣�������ʯī������������������������CaF2-CaO������ʣ�����ͼ����ʾװ�û�ý����ƣ����Ը�Ϊ��ԭ������ԭ���������Ʊ������ѡ�
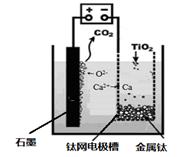
��д��������������Ӧ�ĵ缫��Ӧʽ��
��
�����Ʊ�������ǰ��CaO���������䣬��ԭ���ǣ����Ϸ�Ӧʽ���ͣ�
��
5��ѡ���� ij�¶��£��ڹ̶��ݻ��������У����淴ӦA��g��+3B��g���T2C��g���ﵽƽ�⣬��ʱ���n��A����n��B����n��C��=2��2��1���������¶Ȳ��䣬��n��A����n��B����n��C��=2��2��1�ı�������������ٳ���A��B��C��������
A��ƽ��������Ӧ�����ƶ�
B��ƽ�����淴�����ƶ�
C��ƽ�ⲻ�����ƶ�
D��n��C����С
 2C��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���ͬʱ�����¶Ⱥͼ�Сѹǿ�ﵽ�µ�ƽ�⣬����ƽ��ʱ�����C�ĺ�����ԭƽ����ͬ���������ƶ���ȷ����
2C��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���ͬʱ�����¶Ⱥͼ�Сѹǿ�ﵽ�µ�ƽ�⣬����ƽ��ʱ�����C�ĺ�����ԭƽ����ͬ���������ƶ���ȷ����  CO2(g)��H2(g) ��H����41 kJ/mol
CO2(g)��H2(g) ��H����41 kJ/mol