1、实验题 某学生课外活动小组利用如图所示装置分别做如下实验:
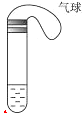
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是__________溶液;加热时溶液由红色逐渐变浅的原因是_____________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是___________溶液;加热时溶液由无色变为红色的原因是_______________。
参考答案:(1)稀氨水和酚酞?;?稀氨水中的NH3逸出,所以溶液的颜色变浅
(2)溶有SO2的品红?;?SO2气体逸出,品红溶液恢复红色
本题解析:
本题难度:一般
2、选择题 150℃时碳酸铵完全分解产生的气态混合物的密度是相同条件下氦气密度的
A.48倍
B.12倍
C.6倍
D.24倍
参考答案:C
本题解析:分析:(NH4)2CO3发生反应:(NH4)2CO3 2NH3↑+H2O↑+CO2↑,由方程式可知,1mol(NH4)2CO3分解生成4mol混合气体,4mol混合气体的质量等于1mol(NH4)2CO3的质量,先根据
2NH3↑+H2O↑+CO2↑,由方程式可知,1mol(NH4)2CO3分解生成4mol混合气体,4mol混合气体的质量等于1mol(NH4)2CO3的质量,先根据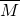 =
=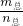 计算混合气体的平均摩尔质量,然后利用密度之比等于摩尔质量之比计算.
计算混合气体的平均摩尔质量,然后利用密度之比等于摩尔质量之比计算.
解答:因(NH4)2CO3发生反应:(NH4)2CO3 2NH3↑+H2O↑+CO2↑
2NH3↑+H2O↑+CO2↑
?方程式可知,1mol(NH4)2CO3分解生成4mol混合气体,4mol混合气体的质量等于1mol(NH4)2CO3的质量,
则混合气平均摩尔质量为=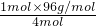 =24g/mol,
=24g/mol,
因气体密度之比等于摩尔质量之比,所以混合气的密度是相同条件下的氢气密度的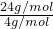 =6倍,
=6倍,
故选C.
点评:本题结合铵盐的化学性质,考查了平均摩尔质量、相对密度的计算等,难度不大,注意基础知识的理解掌握.
本题难度:一般
3、选择题 从下列实验事实中得到的结论,正确的是
A.实验事实:将纯铜片和另一种金属M用导线连接,同时插入稀硫酸中,铜片表面有气泡冒出;结论:金属活动性:M>Cu
B.实验事实:将SO2通入酸性KMnO4溶液中,红色褪去;结论:SO2有漂白性
C.实验事实:将SO2通入品红溶液中,红色褪去;结论:SO2有漂白性
D.实验事实:CO2通入苯酚钠溶液中,出现浑浊;结论;酸性:苯酚<碳酸
E.实验事实:CO2通入苯酚钠溶液中,出现浑浊;结论;酸性:苯酚>碳酸
F.实验事实:Cl2的水溶液可以导电;结论;Cl2是电解质
参考答案:ACD
本题解析:分析:A.M失去电子,作负极;
B.二氧化硫与酸性KMnO4溶液发生氧化还原反应;
C.二氧化硫与品红化合生成无色物质;
D.CO2通入苯酚钠溶液反应生成苯酚和碳酸氢钠;
E.CO2通入苯酚钠溶液反应生成苯酚和碳酸氢钠;
F.氯气为单质;
G.氯气为单质.
解答:A.M失去电子,作负极,Cu电极为正极,则金属活动性为M>Cu,故A正确;
B.二氧化硫与酸性KMnO4溶液发生氧化还原反应,体现二氧化硫的还原性,故B错误;
C.二氧化硫与品红化合生成无色物质,体现二氧化硫的漂白性,故C正确;
D.CO2通入苯酚钠溶液反应生成苯酚和碳酸氢钠,由强酸制取弱酸的反应原理可知,所以酸性为碳酸>苯酚,故D正确;
E.CO2通入苯酚钠溶液反应生成苯酚和碳酸氢钠,由强酸制取弱酸的反应原理可知,所以酸性为碳酸>苯酚,故E错误;
F.Cl2的水溶液可以导电,是氯气与水反应生成酸电离产生自由移动的离子,但氯气为单质,既不是电解质也不是非电解质,故F错误;
G.Cl2的水溶液可以导电,是氯气与水反应生成酸电离产生自由移动的离子,但氯气为单质,既不是电解质也不是非电解质,故G错误;
故选ACD.
点评:本题考查化学实验方案的评价,涉及原电池、二氧化硫的性质、酸性的比较及电解质的判断,题目难度不大,注重基础知识的考查.
本题难度:困难
4、选择题 在图示装置中,将液体Y滴入瓶中并摇动,一会儿小气球胀大。则气体X与液体Y不可能是
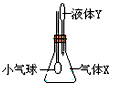
[? ]
气体X 液体Y
A.NH3 水?
B.SO2 浓NaOH?
C.CO2 稀H2SO4?
D.HCl 水
参考答案:C
本题解析:
本题难度:简单
5、选择题 实验室可用下图所示装置干燥、收集某气体R,则R可能是
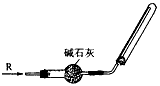
[? ]
A.SO2
B.NH3
C.HCl
D.Cl2
参考答案:B
本题解析:
本题难度:简单