1��ѡ���� �����й����з�����Ӧ��������ȷ����
A����ˮ�к��м�Ԫ�أ�ֻ�辭�������仯�Ϳ��Եõ��ص���
B��Na+��Mg2+��Al3+�õ��������������ʳ��õ������������ķ������Ʊ��䵥��
C�����������з�����������Ĺ����в��漰������ԭ��Ӧ
D���Ӻ�ˮ����ȡ�嵥�ʵĹ������漰�ķ�Ӧ��Ϊ�û���Ӧ
�ο��𰸣�C
���������A. ��ˮ�еļ�Ԫ���Ǽ����ӣ���ȡ�Ȼ��ع��壬ͨ�����õ��أ�������������ԭ��Ӧ����A.���� B.Na��Mg�õ�������Ȼ���ķ������Ʊ��䵥�ʡ�D��ˮ������������������Ϊ�嵥�ʣ����û�ԭ������SO2����ԭ�嵥��Ϊ�����ӣ���������������������Ϊ�嵥��.�˹��̶��ǻ�ѧ�仯��������Ϊ�û���Ӧ��C����������NaOH��Һ�з���Al2O3+2NaOH�T2NaAlO2+H2O��û��Ԫ�صĻ��ϼ۱仯��������������ԭ��Ӧ��ƫ��������Һ���ữ����AlO2-+H++H2O�TAl��OH��3����û��Ԫ�صĻ��ϼ۱仯��������������ԭ��Ӧ�����������������巢��2Al��OH��3 Al2O3+3H2O��û��Ԫ�صĻ��ϼ۱仯��Ҳ������������ԭ��Ӧ��C��ȷ��
Al2O3+3H2O��û��Ԫ�صĻ��ϼ۱仯��Ҳ������������ԭ��Ӧ��C��ȷ��
�����Ѷȣ�һ��
2������� ������������������ͷ�չ����Ҫ���ʻ�����
��1����ͨ��������Ҫ�ɷ���______���ѧʽ��
��2�������ڳ�ʪ��������Ҫ�����绯ѧ��ʴ�������˵�����δ��ʱϴ������Һ�к����Ȼ��ƣ����ڶ������ֺ���ɫ����� ����Ҫ�ɷ���Fe��OH��3ʧˮ��IJ���������йصĵ缫��Ӧʽ����ѧ����ʽ��ʾFe��OH��3�����ɣ�
�ٸ�����______��
��������______��
��Fe��OH��3�����ɣ�______��______��
�ο��𰸣���1����ͨ��������Ҫ�ɷ��Ƕ������衢�����ơ�����ƣ���ѧʽΪ��SiO2��Na2SiO3��CaSiO3��
�ʴ�Ϊ��SiO2��Na2SiO3��CaSiO3��
��2����������Һ�У�������̼�����͵������Һ����ԭ��ط���������ʴ����������ʧ�������ɶ��������ӣ��缫��ӦʽΪFe-2e-=Fe2+��
�ʴ�Ϊ��Fe-2e-=Fe2+��
�������������õ��Ӻ�ˮ��Ӧ�������������ӣ��缫��ӦʽΪO2+4e-+2H2O=4OH-��
�ʴ�Ϊ��O2+4e-+2H2O=4OH-��
���������Ӻ����������ӷ�Ӧ���������������������������ȶ������ױ������е���������������������4Fe��OH��2+O2+2H2O=4Fe��OH��3�������������ʧȥ����ˮ���ɴ��ᾧˮ ��������Fe2O3��xH2O�����������Ҫ�ɷ֣�
�ʴ�Ϊ��Fe2++2OH-=Fe��OH��2����4Fe��OH��2+O2+2H2O=4Fe��OH��3��
���������
�����Ѷȣ���
3������� ú����Ҫ����Դ��Ҳ�ǻ�����������Ҫԭ�ϡ�
(1)úȼ�ղ����ķ���ֱ���ŷŵ������У����ܵ��µĻ�����Ⱦ������_______��
(2)��ͼ�Ƕ�ú��ȼ�ղ����ķ������г���������������ʾ��ͼ��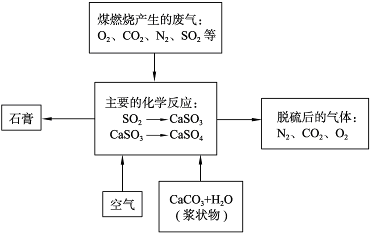
�ٷ�����������У���Ҫ��Ӧ�Ļ�ѧ����ʽΪ______________��_____________��
����ú����ֱ������һ�����ʣ�����Ч����ú��ȼ�ղ�����SO2����������___��
��ʯ��Ĺ�ҵ�����е���;��_________________(д��һ����;����)��
(3)ú����___________(��ӹ�����)���Եõ���¯ú����ú���ͺͽ�̿��ú���;���_______(��ӹ�����)�ɵõ������廯���ú��Ҳ�������⻯��ת��ȼ�ͣ��⻯���ı�����______________��
(4)ú����Һ��ת��ΪCH3OH��������Ƴ���KOH��Һ���õ缫�����һ��ϸС�IJ������缫�����������������ǿ�������ȶ�������CH3OH��O2���ɵ�ȼ�ϵ�ص�����ת����Ҫ��ʽ������?��������ӦʽΪ��������?���缫����Ʋ��۵�ԭ��Ϊ?������
�ο��𰸣�(1)���ꡢ�۳���Ⱦ
(2)��SO2��CaCO3 CaSO3��CO2��2CaSO3��O2��2CaSO4
��CaCO3��CaO��Ca(OH)2
��ҽ�á��������ϡ�ģ�͵Ⱥ�����
(3)����������ú����Ԫ�صú����������ԭ������̼ԭ�����ı�ֵ
(4)�ɻ�ѧ��ת��Ϊ���ܣ�CH3OH+8OH- -6e-=CO32-+6H2O������缫��λ�������CH3OH��O2�����������ٵ缫��Ӧ���ʡ�
���������(1)ú̿ȼ�ջ�������������ܲ������꣬ͬʱú��Ҳ�Ի�������Ⱦ���á�
(2)ʯ��ʯ�Ϳ��������������ǣ�ʯ��ʯ���������Ӧ����������ƺͶ�����̼��������Ƽ���������������ơ���SO2��CaCO3 CaSO3��CO2��2CaSO3��O2��2CaSO4�������������������������CaO��Ca(OH)2��CaCO3��Ӧ�������������ʯ�ࡣ��CaCO3��Ca(OH)2��CaO����ʯ���������ҽ�á��������ϡ�ģ�͵ȡ�
(3)ú���Ծ���ú�ĸ���õ�ú���͡�¯���ͽ�̿��ú����ͨ������õ������廯���ú�в�����Ԫ�أ�����ͨ������ת��Ϊȼ�ͣ��䱾��������ú����Ԫ�صú����������ԭ����̼ԭ�����ı�ֵ��
(4)ԭ��ص�ԭ���ǻ�ѧ��ת��Ϊ���ܡ���������������Ӧ���״��Ӹ���ͨ�룬����缫��Ӧʽ�ǣ�CH3OH+8OH- -6e-=CO32-+6H2O���缫�������һ�㲬�ۣ�������缫��λ�������CH3OH��O2�����������ٵ缫��Ӧ���ʡ�
�����Ѷȣ���
4������� ���������ƣ�Na2S2O5��������ʳƷƯ�������Ʊ������������£�

��֪����Ӧ�����2NaHSO3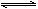 Na2S2O5��H2O�ȶಽ��Ӧ��
Na2S2O5��H2O�ȶಽ��Ӧ��
��1��ʵ������ȡ�����Ļ�ѧ����ʽ��?��
��2�������ա�ʱ������Ӧ�Ļ�ѧ����ʽ��?��
��3����֪Na2S2O5��ϡ���ᷴӦ�ų�SO2�������ӷ���ʽΪ��?��
��4������ƷX�Ļ�ѧʽ�ǣ�?����ѭ�����õ������ǣ�_________��_______��
��5��Ϊ�˼��ٲ�ƷNa2S2O5�����ʺ���������Ʒ�Ӧ�����������������ʵ���֮��ԼΪ?��
�ο��𰸣�
��1��2NH4Cl+Ca(OH)2 2NH3��+CaCl2+2H2O?��2�֣�
2NH3��+CaCl2+2H2O?��2�֣�
��2��2CuS+3O2 2CuO��2SO2?��2�֣�
2CuO��2SO2?��2�֣�
��3�� S2O52��+2H+=2SO2��+H2O?��2�֣�
��4�� CuSO4?5H2O ��2�֣�? CO2��H2O ����2�֣���4�֣�?��5��2��1?��2�֣�
�����������ʵ�������Ʊ��������ù�����������ƺ�����Ȼ�����Ʊ�����2����ͭ����һ����������ͭ�Ͷ�������3�������ʾ��֪���ɶ��������ˮ����4�����������̿��Կ���������ͭ���壻��ͼʾ�п��Կ���������̼��ˮ�����ٴ����ã���Ӧ�������������ֱ��Ƕ��������̼���ƣ����������ʷ�Ӧ�����������������ƣ�Na2CO3��2SO2��2NaHSO3��CO2������������������ʵ���֮��Ϊ��2��1
�����Ѷȣ�һ��
5��ѡ���� ���������У���Ϊȼ��ʱ�Կ���û����Ⱦ����(? )
A��ԭ��
B������
C������
D��ú
�ο��𰸣�B
�������������ȼ�ղ���Ϊˮ������Ⱦ��
�����Ѷȣ���