1、选择题 对下列过程中发生反应的叙述正确的是
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质
C.从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应
D.从海水中提取溴单质的过程所涉及的反应均为置换反应
2、简答题 材料是人类赖以生存和发展的重要物质基础.
(1)普通玻璃的主要成分是______(填化学式)
(2)钢铁在潮湿空气中主要发生电化学腐蚀,炒过菜的铁锅未及时洗净(残液中含有氯化钠),第二天便出现红棕色的锈斑 (主要成分是Fe(OH)3失水后的产物).试用有关的电极反应式、化学方程式表示Fe(OH)3的生成.
①负极:______;
②正极:______;
③Fe(OH)3的生成:______、______.
3、填空题 煤是重要的能源,也是化工生产的重要原料。
(1)煤燃烧产生的废气直接排放到空气中,可能导致的环境污染问题是_______。
(2)下图是对煤矿燃烧产生的废气进行常温脱硫处理的流程示意图。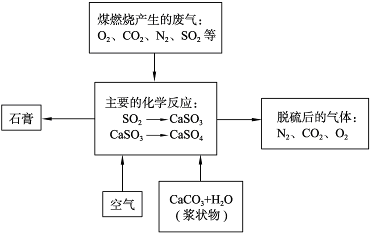
①废气脱硫过程中,主要反应的化学方程式为______________、_____________;
②在煤矿中直接添加一种物质,可有效减少煤矿燃烧产生的SO2,该物质是___;
③石膏的工业生产中的用途是_________________(写出一种用途即可)。
(3)煤经过___________(填加工方法)可以得到焦炉煤气、煤矿焦油和焦炭。煤焦油经过_______(填加工方法)可得到芳得族化合物。煤矿也可以用氢化法转化燃油,氢化法的本质是______________。
(4)煤可以液化转化为CH3OH,有人设计出在KOH溶液中用电极表面镀一层细小的铂粉做电极,铂吸附气体的能力强,性质稳定,利用CH3OH和O2构成的燃料电池的能量转化主要形式是 ?,负极反应式为 ?,电极表面镀铂粉的原因为? 。
4、填空题 焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:

已知:反应Ⅱ包含2NaHSO3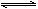 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式:?。
(2)“灼烧”时发生反应的化学方程式:?。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:?。
(4)副产品X的化学式是:?;可循环利用的物质是:_________和_______。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为?。
5、选择题 下列物质中,作为燃料时对空气没有污染的是(? )
A.原油
B.氢气
C.汽油
D.煤