1、填空题 工业上制造普通玻璃的主要原料是______________,主要设备是______________,主要原料熔化后,发生的主要化学反应是___________________________________________、________________________________。普遍玻璃的成分是____________________________。
参考答案:纯碱、石英、石灰石;玻璃熔炉;SiO2+Na2CO3 Na2SiO3+CO2↑;SiO2+CaCO3
Na2SiO3+CO2↑;SiO2+CaCO3 CaSiO3+CO2↑;
CaSiO3+CO2↑;
Na2SiO3、CaSiO3、SiO2
本题解析:
本题难度:一般
2、填空题 (1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”(侯氏制碱法)两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式?;
②写出“联合制碱法”有关反应的化学方程式________________。
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同______________________________________;
(2)钢铁工业对促进经济和社会发展起了重要作用。
① 炼钢时,加入硅、锰和铝的目的是_______________________。
② 不锈钢含有的Cr元素是在炼钢过程的氧吹____(填“前”或“后”)加入。
③ 炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。
参考答案:(1)①2NH4Cl+Ca(OH)2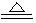 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl? 2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
③氨碱法中的二氧化碳来源于石灰石的煅烧,联合制碱法中的二氧化碳来自于合成氨中工业中的废气。
(2)①脱氧调整钢的成分? ②后? ③ CO?燃料或还原剂
本题解析:(1)①氨碱法中的回收氨而使石灰乳与副产物氯化铵反应,从而产生大量的废渣,2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②联合制碱法的有关反应的化学方程式是:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl? 2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
③氨碱法中的二氧化碳来源于石灰石的煅烧,联合制碱法中的二氧化碳来自于合成氨中工业中的废气。
(2)①炼钢时,加入硅、锰和铝的目的是脱氧调研钢的成分
②因为铬易被氧化,为了防止铬被氧化,不锈钢含的铬在炼钢的过程的吹氧后,如果在吹氧前加入铬,会形成炉渣而被除去。
③炼铁和炼钢的过程中,CO主要起的作用是还原剂,所以尾气中含有污染物CO,应对CO进行处理。
本题难度:一般
3、计算题 (经典回放)
阅读下列短文,完成问题:
汽车作为曾经推动人类文明向前跃进的现代社会的产物,在给人类的生活带来便捷舒适的同时,对自然生态环境的恶化也有难以推卸的责任。据6月15日我市政府发布的“2000年厦门环境状况公报”称:厦门大气污染主要来源于工业污染和汽车尾气,99%的一氧化碳和一氧化氮的排放来源于汽车尾气。我市近几年来汽车持有量的增长达20%,虽然空气质量居全国第四,但环保仍面临如汽车污染等问题的考验。
另据报道:将氢气应用于汽车发动机的技术已在我国研制成功;酒精作为燃料的汽车已在北京市、河南省使用;我市也有一部分汽车改用液化气作为燃料。
(1)汽车尾气中的大气污染物有(写化学式)____________,____________。
(2)我市将部分汽车排气管加装三效转换器,促使一氧化碳在排气管内与空气作用转化为二氧化碳,其反应式为
____________________________________________________________。
(3)请提出我市治理汽车污染的一条合理化建议:
____________________________________。
(4)就目前的情况看,氢气做燃料的汽车要投入使用前,你认为还要研究解决的问题有:_____________________________________________________________________________。
(5)若实验用氢气汽车运行1 km,需要2 858 kJ能量。现这辆汽车在我市环岛路上走一圈(约30 km),需要____________g氢气。(已知每克氢气燃烧放出142.9 kJ能量。)
参考答案:
(1)CO? NO
(2)2CO+O2====2CO2
(3)这是一道开放性问题,可能的答法有如下几类:A选项限制汽车的发展,如限制私人汽车的发展,发展公共交通。B选项将汽车全部加装三效转换器等汽车环保装置,使目前汽车尾气得到净化。C选项改用清洁环保型燃料,如酒精、液化气等。D选项使用电力汽车。E选?项加快研制如氢气等新型环保能源,研制核能的民用化等;
(4)这是一道开放性问题,可能的答法有如下几类:A选项关于氢气的来源问题,如何获得大量而廉价的氢气?B选项关于氢气的保存和运输问题,如何储存和运输大量的氢气?C选项关于氢气在汽车上的使用问题,如汽车上如何灌装一定量的氢气?D选项关于氢气使用的安全问题,如何防止氢气在使用、储存和运输时与空气混合爆炸?
(5)600
本题解析:
此题是以环境保护和能源开发情境设置的试题,其中(3)和(4)为开放性试题。通过此题,使学生认识到我国环境污染的严重性,认识到人类文明与环境恶化的双重性,了解我国新能源开发的迫切性,更强调了公民治理环境的参与性,增强了学生将所学知识运用到环保建设中的意识,使学生养成运用知识研究问题、解决问题的思想方法,让学生成为环保的参与者,体验创造的价值和魅力,激发创新精神。
本题难度:简单
4、选择题 下列说法正确的是
[? ]
A.由于水泥是一种固体粉末,随便找一个东西盛起来就可以储存
B.建筑三峡大坝要用到1. 082×107 t的水泥,为节约开支,购买价格低廉的水泥
C.只要是水泥就可以用来建大厦
D.在具体的建筑中,所用水泥的强度等级要符合
参考答案:D
本题解析:
本题难度:简单
5、填空题 (5分)海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获得氯化钠。将海水进行?可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是_________________。(用序号填一种合理组合)。
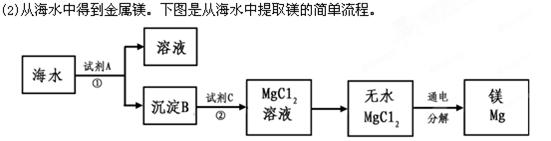 上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
由无水MgCl2制取Mg的化学方程式为_____________________________________。海
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:___________________________________________________________。
参考答案:蒸发结晶? ①③②⑤⑦④⑥(或①⑤③②⑦④⑥或①③⑤②⑦④⑥)
(3) Mg(OH)2?MgCl2通电?Mg+Cl2↑?后者是经过富集和分离后的溶液(或海水中含有氯化钠等多种溶质,氯化镁的浓度很低)
本题解析:略
本题难度:一般