1������� T��ʱ����һ�����Ϊ2L�������У�A������B���巴Ӧ����C���壬��Ӧ������A��B��CŨ�ȱ仯��ͼ��ʾ��
��1��д���÷�Ӧ�ķ���ʽ��______
��2��������¶��¸÷�Ӧ��ƽ�ⳣ����______
��3����֪��K��300�棩��K��350�棩���÷�Ӧ��______�ȷ�Ӧ��
��4��0��4����ʱ��A��ƽ����Ӧ����Ϊ��______
��5������ƽ��ʱB��ת����Ϊ��______
��6�����������£����д�ʩ����ʹn��A��/n��C�����͵���______��
A�����뺤��?��?B��ʹ�ô���
C���ٳ���2.4molA��1.6molB?D�������¶ȣ�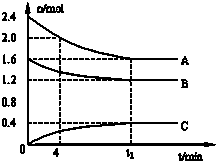
�ο��𰸣���1����ͼ����Կ�������Ӧ��A��B�����ʵ�����С��C�����ʵ������࣬��A��BΪ��Ӧ�CΪ�����
�ҡ�n��A������n��B������n��C��=0.8mol��0.4mol��0.4mol=2��1��1����Ӧ�Ļ�ѧ����ʽΪ��2A+B
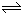
C��
�ʴ�Ϊ��2A+B
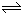
C��
��2��k=c(C)c2(A)?c(B)=0.2mol/L(0.8mol/L)2?0.6mol/L=0.52��mol/L��-2���ʴ�Ϊ��0.52��
��3��K��300�棩��K��350�棩��˵���¶����ߣ�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ���ʴ�Ϊ���ţ�
��4��0��4����ʱ��A��ƽ����Ӧ����Ϊ��v��A��=2.4mol-2.0mol2L4min=0.05mol?L-1?min-1���ʴ�Ϊ��0.05mol?L-1?min-1��
��5������ƽ��ʱB��ת����Ϊ��1.6mol-1.2mol1.6mol��100%=25%���ʴ�Ϊ��25%��
��6��n(A)n(C)���ͣ�˵��ƽ��������Ӧ�����ƶ���
A�����뺤���������ʵ����ʵ���Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�����A����?
B��ʹ�ô�����ƽ�ⲻ�ƶ�����B����
C���ٳ���2.4molA��1.6molB����Ӧ���Ũ������ƽ��������Ӧ�����ƶ�����C��ȷ��
D�������¶ȣ�ƽ��������Ӧ�����ƶ�����D��ȷ��
�ʴ�Ϊ��CD��
���������
�����Ѷȣ�һ��
2��ѡ���� һ�������£����ݻ�Ϊ10L���ܱ������У�1mol X��1mol Y�������·�Ӧ��2X��g��+Y��g��?Z��g������60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ���ǣ�������
A����XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.001mol/��L?s��
B���������ݻ���Ϊ20L��Z��ƽ��Ũ��Ϊԭ����1/2
C���������ǿ��������Ӧ���������淴Ӧ���ʼ�С
D���������¶ȣ�X���������������÷�Ӧ�ġ�H��0
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� ��ͼI��ʾ���ס���֮��ĸ���K�ͻ���F�����������ƶ���F��ѹ���㶨�����г���2mol?A��1mol?B�����г���2mol?C��1mol?He����ʱKͣ��0������һ�������·������淴Ӧ��2A��g��+B��g��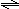 2C��g������Ӧ�ﵽƽ����ٻָ���ԭ�¶ȣ�������˵����ȷ���ǣ�? ��
2C��g������Ӧ�ﵽƽ����ٻָ���ԭ�¶ȣ�������˵����ȷ���ǣ�? ��
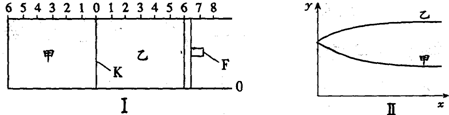
A���ﵽƽ��ʱ������K����ͣ����0�̶�����2��4֮��
B�����ﵽƽ��ʱ������K����ͣ�������1����������C��ת����С��50%
C�����ﵽƽ��ʱ������K����ͣ��������2����������F����ͣ�����Ҳ�Ŀ̶ȴ���4
D����ͼII��ʾ����x���ʾʱ�䣬��y��ɱ�ʾ�ס���������������������ʵ�����A�����ʵ���
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� �Դﵽƽ��״̬�Ŀ��淴Ӧ��A+B?C+D����t1ʱ����ѹǿ�������淴Ӧ���ʱ仯��ͼ��ʾ���ʹ�����Ӧ���ʣ�t����ʱ�䣩�������й�A��B��C��D��״̬��������ȷ���ǣ�������
A��A��B��C�����壬D��������
B��A��B�����壬C��D��һ��������
C��C��D�����壬A��B��һ��������
D��C��D��һ�������壬A��B����������
