1、选择题 以下有关原子半径的叙述正确的是( )
A.原子半径的大小取决于原子核外电子层数
B.原子半径的大小取决于核电荷数
C.同周期主族元素,原子半径随原子序数增大而增大
D.同主族元素,原子半径随原子序数减小而减小
参考答案:A.原子半径大小由核电荷数、核外电子数、电子层数决定,故A错误;
B.原子半径大小由核电荷数、核外电子数、电子层数决定,故B错误;
C.同周期元素,原子电子层数相同,其原子半径随核电荷数的增加而减小,故C错误;
D.同主族元素,电子层越多原子半径越大,即原子半径随原子序数减小而减小,故D正确,
故选D.
本题解析:
本题难度:一般
2、选择题 某主族元素R的最高正价与最低负价的代数和等于2,则该族元素最高价氧化物的水化物的分子式应是
[? ]
A.H2RO3
B.H2RO4
C.H3RO4
D.HRO2
参考答案:C
本题解析:
本题难度:简单
3、填空题 材料是科学技术进步的关键,是科学技术和社会发展的物质基础。材料的发展不仅影响了人类的昨天和今天,而且还将影响到人类的明天。请回答以下与材料有关的问题。
(1)无机非金属材料。单晶硅是一种比较活泼的非金属元素,是晶体材料的重要组成部分,处于新材料发展的前沿。其主要用途是用做半导体材料和利用太阳能光伏发电、供热等。单晶硅的制备方法如下:
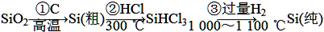
①写出步骤①的化学方程式:______________________。
②已知以下几种物质的沸点:
物质
| SiHCl3
| SiCl4
| HCl
|
沸点
| 33.0 ℃
| 57.6 ℃
| -84.7 ℃
|
在步骤②中提纯SiHCl3所进行的主要操作的名称是________。
(2)金属材料。金属材料是指金属元素或以金属元素为主构成的具有金属特性的材料的统称。包括纯金属、合金和特种金属材料等。
①下列物质中不属于合金的是( )。
A.钢铁 ?B.青铜 ?C.硬铝 ?D.水银
②铜器制品常因接触空气中的O2、CO2和H2O而易生成铜锈。试写出保护铜制品的方法:___________________________________________________。
(3)纳米材料,胶体粒子的直径大约是________,与纳米材料的尺寸相当。实验室制取Fe(OH)3胶体溶液的方法是_________________________________,
用________方法消除胶体中的浑浊,根据________现象证明胶体已经制成。实验中必须要用蒸馏水,而不能用自来水,其原因是____________________。
(4)磁性材料。某磁性粉末材料是一种复合型氧化物,为测定其组成,现称取6.26 g样品,将其全部溶于过量稀HNO3,加入过量Na2SO4溶液,生成4.66 g白色沉淀、过滤、在滤液中加入过量NaOH溶液,生成红褐色沉淀,将沉淀过滤、洗涤、灼烧后得3.20 g固体。①该磁性粉末中氧元素的质量分数为________;②该材料的化学式为________。
参考答案:(1)①SiO2+2C Si+2CO↑ ②蒸馏
Si+2CO↑ ②蒸馏
(2)①D ②在干燥的环境下保存
(3)1~100 nm;在沸腾的蒸馏水中逐滴加入少量FeCl3饱和溶液,待溶液呈红褐色,停止加热,即制得胶体; 过滤; 丁达尔;自来水中含较多的阴离子和阳离子,能中和胶体粒子的电性,易使制备的胶体马上发生凝聚,导致实验失败
(4)①20.45% ②BaO・Fe2O3
本题解析:(1)提纯SiHCl2可利用沸点差异,用蒸馏的方法。
(2)硬铝是由Al、Cu、Mg、Mn、Si形成的合金,黄铜是Cu-Zn合金,钢铁是Fe与其他元素形成的合金。因此唯一不属于合金的是水银。
(3)胶体粒子直径的范围是:1~100 nm;利用FeCl3的水解反应制取Fe(OH)3胶体:在沸腾的蒸馏水中逐滴加入少量FeCl3饱和溶液,待溶液呈红褐色,停止加热,即制得胶体;难溶固体不能透过滤纸,胶体可透过滤纸,所以用过滤的方法,可消除胶体中的浑浊;胶体具有丁达尔现象,其它分散系不具备,所以用丁达尔现象可证明胶体已经制成;因为自来水中含较多的阴离子和阳离子,能中和胶体粒子的电性,易使制备的胶体马上发生凝聚,导致实验失败,所以不能用自来水制备胶体。
(4)①n(BaSO4)=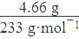 =0.02 mol,
=0.02 mol,
m(Ba)=137 g・mol-1×0.02 mol=2.74 g。
滤液中加入过量NaOH溶液,生成红褐色沉淀为Fe(OH)3沉淀。洗涤,灼烧后得3.20 g固体。此固体应是Fe2O3,则
n(Fe2O3)= =0.02 mol,
=0.02 mol,
m(Fe)=56 g・mol-1×0.02 mol×2=2.24 g。
复合氧化物中氧元素的质量=6.26 g-2.74 g-2.24 g=1.28 g。
则氧元素的质量分数=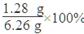 =20.45%。
=20.45%。
②1.28 g氧元素的物质的量是:
n(O)= =0.08 mol。
=0.08 mol。
由以上计算知,复合氧化物中钡原子、铁原子、氧原子的物质的量之比是1∶2∶4,它们的原子个数比也是1∶2∶4。故该复合氧化物可表示为BaO・Fe2O3。
本题难度:一般
4、推断题 Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布为msnmpn;
③R原子核处L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+的核外电子排布式是___________。
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3,分子提供的____________形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是____________。
a.稳定性:甲>乙,沸点:甲>乙
b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙
d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为____________(用元素符号 作答)。
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为____________
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____________(填晶体类型)。
参考答案:(1)ls22s22p63s23p63d9
(2)孤对电子(孤电子对)
(3)b
(4)Si<C<N
(5)3:2
(6)原子晶体
本题解析:
本题难度:困难
5、选择题 下列叙述中不正确的是( ? )
A.C60与石墨是同素异形体
B.H(氕)、D(氘)T(氚)互为同位素
C.甲烷和戊烷是同系物
D.2-甲基丁烷与丁烷互为同分异构体
参考答案:D
本题解析:
本题难度:一般