1、选择题 某元素X的气态氢化物的化学式为XH3,则下列叙述中不正确的是
[? ]
A.该元素原子的最外电子层上有5个电子
B.该元素最高价氧化物的化学式为X2O5
C.该元素在元素周期表中位于第VA族
D.该元素最高价氧化物对应的水化物的化学式为H2XO3
参考答案:D
本题解析:
本题难度:简单
2、选择题 运用元素周期律分析,下列说法错误的是
A.Ra是第7周期、ⅡA族的元素,Ra(OH)2的碱性比Mg(OH)2的碱性强
B.As是第4周期、ⅤA族的元素,AsH3的还原性比NH3的还原性弱
C.Cs的原子半径比Na的原子半径大,Cs与水反应比Na与水反应更剧烈
D.Cl的核电荷数比Al的核电荷数大,Cl的原子半径比Al的原子半径小
参考答案:B
本题解析:此题考查同周期主族元素性质递变规律.AsH3的还原性强于NH3.
本题难度:简单
3、选择题 下列各粒子半径依次增加的是( )
A.Cs+K+Mg2+Al3+
B.F? F-Cl-Br-
C.Ca2+K+S2-Cl-
D.Al? Al3+Mg? K
参考答案:A、Cs+、K+是同一主族相同类型的阳离子,核电荷数越大,离子半径越大,K+的电子层数大于Mg2+、Al3+,所以钾离子半径大于镁离子、铝离子半径,故A错误.
B、F-、Cl-、Br-是同一主族相同类型的阴离子,核电荷数越大,离子半径越大,所以氟离子半径<氯离子半径<溴离子半径,氟原子半径小于氟离子半径,故B正确.
C、电子层结构相同的离子的半径与其原子序数成反比,Ca2+、K+、S2-、Cl-电子层结构相同,所以钙离子半径<钾离子半径<氯离子半径<硫离子半径,故C错误.
D、钾原子电子层数大于铝原子、镁原子电子层数,所以钾原子半径大于铝原子、镁原子半径,镁、铝属于同一周期,根据元素周期律知,镁原子半径大于铝原子半径,同一元素的原子半径大于阳离子半径,所以铝离子半径小于铝原子半径,故D错误.
故选B.
本题解析:
本题难度:简单
4、选择题 根据元素周期表知识,下列说法不正确的是( )
A.最外层电子数为3~7的原子一定是主族元素的原子
B.短周期元素X、Y,若X、Y的最外层电子数相同,且X原子半径小于Y,当X(OH)n为强碱时,Y(OH)n必为强碱
C.短周期元素A、B,若A、B电子层数相同,且A原子半径小于B,当HnAOm为强酸时,B必为活泼非金属元素
D.2007年3月21日,中国科学技术名词审定委员会公布了111号元素Rg的中文名称,111号元素属于过渡元素
参考答案:C
本题解析:
本题难度:简单
5、推断题 (三选一)【物质结构与性质】
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数:A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M 层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
(1)A的简单氢化物分子中中心原子采取____杂化,E的最高价氧化物分子的空间构型是____。
(2)B的氯化物的熔点比D的氯化物的熔点____(填“高” 或“低”),理由是____。
(3)A、B、C、D的第一电离能由小到大的顺序为 ____(用元素符号表示)。
(4)A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),则其化学式为__________(每个球均表示1个原子)。
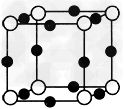
(5)F的价电子轨道表示式是_________,A、C形成的化合物具有高沸点和高硬度的性质,是一种新型无机非金属材料,则其化学式为_________。
参考答案:(1)sp3;平面三角形
(2)高;NaCl为离子晶体而SiCl4为分子晶体
(3)Na<Al<Si<N
(4)Cu3N
(5)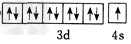 ;AlN
;AlN
本题解析:
本题难度:一般