1、实验题 (1)下图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀。
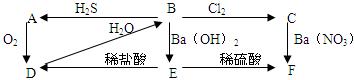
①写出B→C的化学方程式
?
②写出B→A的化学方程式
?
③C→F的离子方程式?
④E→D的离子方程式?
⑤上图中共发生了8个反应(每根箭头一个反应),其中有?个是氧化还原反应;从上图出现的物质中选出反应物,写出一个置换反应,以验证氯元素原子的氧化性比硫元素原子的氧化性强?
(2)把某黑色固体单质A加热至红热,投入到一种无色溶液B中,产生由两种气体组成的混合气体X ,将X做如下图所示的实验:

①由此可以推断:A为?;C为??和 ?
②写出D加入F生成E和G的离子方程式?
③C通入澄清石灰水时,若气体通过量则白色沉淀又会溶解,写出白色沉淀溶解的化学方程式?
?
参考答案:(1)①H2O+H2SO3+Cl2=2HCl+H2SO4 (2分)②2H2S+H2SO3=3S+3H2O (2分) ③Ba2++SO42-=BaSO4↓(2分)
④BaSO3+2H+=SO2↑+Ba2++H2O(2分)?⑤(2分)3;H2S+ Cl2=S+2HCl(2分)
(2)①碳(2分);二氧化碳和一氧化氮(2分)?
②3Cu+2NO3-+8H+=3Cu2++4H2O+2NO↑ (2分)
③CaCO3+CO2+H2O=Ca(HCO3)2(2分)
本题解析:略
本题难度:一般
2、填空题 已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).
请回答下列问题;
(1)E的化学式为______
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:______.
(3)反应①②③④中属于置换反应的是______?(填序号).
(4)反应②的离子方程式为______
(5)用石墨作电极电解500mL?X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1.6g.
请回答下列问题:
①写出电解时的阳极反应式______
②电解一段时间后转移______mol电子,溶液的pH______(填“升高”、“不变”、“降低”)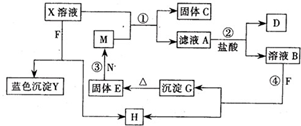
参考答案:X为中学化学中一种常见的盐,F为淡黄色固体,与X溶液反应生成蓝色沉淀Y为氢氧化铜可知,F为Na2O2;X溶液中含铜离子;M、N为常见的金属,结合N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器,E和N反应生成M可知发生了置换反应,判断N为Al,E为Fe2O3;M为Fe,结合M和含铜离子的X溶液反应生成固体C为铜,滤液A为亚铁盐溶液,加入盐酸会发生反应生成无色气体D,说明A只能是硝酸亚铁,即X溶液为硝酸铜溶液;F为过氧化钠加入到溶液B中生成H为气体单质氧气,D为无色气体一氧化氮,D在空气中会出现红棕色二氧化氮;综上所述:A、Fe(NO3)2;B、Fe(NO3)3;C、Cu;D、NO;E、Fe2O3;F、Na2O2;G、Fe(OH)3;H、O2;M、Fe;N、Al;X、Cu(NO3)2;Y、Cu(OH)2;根据判断出的物质分析回答问题:
(1)依据上述推断E为:Fe2O3,故答案为:Fe2O3
(2)将M丝插入盛有X溶液的试管中,是Fe和硝酸铜溶液反应生成铜和硝酸亚铁,反应一段时间后的现象,铁丝上附有红色物质,溶液颜色逐渐变为浅绿色;故答案为:铁丝上附有红色物质,溶液颜色逐渐变为浅绿色;
(3)反应①是铁和硝酸铜溶液反应发生置换反应;②是硝酸亚铁和盐酸发生氧化还原反应;③是氧化铝和铁反应生成铝和氧化铁,是置换反应;④是硝酸铁和过氧化钠反应,不是置换反应,所以中属于置换反应的是①③,故答案为:①③;
(4)反应②是亚铁离子在硝酸溶液中发生的氧化还原反应,离子方程式为:反应②的离子方程式反应为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(5)用石墨作电极电解500mL Cu(NO3)2溶液,观察到A电极表面有红色的固态物质Cu生成,B电极有无色气体O2生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1.6g为铜,物质的量为0.025mol;
①阳极电极反应是氢氧根离子放电,电极反应为:4OH--4e-=O2↑+2H2O;
②阳极电极反应为4OH--4e-=O2↑+2H2O;阴极电极反应为:Cu2++2e-=Cu;析出铜0.025mol,电子转移为0.05mol;电解过程中氢氧根离子减少生成氢离子,所以溶液PH降低;
故答案为:0.05;?降低;
本题解析:
本题难度:一般
3、选择题 甲、乙、丙、丁分别是NaOH、Al2(SO4)3、MgSO4、BaCl2四种物质中的一种,若将丙溶液逐滴滴入甲溶液,发现开始时无沉淀,继续滴加产生沉淀,最终沉淀不消失,若将丙溶液滴入丁溶液产生沉淀,据此推断乙溶液是( )
A.NaOH
B.Al2(SO4)3
C.MgSO4
D.BaCl2
参考答案:C
本题解析:略
本题难度:一般
4、填空题 (10分)甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。x、 A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图:

(1)用化学式表示:丙为?,C为 ??
(2)X的电子式为?。
(3)写出A与H2O反应的化学方程式:??
(4)写出B与G溶液反应的离子方程式:??
参考答案:(1) O2? Na2SO4? (2)
. .
本题解析:略
本题难度:简单
5、推断题 下图所示各物质是由1~20号元素中部分元素组成的单质或化合物,图中部分反应条件未列出。已知D、L、M为气体单质,C、E、H为气体化合物,反应②、④、⑥是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。
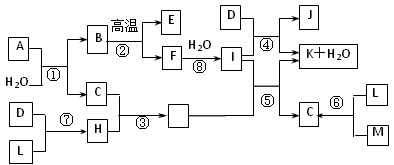
请回答下列问题:
(1)物质E的结构式为__________。
(2)属于化合反应,但不属于氧化还原反应的是__________(用编号填空)。
(3)C、H的熔沸点比较:C___H(填““>”、“<”或“=”))原因是:_________________________。
(4)物质A由三种元素组成,1molA与水反应可生成1molB和2molC,A的化学式为 ______________。
(5)在一定温度下,有甲、乙两容积相等的密闭容器。
I.向甲容器中通入3 mol M和4 mol L,反应达到平衡时,生成C的物质的量为a mol。此时,M的转化率为__________。下列能提高反应物L的转化率,但实际生产过程中并没有采用的措施是_____________。
①降低合成塔温度 ②适当增大压强 ③不断分离出产物C ④加入合适催化剂
II.向乙中通入2 mol C,欲使反应达到平衡时,各物质的浓度与I中第一次平衡时相同,则起始时还需通入__________mol M和__________mol L。
III.若起始时,向乙中通入6mol M和8mol L,达到平衡时,生成C的物质的量为b mol,则a/b______1/2(选填“>”、“<”或“=”)。
参考答案:(1)O=C=O
(2)③⑧
(3)>
(4)CaCN2
(5)I a/6 ;①II 2 ;1III <
本题解析:
本题难度:一般