1、实验题 (10分)实验室有CuO和铜粉的混合物。要测定该样品(已称得其质量为m g)中氧化铜的质量分数。用下图所示仪器装置制取H2,再用H2还原CuO,最后根据样品质量的减少和无水CaCl2质量的增加来测定样品中氧化铜的质量分数。
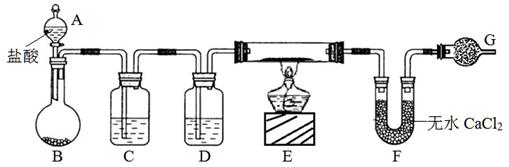
请回答:
(1)仪器中装入的试剂:D?。
(2)操作“①打开A的活塞”和“②点燃E处酒精灯”应该先进行的是?(填序号),在这两步操作之间还应进行的操作是:?。
(3)若实验中有部分CuO被还原为红色的Cu2O,对实验的影响为_____(偏大、偏小、无影响)。
(4)若测得的原质量为a g的硬质玻璃管(E),反应后质量变为b g;U型管实验后质量增加n g,由以上数据可以列出计算氧化铜质量分数的两个不同计算式:
计算式1:?;计算式2:?。
参考答案:(1)浓硫酸(1分)
(2)①(1分)收集G处的气体检验纯度(2分)
(3)偏小(2分)
(4)5(a-b)/m(2分) 40n/9m(2分)
本题解析:(1)由于生成的氢气中含有水蒸气,会干扰后面的实验,所以D中的盛放的应该是浓硫酸,用来除去水蒸气。
(2)由于装置中含有空气,所以应该首先生成氢气,将装置中的空气排尽。氢气是可燃性气体,再点燃之前,需要收集G处的气体检验纯度。
(3)若实验中有部分CuO被还原为红色的Cu2O,则生成的水就减少,因此氧化铜的质量分数就减少。
(4)根据方程式H2+CuO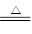 Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是
Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是 ,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是
,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是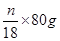 ,所以氧化铜的质量分数是40n/9m。
,所以氧化铜的质量分数是40n/9m。
本题难度:一般
2、实验题 某化学研究性学习小组探讨Fe3+和SO32-之间发生怎样的反应,请你一起参与并协助他们完成实验。
(1)提出猜想:甲同学认为发生氧化还原反应,其反应的离子方程式为__________________;乙同学认为发生双水解反应,其反应方程式为2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3;
(2)实验验证:丙同学设计了下列实验来探究反应的可能性。①为了检验所用Na2SO3是否变质,应选用的试剂是__________________。②取5mLFeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红棕色(无气泡产生,也无沉淀生成)。③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:①根据丙同学的实验得出的结论是:___________________________;②实验③中溶液变成血红色的离子方程式为_____________________________。
(4)拓展探究:①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是_______________________。②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除SO32-水解能力较CO32-小外,还有________________________________________。
参考答案:(1)2Fe3++SO32-+H2O=2Fe2++SO42-+2H+
(2)①稀盐酸、BaCl2溶液
(3)①Fe3+与SO32-同时发生氧化还原反应和双水解反应②Fe(OH)3(胶体)+3SCN-= Fe(SCN)3 +3OH-
(4)①2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑②SO32-有较强的还原性,而CO32-没有还原性
本题解析:
本题难度:一般
3、实验题 已知某混合金属粉末中,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验,探究该混合金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1 mol/L硫酸、2 mol/L硝酸、2 mol/LNaOH溶液、 20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设
假设1该混合金属粉末中除铝外还含有____________元素。
假设2该混合金属粉末中除铝外还含有_______________元素。
假设3该混合金属粉末中除铝外还含有Fe、Cu元素。
设计实验方案
基于假设3,设计出实验方案。
(2)实验过程
根据上述的实验方案,叙述实验操作、预期现象和结论。
参考答案:(1)Cu,Fe(2)
本题解析:
本题难度:一般
4、选择题 某地污水中含有Zn2+、Hg2+、Fe3+和Cu2+四种阳离子。甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下
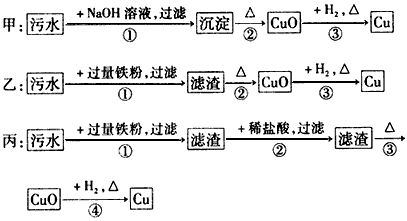
下列判断正确的是
[? ]
A.三种实验方案中都能制得纯净的铜
B.乙方案中加过量铁粉可以将四种阳离子全部还原
C.甲方案中的反应涉及置换、分解、化合、复分解四种反应类型
D.丙方案会产生环境污染
参考答案:D
本题解析:
本题难度:一般
5、实验题 (14分)氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置均略去)。回答下列问题。
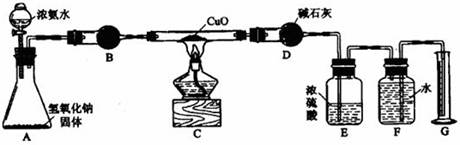
⑴写出氨气与氧化铜反应的化学方程式。
⑵在A的锥形瓶中放入NaOH固体的目的是。
⑶在干燥管B里不能选用的干燥剂是(填序号)。
A 碱石灰 B 生石灰 C 五氧化二磷 D 氢氧化钠
⑷在C的玻管中观察到的现象是?。
⑸E装置中盛装浓硫酸的目的是?。
⑹待实验完毕后,若实验测得N2的体积(折算成标准状况)为aL,则被还原的氧化铜的物质的量为?mol;若测得干燥管D增重bg,则氨分子中氮、氢的原子个数比为?。(用含a、b字母的代数式表示)
参考答案:⑴2NH3+3CuO N2+3Cu+3H2O (2分)
N2+3Cu+3H2O (2分)
⑵NaOH固体吸水及溶解产生的热利于氨气的逸出。(2分)
⑶C (2分)
⑷黑色粉末变为光亮的红色固体。(2分)
⑸将反应剩余的氨吸收,防止F中的水蒸气进入D中,引起测量误差。(2分)
⑹3a/22.4(2分) 9a/11.2b(2分)
本题解析:考查氨气的制取与性质、分子组成的测定;
实验目的之一是测定氨分子的组成,结合所给装置可看出,通过氨气还原氧化铜,氮元素转化为氮气,可用排水法来测定其体积,而氢元素转化为水,其质量可通过装置D的增重来测得。
(1)氨气中的氮元素为其最低负价,可将氧化铜还原:2NH3+3CuO N2+3Cu+3H2O
N2+3Cu+3H2O
(2)此为简易法来制备氨气;在氨水中存在平衡:NH4++OH- NH3・H2O
NH3・H2O NH3+H2O
NH3+H2O
NaOH固体溶解产生大量的热且可产生大量的OH-,均可促使氨气的生成与逸出:NH3・H2O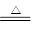 NH3↑+H2O
NH3↑+H2O
(3)氨所碱性氧化,不能用酸性干燥剂来干燥,故答案为C
(4)氧化铜为黑色粉末,被氨气还原为红色的金属铜
(5)为保证装置D只吸收反应所生成的水,可知装置E主要有两个作用,一是吸收未反应的氨气,二是防止装置F中的水气进入装置E中
(6)氨气的物质的量为a/22.4 mol,由化学方程式可知,被还原的氧化铜的物质的量为3a/22.4 mol;
水的物质的量为b/18 mol;所以氨分子中氮、氢的原子个数比为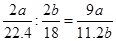
本题难度:一般