1��ѡ���� ��֪��aM2++bO2+4H+=cM3++dH2O����ϵ�� c��ֵ��
A.1
B.2
C.3
D.4
2��ѡ���� ��ij��Һ�м�������������Һ��ԭ��Һ��������Ũ���������ٵ���
A��CO32��
B��SO42��
C��Mg2��
D��Ba2��
3������� ��16�֣�±�����Ҫ�ɷ���MgCl2�������Fe2+��Fe3+��Mn2+���������ӡ���±��Ϊԭ�ϰ���ͼ��ʾ���̽������������Ƶ���������þ��
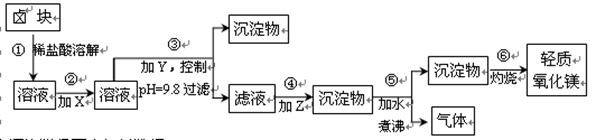
�������ϵ��±�������ݣ�
��1�� �����������������pH
| ��2�� ԭ�ϼ۸��
|
����
| ��ʼ����
| ������ȫ
| ����
| �۸�Ԫ/�֣�
|
Fe(OH)3
| 2.7
| 3.7
| a��ƯҺ����25.2%NaClO��
| 450
|
Fe(OH)2
| 7.6
| ? 9.6�~
| b��˫��ˮ����30%H2O2��
| 2400
|
Mn(OH)2
| 8.3
| 9.8
| c���ռ��98%NaOH��
| 2100
|
Mg(OH)2
| 9.6
| 11.1
| d�������99.5%Na2CO3��
| 600
|
�~Fe2+�����������״�����״���Һ�г�ȥ�����뽫����������Fe(OH)3������ʽ���ܳ�����
��Ҫ���Ʒ�������������������ɱ��ϵͣ�������ϱ��ṩ�����ϻش�
��1�������м�����Լ�X��Y��Z���ѡ�������DZ�2�е�??��ѡ���Լ���ţ���
��2������ڷ�����Ӧ�����ӷ���ʽΪ?��������з�����Ӧ�Ļ�ѧ����Ϊ???��
��3������ۿ���pH=9.8��Ŀ����???��
��4�� ����ʵ���ҽ��в��������ʵ�飬�����õ��������������š��ƾ���ơ�?��
�����ǡ�
��5����̽��Mg(OH)2�ܽ��Ե�ʵ���У�������װ������Mg(OH)2��Һ���Թ��м�������
NH4Cl���壬�������Һ�����壬���û�ѧƽ���ԭ��������Һ������ԭ
��?��
4��ѡ���� ���з�Ӧ�������ӷ�Ӧ����������������ԭ��Ӧ���ǣ�������
A��ͭ��ϡ���ᷴӦ����NO
B��MgCl2��Һ��KOH��Һ��������
C��̼��������ȼ��
D��Ũ����ε�������ع����ϲ�������
5��ѡ���� ���н���ʵ������ķ�Ӧ����ʽ��ȷ����? (����)
A���п��Ľ���Na��¶�ڿ����У����������䰵2Na��O2=Na2O2
B����AgCl����Һ�еμ�Na2S��Һ����ɫ������ɺ�ɫ2AgCl��S2��=Ag2S����2Cl��
C��Na2O2�ڳ�ʪ�Ŀ����з���һ��ʱ�䣬��ɰ�ɫճ����2Na2O2��2CO2=2Na2CO3��O2
D����NaHCO3��Һ�м�������ij���ʯ��ˮ�����ְ�ɫ����2HCO3-��Ca2����2OH��=CaCO3����CO32-��2H2O