1��ѡ���� �������У�ֻ���������Ե���
A.S
B.Na
C.Fe2+
D.Cu2+
�ο��𰸣�D
�������������������Ԫ�ػ��ϼ۵ĸߵ��ж����������ԡ���ԭ�ԣ����̬��ֻ�������ԣ���ͼ�̬��ֻ�л�ԭ�ԣ��м��̬�ļ������������л�ԭ�ԣ�
���A����Ԫ�صĻ��ϼ۴����м��̬�������������Ժͻ�ԭ�ԣ���A����
B�������ƵĻ��ϼ۴�����ͼ�̬�������л�ԭ�ԣ���B����
C��Fe2+�Ļ��ϼ۴����м��̬�����Լ������������л�ԭ�ԣ���C����
D��Cu2+�Ļ��ϼ۴������̬������ֻ�������ԣ���D��ȷ��
��ѡD��
���������⿼����������ԭ��Ӧ�ĸ���Ӧ�ã��ж��������Ի�ԭ�ԵĹ����ǣ����̬��ֻ�������ԣ���ͼ�̬��ֻ�л�ԭ�ԣ��м��̬�ļ������������л�ԭ�ԣ�
�����Ѷȣ�һ��
2��ѡ���� ��100mL���е����ʵ�����HBr��H2SO3����Һ��ͨ��0.01mol?Cl2����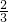 ��Br?-ת��ΪBr2����֪Br2������H2SO3������ԭ��Һ��HBr��H2SO3�����ʵ���Ũ��Ϊ
��Br?-ת��ΪBr2����֪Br2������H2SO3������ԭ��Һ��HBr��H2SO3�����ʵ���Ũ��Ϊ
A.0.0075?mol?L-1
B.0.075?mol?L-1
C.0.008?mol?L-1
D.0.08?mol?L-1
�ο��𰸣�B
���������������Br2������H2SO3����ԭ��H2SO3��Br-��������������H2SO3ΪH2SO4��H2SO3��Ӧ��ϣ�Ȼ��������Br-������Br-����ת��Br2������HBr���ֱ�������H2SO3ȫ������������ԭ��Һ��HBr��H2SO3��Ũ��Ϊcmol/L�����ݵ���ת���غ㣬�з��̼���c��ֵ��
���Br2������H2SO3����ԭ��H2SO3��Br-��������������H2SO3ΪH2SO4��H2SO3��Ӧ��ϣ�Ȼ��������Br-������2/3��Br-ת��Br2��������2/3HBr���ֱ�������H2SO3ȫ������������ԭ��Һ��HBr��H2SO3��Ũ��Ϊcmol/L�����ݵ���ת���غ㣬��
0.1L��cmol/L����6-4��+0.1L��cmol/L��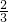 ��1=0.01mol��2��
��1=0.01mol��2��
��ã�c=0.075��
��ѡB��
���������⿼��������ԭ��Ӧ���㣬�Ѷ��еȣ�����Br2������H2SO3?�жϻ�ԭ��H2SO3��Br-�ǹؼ���
�����Ѷȣ�����
3��ѡ���� ʵ����������һ�ֽ����������ӣ���������Դ��ˮ��������ӣ�����Һ������Һ���������ӵ�Ũ�Ⱦ�Ϊ1mol?L-1���ܴﵽ��Ŀ����
A.Al3+��Cu2+��SO42-��Cl-
B.Mg2+��K+��SO42-��NO3-
C.ClO-��I-��K+��Na+
D.Mg2+��HCO3-��SO42-��OH-
�ο��𰸣�B
�����������������������֮�䲻�ܽ�����ɳ��������塢ˮ�ȣ����ܷ���������ԭ��Ӧ�ȣ����ܴ������棬����ϵ���غ������
���A����������֮�䲻��Ӧ���ܹ��棬���������ӵ�Ũ�Ⱦ�Ϊ1mol?L-1����ѭ����غ㣬��A��ѡ��
B����������֮�䲻��Ӧ���ܹ��棬���������ӵ�Ũ�Ⱦ�Ϊ1mol?L-1��ѭ����غ㣬��Bѡ��
C��ClO-��I-����������ԭ��Ӧ�ȣ����ܴ������棬��C��ѡ��
D��Mg2+��HCO3-��OH-������ɳ�����ˮ�����ܹ��棬��D��ѡ��
��ѡB��
���������⿼�����ӵĹ��棬��ȷ����֮��ķ�Ӧ������غ��ǽ����Ĺؼ���ע��ѡ��C�е�������ԭΪ�����ѵ㣬��Ŀ�Ѷ��еȣ�
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��д��ȷ����
A.���⻯����Һ��ⷴӦ��HS-+I2�TS��+2I-+H+
B.�����ʵ���Ũ�ȵ�FeBr2��CuCl2�����Һ�ö��Ե缫�����������ķ�Ӧ��Fe2++2Cl-?Fe+Cl2��
C.ʯ��ʯ���ڴ��CaCO3+2H+�TCa2++CO2��+H2O
D.����ʯ��ˮ�м��������Ca��HCO3��2��Һ��Ca2++OH-+HCO3-�TCaCO3��+H2O
�ο��𰸣�AD
���������������A�����⻯����Һ��ⷢ��������ԭ��Ӧ���ɵ⻯�ơ�S��HI��
B��������ͭ���ӡ������ӷŵ磻
C������Ϊ���ᣬ�����ӷ�Ӧ�б�����ѧʽ��
D������ʯ��ˮ�м��������Ca��HCO3��2��Һ����̼��Ƴ�����ˮ��
���A�����⻯����Һ��ⷴӦ�����ӷ�ӦΪHS-+I2�TS��+2I-+H+����A��ȷ��
B�������ʵ���Ũ�ȵ�FeBr2��CuCl2�����Һ�ö��Ե缫�����������ķ�Ӧ�����ӷ�ӦΪ
Cu2++2Br-? Cu+Br2����B����
Cu+Br2����B����
C��ʯ��ʯ���ڴ�������ӷ�ӦΪCaCO3+2HAc�TCa2++CO2��+H2O+2Ac-����C����
D������ʯ��ˮ�м��������Ca��HCO3��2��Һ�����ӷ�ӦΪCa2++OH-+HCO3-�TCaCO3��+H2O����D��ȷ��
��ѡAD��
���������⿼�����ӷ�Ӧ����ʽ����д����ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ�������Ϥ���ӷ�Ӧ����ʽ����д���������DΪ�״��㣬��Ŀ�ѶȲ���
�����Ѷȣ�һ��
5��ѡ���� ��ˮ��Һ���ܴ��������һ��������
A.H+��K+��Cl-��CO32-
B.Ba2+��Mg2+��SO42-��Cl-
C.ClO-��I-��K+��Na+
D.Mg2+��K+��SO��NO
�ο��𰸣�D
���������������������֮�䲻�����κη�Ӧ�������ɳ��������塢������ʣ�����������ԭ��Ӧ������ˮ�ⷴӦ����ɴ������森
���A��H+�뷴Ӧ�����ܴ������棬��A����
B��Ba2+��SO42-��Ӧ���ɳ��������ܴ������棬��B����
C��ClO-��I-����������ԭ��Ӧ�����ܴ������棬��C����
D������֮�䲻�����κη�Ӧ���ɴ������棬��D��ȷ��
��ѡD��
���������⿼�����ӹ������⣬��Ŀ�ѶȲ���ע��������ӵ������Լ����ܷ�����Ӧ�����ͣ�ѧϰ��ע����ۣ�
�����Ѷȣ�һ��