1��ѡ���� �����£���200ml pH��a��CuSO4��K2SO4�Ļ����Һ��ʯī�缫���һ��ʱ�䣬�����Һ��PH��Ϊb����Һ����ı仯���Բ��ƣ�����������������ʼ�շ���ֻ��һ���缫���������������˵��������� (? )
A����ʹ�������Һ�ָ������ǰ��Ũ�ȿ�����Һ�м���9.8��(10-b��10-a)g Cu(OH)2
B��b��a��7
C������������������O2�����������״���£�Ϊ��1.12��(10-b��10-a)L
D�������缫��ӦʽΪ��Cu2+��2e-��Cu
�ο��𰸣�A
������������⿼���˵��ʱ���ӵķŵ�˳�缫��Ӧʽ��������ҺPH�ı仯����ԭ�ķ������йص��ļ��㣬��Ҳ������߿����ⳣ�漰�����ݡ�����Ĺؼ��ǿ�����������������ʼ�շ���ֻ��һ���缫��������������Ͼ�֪������������������������������������ͭ���ʣ�D����ȷ��C�����Ҳ��ȷ��Ҫ�ָ����ǰ����Һ��Ҫ��������ͭ������ת��Ϊ����ͭ��̼��ͭ�����Բ��ܼ�������ͭ��A���Ǵ���ģ���������ͭˮ��a��7�����ת�������b��a��B����ȷ��
�����Ѷȣ�һ��
2������� ��7�֣�KMnO4��һ�ֳ��õ�ǿ����������ҵ�ϳ��õ�ⷨ�Ʊ����ܷ�ӦΪ2K2MnO4+2H2O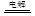 2 KMnO4+2KOH+H2������ش��������⣺
2 KMnO4+2KOH+H2������ش��������⣺
��1�����ʱ���ֱ��ò������������缫���ϣ���������Ϊ �����������������ͬ�������ϡ�
��2��ͨ��������Һ��K+ �� ���ƶ���MnO42�� �� ���ƶ���
��3�����һ��ʱ�����������Һ�еμӷ�̪�� ���ʺ�ɫ��
��4�������Ϸ��� �����������ԭ������Ӧ���ü��ĵ缫��ӦʽΪ ��
�ο��𰸣�����7�֣����缫��Ӧʽ2���⣬����ÿ��1�֣�
��1���� ��2�������� ��3���� ��4������ MnO42��?e��="=" MnO4��
�����������1�����ʱ���ֱ��ò������������缫���ϣ����ݷ���ʽ��֪���ʱ�����ʧȥ����ת��Ϊ������أ������缫�ǻ��Ե缫������������Ϊ�������ϡ�
��2�������������õ����ӣ����������������ƶ������ͨ��������Һ��K+ �������ƶ���MnO42�� �������ƶ���
��3�������������ӷŵ磬����������ͬʱ�������������ӣ���˵��һ��ʱ�����������Һ�еμӷ�̪�������ʺ�ɫ��
��4�������������������ʧȥ���ӣ�����������Ӧ���ü��ĵ缫��ӦʽΪMnO42��?e��="=" MnO4����
���㣺����绯ѧԭ����Ӧ��
�����Ѷȣ�һ��
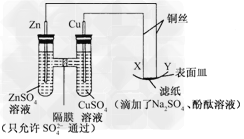
3��ѡ���� ��ͼ��ʾ������������ȷ����
[? ]
A��YΪ������������ԭ��Ӧ
B��XΪ����������������Ӧ
C��Y����ֽ�Ӵ�������������
D��X����ֽ�Ӵ������
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� ��ҵ��Ϊ�˴�������Cr2O72-���Թ�ҵ��ˮ����������Ĵ�������������ҵ��ˮ��������NaCl����FeΪ�缫���е�⣬����һ��ʱ�䣬��Cr(OH)3��Fe(OH)3�������ɣ���ҵ��ˮ�и��ĺ����ѵ����ŷű�����ش��������⣺
?��1������������Ӧ�ĵ缫��Ӧʽ��������______________ ��������______________ ��
?��2��д��Cr2O72-��ΪCr3+���ӷ���ʽ��_______________________ ��?
?��3����ˮ�����Ա�Ϊ���Ե�ԭ����_____________________________ ��
?��4��________(��ܡ����ܡ�)����ʯī�缫��ԭ����_________________ ��
�ο��𰸣�
��1��Fe�D2e-��Fe2+��2H+��2e-��H2��
��2��Cr2O72-��6Fe2+��14H+ ��2Cr3+��6Fe3+��7H2O
��3��H+�����������ϵõ��ӳ�ΪH2����������Cr2O72-��Fe2+�ķ�ӦҲ������H+��ʹ����Һ���Ա�Ϊ���ԣ��������Ա�Ϊ���ԣ�Cr3+��3OH-��Cr(OH)3��, Fe3+��OH-��Fe(OH)3��
��4�����ܣ�������ʯī�缫����������ΪCl2��������Fe2+��û��Fe2+�Ļ�ԭ���ã� Cr2O72-�Ͳ��ܱ�ΪCr3+��Ҳ�Ͳ���ת����Cr(OH)3����������ȥ��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ҵƷ����������Һ�к���ijЩ����������ʣ��������ӽ���Ĥ������ᴿ��������װ�������ӽ���Ĥ��ֻ����������ͨ�������乤��ԭ����ͼ��ʾ������˵������ȷ����
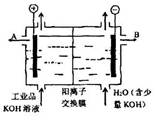
A���������Ͽ�����Fe������������ʲ�����缫�Ϸŵ�
B���õ��۵�������ӦʽΪ��4OH�D�D 4e��= 2H2O+O2��
C��ͨ��õ�������������ҺpH���С
D����ȥ���ʺ�����������Һ�ӳ���B����
�ο��𰸣�C
����������õ��ط�Ӧ��ʵ���ǵ��ˮ��������Ӧ��2H2O+2e-=2OH-+H2��,ͨ�����������pH����������Ӧ��2H2O-4e-=4H++O2��,K+ͨ�������ӽ���Ĥ���������������OH-����KOH��Һ����ʽ��B�ڵ������ɴ˿��Եó�A��B��D��ȷ��C����ѡC��
�����Ѷȣ�һ��