1、填空题 pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
(1)写出正盐的化学式:______________________________。
(2)若该盐中只有一种离子水解,该离子水解的离子方程式为_________________________。
(3)简述该混合液呈碱性的原因。
参考答案:(1)BnAm
(2)Bm++mH2O B(OH)m+mH+
B(OH)m+mH+
(3)等体积混合时,酸中的n(H+)与碱中的n(OH-)(溶液中)完全中和,pH=8说明碱为弱碱,H++OH-====H2O后,继续电离。
本题解析:因为酸的pH与碱的pH之和等于14,等体积混合后pH=8>7,说明碱为弱碱,Bm+水解的离子方程式是:Bm++mH2O B(OH)m+mH+。HnA与B(OH)m等体积混合后,已电离的H+与OH-完全中和,弱碱继续电离产生OH-,显碱性。
B(OH)m+mH+。HnA与B(OH)m等体积混合后,已电离的H+与OH-完全中和,弱碱继续电离产生OH-,显碱性。
本题难度:简单
2、填空题 (6分)化合物SOCl2是―种液态化合物,沸点为77℃。在盛有10mL水的锥形瓶中,小心地滴加8滴~10滴SOC12,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。该气体可使滴有品红试液的滤纸褪色。轻轻振荡锥形瓶,等白雾消失后,往溶液中滴加AgNO3溶液,有不溶于HNO3的白色凝乳状沉淀析出。
(1)根据上述实验,写出SOCl2和水反应的化学方程式:_________________________
(2)AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3・6H2O混合共热,可得到无水AlCl3,其原因是_________________________________________________。
参考答案:(1)SOCl2 + H2O = SO2 + 2HCl
(2)SOCl2与水反应既减少了水的量,生成HCl又抑制AlCl3水解。
本题解析:(1)将SOCl2滴到水中,产生能是品红褪色的刺激性气味的气体,则该气体是SO2,得到的溶液加AgNO3溶液产生不溶于HNO3的白色沉淀,说明溶液中有Cl-,所以SOCl2与水反应的化学方程式为:SOCl2 + H2O = SO2 + 2HCl。
(2)AlCl3+3H2O Al(OH)3+3HCl,加热蒸干灼烧HCl所以得不到AlCl3,当与SOCl2混合共热时,SOCl2与水反应既减少了水的量,生成HCl又抑制AlCl3水解。
Al(OH)3+3HCl,加热蒸干灼烧HCl所以得不到AlCl3,当与SOCl2混合共热时,SOCl2与水反应既减少了水的量,生成HCl又抑制AlCl3水解。
点评:本题主要考查获得信息的能力,通过题中所给信息作答。
本题难度:一般
3、选择题 下列混合溶液中,各离子浓度的大小顺序正确的是?(?)
A.10 mL 0.1 mol・L-1氨水与10 mL 0.1 mol・L-1盐酸混合,
c(Cl-)>c(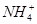 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.10 mL 0.1 mol・L-1NH4Cl溶液与5 mL 0.2 mol・L-1NaOH溶液混合,
c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.10 mL 0.1 mol・L-1CH3COOH溶液与5 mL 0.2 mol・L-1NaOH溶液混合,
c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10 mL 0.5 mol・L-1NaOH溶液与6 mL 1 mol・L-1盐酸混合,