1、选择题 下列实验操作中正确的是( )
A.I2易溶于酒精,可以用酒精萃取溴水中的溴
B.蒸馏时,冷凝水应从冷凝管的上口进水
C.分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
D.称量时,试剂应该直接放在天平的左盘上称量
参考答案:C
本题解析:
本题难度:简单
2、实验题 实验室可用如图装置将CO2和CO进行分离和干燥,已知a、b均为活塞,请回答
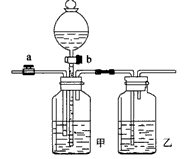
(1)甲瓶中应装____溶液,乙瓶中应装 ___,分液漏斗中应装____,
(2)当CO2和CO混合气体通过该装置时,先分离得到的是___气体,活塞操作是:关闭___,打开___;然后得到___气体,活塞操作是:关闭____,打开____。
参考答案:(1)碳酸钠溶液 ;浓硫酸 ;稀硫酸
(2)CO ;b ;a ;CO2 ;a ;b
本题解析:
本题难度:一般
3、选择题 氯气和水反应生成HCl和HClO,欲从反应混合物中分离出HClO溶液,下列方法可选的是
[? ]
A.加硫酸钙,充分反应后蒸馏
B.加碳酸钙,充分反应后蒸馏
C.加磷酸钙,充分反应后蒸馏
D.加氯化钙,充分反应后蒸馏
参考答案:B
本题解析:
本题难度:一般
4、实验题 发酵粉是一种生产面制品和膨化食品的化学膨松剂,由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成。某研究性学习小组为探究不同品牌的发酵粉的化学成分,进行如下实验。
【提出假设】
(1)假设1:由小苏打和臭粉组成;
假设2:由小苏打和明矾组成;
假设3:由________________组成。
【方案与流程】
为探究某品牌的发酵粉的化学成分,某同学设计如下实验,得到如下现象:
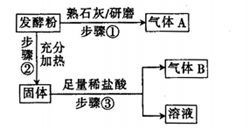
(2)该发酵粉的成分为________ (填化学式)。
(3)另一品牌的发酵粉的化学组成可能为假设2情况,请你设计实验验证,写出实验步骤、预期现象和结论。
实验步骤
|  预期现象结论 预期现象结论
|
1.取少量样品溶于稀盐酸后,将溶液分成两份
| ?
|
2.?
_______________________________________
| ?
?
|
3.?
________________________________________
| ?
?
|
?
(4)另一品牌的发酵粉的化学组成为小苏打和碳酸氢铵,为探究其化学式[化学式可表示为nNaHCO3・m NH4HCO3],称取4.05 g该产品在烧杯中溶解后,移入________配成100 mL溶液,用移液管取25.00mL溶液,滴加足量盐酸,生成的气体通入过量澄清石灰水中,生成的白色沉淀经干燥,称量为1.25 g。则该发酵粉的化学式为?。
(相对分子质量:NaHCO3:84? NH4HCO3:79? CaCO3:100)
参考答案:(17分)
(1)臭粉和明矾?(2分)
(2)NH4HCO3和NaHCO3?(2分)
(3)(8分)
实验步骤
 预期现象结论
预期现象结论
1.取少量样品溶于稀盐酸后,将溶液分成两份
?
2.用光洁无锈的铁丝(1分)蘸取其中一份溶液在酒精灯外焰灼烧,观察火焰颜色(1分)____
?火焰呈黄色(1分),该发酵粉中含有NaHCO3(1分)
3. 向另外一份溶液中滴加少量(1分)BaCl2溶液(1分)振荡
(少量、1―2滴均可得1分,?
试剂BaCl2得分,Ba(NO3)2,Ba(0H)2不得分,多写足量HCl酸化不扣分)
?有白色沉淀生成(1分),结合步骤2的结论假设二(1分)成立?
?
(4)100mL容量瓶( 2分)? 2NaHCO3・3NH4HCO3?(3分)
本题解析:(1)根据题意可知,不同品牌的发酵粉可能小苏打和臭粉组成,也可能由小苏打和明矾组成,还可能由臭粉和明矾组成,根据已知的假设1、假设2推断假设3为臭粉和明矾;(2)根据NaHCO3、NH4HCO3、Al2(SO4)2?12H2O的主要性质可知,NH4HCO3是铵盐,与熟石灰混合研磨可以放出氨气,其余两种盐与熟石灰研磨都不能放出气体,则A为NH3,发酵粉甲一定含有臭粉;NH4HCO3固体充分加热后完全变为气体逸出,NaHCO3固体充分受热变为Na2CO3固体和CO2、H2O,Na2CO3固体与盐酸易反应生成二氧化碳气体、NaCl、H2O,而Al2(SO4)2?12H2O或其水解产物Al(OH)3与盐酸混合都无气体产生,由此推断B为CO2,该发酵粉一定含有小苏打,所以甲品牌的发酵粉的主要成分是NaHCO3、NH4HCO3;(3)根据实验方案中步骤2的结论逆推可知,步骤2是用洁净的铂丝蘸取A中的溶液,再酒精灯外焰上灼烧,火焰的颜色呈黄色,证明有Na+,发酵粉中有NaHCO3;由于假设2是发酵粉由小苏打和明矾组成,则步骤3的结论是证明发酵粉有Al2(SO4)2?12H2O,根据其性质及提供试剂的性质推断,步骤3是设计实验方案证明发酵粉中含有Al3+,因此应向B试管中逐滴滴加0.1mol/LNaOH溶液,观察到白色沉淀或先产生白色沉淀后沉淀溶解,证明有Al3+,发酵粉中有明矾;(4)配制溶液主要包括称量、搅拌溶解、转移、洗涤、定容等步骤,因此配成100 mL溶液需要将溶解、冷却后的溶液移入100mL容量瓶中;25.00mL待测完全反应后,由于CO2+Ca(OH)2=CaCO3↓+H2O,则白色沉淀为碳酸钙;由于n=m/M,则n(CaCO3)=1.25g÷100g/mol=0.0125mol;由于100mL所配溶液的体积与25.00mL待测溶液之比为100/25.00,则100mL所配溶液与足量盐酸反应放出的二氧化碳为0.0125mol×100/25.00=0.05mol;设发酵粉中NaHCO3、NH4HCO3分别为xmol、ymol,由于m=n×M,则84x+79y=4.05;由于盐酸足量,NaHCO3+HCl=NaCl+CO2↑+H2O、NH4HCO3+HCl=NH4Cl+CO2↑+H2O,则xmol小苏打完全反应放出xmol二氧化碳气体,ymol碳酸氢铵完全反应放出ymol二氧化碳,则x+y=0.05;联合两个方程求解,则x=0.02,y=0.03;说明该发酵粉中小苏打和碳酸氢铵的物质的量之比为0.2∶0.3=2∶3,所以该发酵粉的组成可以表示为2NaHCO3・3NH4HCO3。
本题难度:一般
5、选择题 除去镁粉中的铝粉,应选用的试剂是
[? ]
A.稀盐酸
B.氯水
C.烧碱溶液
D.纯碱
参考答案:C
本题解析:
本题难度:一般