1������� 1molC��1molCO�ֱ���ʽ��Ӧ���ش��������⣺C��S��+1/2O2��g��=CO��g��?�ų�110.5KJ����?CO��g��+1/2O2��g��=CO2��g��?�ų�283.0KJ����? C��S��+O2��g��=CO2��g��?�ų�393.5KJ����
��1��������ݺͷ�Ӧ����˵����ú̿���ȼ���ŵ��ǣ�______��______��
��2������̼ͨ������������Ӧ����CO��g��������������Ӧ����CO2��g�������ų�������֮��______������ڡ����ڻ�С�ڣ���ͬ������̼��������ȫȼ������CO2��g�����ų�������
��3����֪C�����ʯ��S��+O2��g��=CO2��g��?�ų�����ΪQ1 C��ʯī��S��+O2��g��=CO2��g��?�ų�����ΪQ2����Q1��Q2��C�����ʯ��S��=C��ʯī��S��Ϊ______�������Ȼ���ȣ���Ӧ���ų�����Ϊ______KJ����Q1��Q2��ʾ��
�ο��𰸣���1��������ݺͷ�Ӧ����˵������֪ú̿���ȼ�ղ�����������Ͳ�������Ⱦ���ʴ�Ϊ�������������ࣻ��������Ⱦ��
��2����֪����C��S��+1/2O2��g��=CO��g����H=-110.5KJ?mol-1��
? ��CO��g��+1/2O2��g��=CO2��g����H=-283.0KJ?mol-1��
���ø�˹���ɽ���+�ڿɵã�
? ? C��S��+O2��g��=CO2��g����H=��-110.5kJ?mol-1��+��-283.0kJ?mol-1��=-393.5KJ?mol-1��
������̼ͨ������������Ӧ����CO��g��������������Ӧ����CO2��g�������ų�������֮�͵�����ͬ������̼��������ȫȼ������CO2��g�����ų���������
�ʴ�Ϊ�����ڣ�
��3���ɸ�˹���ɿ�֪��Ҫ�õ����ʯת��Ϊʯī�������仯���ɽ���������������ȫȼ��ʱ�ų�������������ɣ�
��C�����ʯ��s���TC��ʯī��s����H=-Q1J/mol-��-Q2kJ/mol��=-��Q1-Q2��kJ/mol�������ʯת��Ϊʯī�ų��������ų�������ΪQ1-Q2��
�ʴ�Ϊ�����ȣ�Q1-Q2��
���������
�����Ѷȣ�һ��
2��ѡ���� �״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
��CH3OH(g)��H2O(g)=CO2(g)��3H2(g)�� ��H=��49��0 kJ��mol-1
��CH3OH(g)��1/2O2(g)=CO2(g)��2H2(g)������H=��192��9 kJ��mol-1����
����˵����ȷ����
[? ]
A��CH3OH�ķ�Ӧ�Ȳ���������ʵ�״̬�йأ�Ҳ��μӷ�Ӧ�ķ�Ӧ������й�
B��CH3OH������ȼ���ȴ���676��7kJ��mol-1
C��CH3OHת���H2�Ĺ���ֻ����һ���Ӹ��������������Ĺ���
D�����ݢ���֪��Ӧ��CO2(g)��3H2(g)=CH3OH(l)��H2O(g) �ġ�H����49��0kJ��mol-1
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
3������� ���ǵ����Ϻ����ḻ��һ��Ԫ�أ���Ԫ�صĵ��ʺͻ������ڹ�ũҵ����������������Ҫ��;��
��1���������������仯ʾ��ͼ��
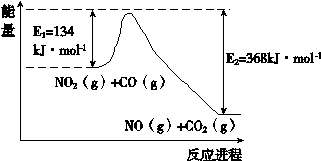
д��CO��NO2��Ӧ����NO��CO2���Ȼ�ѧ����ʽ
��2���ڹ̶�������ܱ������У��������»�ѧ��Ӧ��N2(g)+3H2(g)  2NH3 (g) ��H<0��
2NH3 (g) ��H<0��
��ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±������ж�K1 K2���>������=����<����
��3�����и�����˵���÷�Ӧ�ﵽƽ��״̬���� ������ĸ��ţ�
a�� v(H2)��="3" v(N2)��
b�� ������ѹǿ���ֲ���
c�� �����л��������ܶȱ��ֲ���
d.�� N2��H2��NH3��Ũ��֮��Ϊ1:3:2
��4��������������ˮ,������ͼʵ������֤,�ڱ�״����,��ƿ�еİ�ˮʹ��̪��졣

��ش�
���û�ѧ����˵�����ð�ˮ��ʹ��̪����ԭ�� ��
��250Cʱ����һ�����İ�ˮ�������Ϻ�pH=7����û����Һ��c(Cl-)��c(NH4+)��ϵΪ ������ĸ��ţ�
a��c(Cl-)
�ο��𰸣�
���������
�����Ѷȣ�����
4������� ��֪�Ȼ�ѧ����ʽ��
Mg��OH��2��S��=MgO��S��+H2O��g������H1=+81.5kJ/mol
Al��OH��3��S��=
Al2O3��S��+H2O��g������H1=+87.7kJ/mol
��1��Mg��OH��2��Al��OH��3����ȼ���õ���Ҫԭ����______��
��2��������Mg��OH��2��Al��OH��3����ȼ����Ч���Ϻõ���______��
�ο��𰸣���1��Mg��OH��2��Al��OH��3���ȷֽ�ʱ���մ������ȣ�ʹ�����¶��½���ʹ�����ȶ��ﵽ�Ż�����£���ֹ��ȼ�ϵ�ȼ�գ���ͬʱ���ɵ����¡��ȶ��Ժõ�MgO��Al2O3�����ڿ�ȼ����棬ʹ��ȼЧ�����ѣ�
�ʴ�Ϊ��Mg��OH��2��Al��OH��3���ȷֽ�ʱ���մ������ȣ�ʹ�����¶��½���ͬʱ���ɵ����¡��ȶ��Ժõ�MgO��Al2O3�����ڿ�ȼ����棬��ȼЧ�����ѣ�
��2��Mg��OH��2������Ч��Ϊ��81.5KJ/mol58g/mol=1.41 kJ?g-1��
Al��OH��3������Ч��Ϊ��8.7KJ/mol78g/mol=1.12 kJ?g-1��
��������Mg��OH��2��Al��OH��3���ȶ࣬������ȼЧ���Ϻõ���Mg��OH��2��
�ʴ�Ϊ��Mg��OH��2��
���������
�����Ѷȣ�һ��
5������� ����( COCl2)�����ϡ��Ƹ��ҩ�ȹ�ҵ����������;����ҵ�ϲ��ø�����CO��C12�ڻ���̿���ºϳɡ�
��1��ʵ�����п����ȷ�(CHC13)��˫��ˮֱ�ӷ�Ӧ�Ʊ��������䷴Ӧ�Ļ�ѧ����ʽΪ ��
��2����ҵ��������Ȼ��(��Ҫ�ɷ�ΪCH4)��CO2���и��������Ʊ�CO����֪CH4��H2��CO��ȼ����(��H)�ֱ�Ϊ?890.3kJ?mol?1��?285. 8 kJ?mol?1��?283.0 kJ?mol?1����1molCH4��CO2��Ӧ���Ȼ�ѧ����ʽ��
��3��COCl2�ķֽⷴӦΪCOCl2(g) Cl2(g)��CO(g) ��H=��108kJ��mol��1����Ӧ��ϵ�ﵽƽ������ʵ�Ũ���ڲ�ͬ�����µı仯״������ͬ��ʾ(��10min��14min��COCl2Ũ�ȱ仯����δʾ��)��
Cl2(g)��CO(g) ��H=��108kJ��mol��1����Ӧ��ϵ�ﵽƽ������ʵ�Ũ���ڲ�ͬ�����µı仯״������ͬ��ʾ(��10min��14min��COCl2Ũ�ȱ仯����δʾ��)��

�ٱȽϵ�2 min��Ӧ�¶�T��2�����8min��Ӧ�¶�T��8���ĸߵͣ�T��2�� ____ T��8��(�<������>����=��)
�ڱȽϷ�Ӧ��COCl2��5?6min��15?16 minʱƽ����Ӧ���ʵĴ�С��v(5?6)
v(15?16)(�<������>����=��)��ԭ���� ��
�ۼ��㷴Ӧ�ڵ�8 minʱ��ƽ�ⳣ��K= �����г�������̣����������λС����
�ο��𰸣���1�� CHCl3��H2O2 HCl��H2O��COCl2��3�֣���©д����0�֣���ƽ�����1�֣�
HCl��H2O��COCl2��3�֣���©д����0�֣���ƽ�����1�֣�
��2�� CH4��g��+ CO2��g��= 2CO��g��+ 2H2��g������H=" +" 247.3kJ��mol-1��3�֣�
���ȷ�Ӧ����ʽ2�֣���Ӧ��1�֣�©д����״̬��2�֣���Ӧ��������д��0�֣�
��3�� ��<��2�֣���
��> ��2�֣�������ͬ�¶�ʱ���÷�Ӧ�ķ�Ӧ��Ũ��Խ�ߣ���Ӧ����Խ��2�֣���ֻд��Ũ�Ȼ������ʵı仯��1�֣�
��0.23mol��L��1��4�֣�
COCl2(g)  Cl2(g) �� CO(g)
Cl2(g) �� CO(g)
ƽ��Ũ�ȣ�mol/L�� 0.04 0.11 0.85 ��1�֣�
K��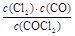 ��
��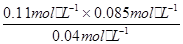 ��0.23 mol��L-1
��0.23 mol��L-1
�����������1��ʵ�����п����ȷ�(CHC13)��˫��ˮֱ�ӷ�Ӧ�Ʊ�����������Ԫ���غ��֪���ﻹӦ��HCl��ˮ���ʷ���ʽΪCHCl3��H2O2 HCl��H2O��COCl2����2������CH4��H2����CO��ȼ���ȷֱ�д��ȼ�յ��Ȼ�ѧ����ʽ����O2��g��+2H2��g��=2H2O��L����H=-571.6kJ?mol-1����CH4��g��+2O2��g��=CO2��g��+2H2O��L����H=-890.3kJ?mol-1����2CO��g��+O2��g��=2CO2��g����H=-566.03kJ?mol-1�����ø�˹���ɽ���-��-�ۿɵã�CH4��g��+CO2��g��=2CO��g��+2H2��g������H=+247.3 kJ?mol-1����3���ٵ�8minʱ��Ӧ���Ũ�ȱȵ�2minʱ��С��������Ũ������ƽ��������Ӧ�����ƶ���4min˲��Ũ�Ȳ��䣬������Ϊ�ı�ѹǿ��Ũ�ȣ�Ӧ�Ǹı��¶ȣ�����Ϊ����ӦΪ���ȷ�Ӧ������T��2����T��8��������5��6 min��15��16 minʱ��Ӧ�¶���ͬ������ͬ�¶�ʱ���÷�Ӧ�ķ�Ӧ��Ũ��Խ�ߣ���Ӧ����Խ��15��16 minʱ����ֵ�Ũ�ȶ�С����˷�Ӧ����С����v��5��6����v��15��16��������ͼ��֪��8minʱCOCl2��ƽ��Ũ��Ϊ0.04mol/L��Cl2��ƽ��Ũ��Ϊ0.11mol/L��CO��ƽ��Ũ��Ϊ0.085mol/L���ʸ��¶���K��
HCl��H2O��COCl2����2������CH4��H2����CO��ȼ���ȷֱ�д��ȼ�յ��Ȼ�ѧ����ʽ����O2��g��+2H2��g��=2H2O��L����H=-571.6kJ?mol-1����CH4��g��+2O2��g��=CO2��g��+2H2O��L����H=-890.3kJ?mol-1����2CO��g��+O2��g��=2CO2��g����H=-566.03kJ?mol-1�����ø�˹���ɽ���-��-�ۿɵã�CH4��g��+CO2��g��=2CO��g��+2H2��g������H=+247.3 kJ?mol-1����3���ٵ�8minʱ��Ӧ���Ũ�ȱȵ�2minʱ��С��������Ũ������ƽ��������Ӧ�����ƶ���4min˲��Ũ�Ȳ��䣬������Ϊ�ı�ѹǿ��Ũ�ȣ�Ӧ�Ǹı��¶ȣ�����Ϊ����ӦΪ���ȷ�Ӧ������T��2����T��8��������5��6 min��15��16 minʱ��Ӧ�¶���ͬ������ͬ�¶�ʱ���÷�Ӧ�ķ�Ӧ��Ũ��Խ�ߣ���Ӧ����Խ��15��16 minʱ����ֵ�Ũ�ȶ�С����˷�Ӧ����С����v��5��6����v��15��16��������ͼ��֪��8minʱCOCl2��ƽ��Ũ��Ϊ0.04mol/L��Cl2��ƽ��Ũ��Ϊ0.11mol/L��CO��ƽ��Ũ��Ϊ0.085mol/L���ʸ��¶���K��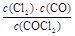 ��
��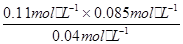 ��0.23 mol��L-1��
��0.23 mol��L-1��
���㣺�����Ȼ�ѧ����ʽ����ѧ��Ӧ���ʡ���ѧƽ�ⳣ�������֪ʶ��
�����Ѷȣ�����