1������� ?����̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ����
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��
___?C+?___?KMnO4+?____?H2SO4��____CO2��+?____MnSO4?+?____K2SO4+?____H2O?
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ
CO��g����H2O��g��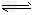 CO2��g����H2��g�����õ�������������
CO2��g����H2��g�����õ�������������
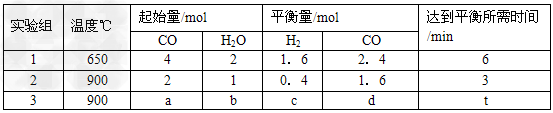
��ʵ��1������ƽ�ⳣ��K=________��ȡС����λ����ͬ����
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a/b?��ֵ_______(�����ֵ��ȡֵ��Χ)��
��ʵ��4����900��ʱ���ڴ������м���10molCO��5molH2O��2molCO2��5molH2�����ʱ
V��______V�棨�<��>��=������
��3����֪�ڳ��³�ѹ�£�
��?2CH3OH(l)?��?3O2(g)?��?2CO2(g)?��?4H2O(g)?��H?��?��1275.6?kJ/mol
��?2CO(g)+?O2(g)?��?2CO2(g)?��H?��?��566.0?kJ/mol
��?H2O(g)?��?H2O(l)?��H?��?��44.0?kJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��___________________
��4������п�ѧ��������룺�ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��ʹ֮��Ϊ������ȼ�ϼ״����ù��뼼���������£�
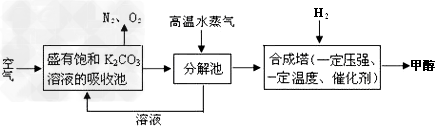
��ֽ����ͨ�����ˮ������������_______________________________?
��5��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��
CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mo1/L?�������ɳ�������CaCl2��Һ����СŨ��Ϊ________________?��
�ο��𰸣���1��5��4��6��5��4��2��6
��2����2.67����<1?��?��<?
��3��CH3OH(l)+?O2(g)?��?CO(g)?+?2H2O(l)?��H����442.8?kJ�Mmol?
��4���ṩ���»���ʹKHCO3�ֽ�
��5��5��6��10-5 mo1/L
���������
�����Ѷȣ�һ��
2��ѡ���� ��֪�Ȼ�ѧ����ʽ��
H2O(g)��H2(g) + 1/2O2(g)? ��H = +241.8kJ��mol
H2(g)+ 1/2O2(g) �� H2O(1)? ��H = ��285.8kJ��mol
��1gҺ̬ˮ��Ϊˮ����ʱ���������仯��
[? ]
A������88kJ
B������2.44KJ
C������44kJ
D������44KJ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3������� ���ø�˹���ɽ�����и�С��
��1����֪��TiO2��s��+2Cl2��g���TTiCl4��l��+O2��g����H=+140kJ?mol-1
2C��s��+O2��g���T2CO��g����H=-221kJ?mol-1
д��TiO2�ͽ�̿��������Ӧ����TiCl4��CO������Ȼ�ѧ����ʽ��______��
��2��25�桢101kPa�£���2Na��s��+
O2��g���TNa2O��s����H1=-414kJ?mol-1
��2Na��s��+O2��g���TNa2O2��s����H2=-511kJ?mol-1
д������������Na2O2��Na����Na2O���Ȼ�ѧ����ʽ��______
��3����֪��C��s��ʯī��+O2��g���TCO2��g����H1=-393.5kJ?mol-1��
2H2��g��+O2��g���T2H2O��l����H2=-571.6kJ?mol-1��
2C2H2��g��+5O2��g���T4CO2��g��+2H2O��l����H2=-2599kJ?mol-1��
д����C��s��ʯī����H2��g������1mol?C2H2��g�����Ȼ�ѧ����ʽ______��
�ο��𰸣���1����֪��TiO2��s��+2Cl2��g���TTiCl4��l��+O2��g����H=+140kJ?mol-1��
��2C��s��+O2��g���T2CO��g����H=-221kJ?mol-1��
TiO2�ͽ�̿��������Ӧ����TiCl4��CO����Ļ�ѧ����ʽΪ��2C+TiO2+2Cl2�TTiCl4+2CO�����Ը��ݢ�+�ڵõ������Է�Ӧ���ʱ�T+140kJ?mol-1+��=-221kJ?mol-1��=-81kJ?mol-1��
�ʴ�Ϊ��2C��s��+TiO2��s��+2Cl2��g���TTiCl4��l��+2CO��g����H=-81kJ?mol-1��
��2����֪������2Na��s��+12O2��g���TNa2O��s����H1=-414kJ?mol-1
��2Na��s��+O2��g���TNa2O2��s����H2=-511kJ?mol-1
Na2O2��Na����Na2O�Ļ�ѧ����ʽΪ��2Na+Na2O2=2Na2O�����Ը��ݢ١�2-�ڵõ������Է�Ӧ���ʱ�=��-414kJ?mol-1����2-��-511kJ?mol-1��=-317kJ?mol-1��
�ʴ�Ϊ��2Na��s��+Na2O2��s��=2Na2O��s����H1=-317kJ?mol-1��
��3����֪����C?��s��ʯī��+O2��g��=CO2��g����H1=-393.5kJ?mol-1��
��2H2��g��+O2��g��=2H2O?��l����H2=-571.6kJ?mol-1��
��2C2H2��g��+5O2��g���T4CO2��g��+2H2O?��l����H2=-2599kJ?mol-1��
2C?��s��ʯī��+H2��g��=C2H2��g���ķ�Ӧ���Ը��ݢ١�2+�ڡ�12-�ۡ�12�õ���
���Է�Ӧ�ʱ��H=2����-393.5kJ?mol-1��+��-571.6kJ?mol-1����12-��-2599kJ?mol-1����12=226.7kJ?mol-1��
�ʴ�Ϊ��2C?��s��ʯī��+H2��g��=C2H2��g������H1=226.7kJ?mol-1��
���������
�����Ѷȣ�һ��
4������� ��֪�����Ȼ�ѧ����ʽ��
��H2(g)��1/2O2(g)��H2O(l)����H����285.8 kJ��mol-1
��H2(g)��1/2O2(g)��H2O(g)����H����241.8 kJ��mol-1
��C(s)��1/2O2(g)��CO(g)����H����110.5 kJ��mol-1
��C(s)��O2(g)��CO2(g)����H����393.5 kJ��mol-1
�ش��������⣺
��1��������Ӧ�����ڷ��ȷ�Ӧ����____________��
��2��H2��ȼ����Ϊ____________��C��ȼ����Ϊ____________��
��3��ȼ��10g H2����Һ̬ˮ���ų�������Ϊ____________��
��4��д��COȼ�յ��Ȼ�ѧ����ʽ__________________________________��
�ο��𰸣���1���٢ڢۢ�
��2��285.8 kJ/mol��393.5 kJ/mol
��3��1429 kJ
��4��CO(g)+1/2O2(g)��CO2(g)����H����283 kJ/mol
���������
�����Ѷȣ�һ��
5������� ������һ����Ҫ�Ļ���ԭ�ϣ����ĺϳɺ�Ӧ���ǵ�ǰ����Ҫ�о�����֮һ��
��1������Ȼ��Ϊԭ����H2�Ǻϳɰ���һ����Ҫ��·�ߣ�����IJ����������䷴Ӧʽ���£�
��CH4��g��+1/2O2?��g��=CO?��g��+2H2��g����H1=-35.6kJ?mol��1
���жϳ����£�������Ӧ�ܷ��Է�����______����ܡ��������о���Ϊ���鲿�������Ļ���Ϊ��
��CH4��g��+2O2?��g��=CO?2��g��+2H2O��g����H2=-890.3kJ?mol��1
��CH4��g��+CO2?��g��=2CO?��g��+2H2��g����H3=247.3kJ?mol��1
�Խ�Ϸ�Ӧ�٣�ȷ�������Ȼ�ѧ��Ӧ����ʽ�еġ�Hֵ
CH4��g��+H2O?��g��=CO?��g��+3H2��g����H=______kJ?mol��1
��2�������£���һ��2L���ܱ������г���1mol?N2��2.6mol?H2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±���ʾ��
| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30
c��NH3��/��?mol?L��1��
0.08
0.14
0.18
0.20
0.20
0.20
|
�������£��÷�Ӧ�ﵽ��ѧƽ��ʱ��������Ũ��Ϊ______��
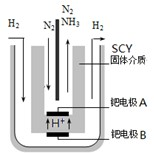
��3��ϣ������˹��´�ѧ��Marmellos��Stoukides��һ������ĵ�ⷽ���ϳɰ������ڳ�ѹ�°��������ú���ϡ�͵ĵ������ֱ�ͨ�뵽570��ĵ����У��ø����ӵ����Ե�SCY�մɣ��ܴ���H+��Ϊ���ʣ������ٶྦྷ��Ĥ���缫��ת���ʸߴ�78%����ʵ��װ������ͼ�������ĵ缫��Ӧʽ______��
��4���ñ�����궨ij��ˮ��Ũ��ʱӦ��ѡ����������ָʾ�����______��
A������?B��ʯ��?C����̪
����?pC����pH����ָ��ϡ��Һ���������ʵ���Ũ�ȵij��ö�����ֵ������Һ��ij���ʵ�Ũ��Ϊ��1��10��3mol?L��1����pC=-lg��1��10��3��=3��ij�¶��£�H2CO3��Һ��pC-pH��ϵ��ͼ��
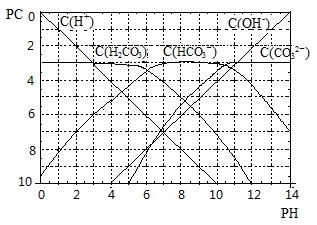
��ش��������⣺
��1��pH=2��4ʱ��H2CO3��Һ����Ҫ���ڵ�����Ϊ______��
��2������¶���H2CO3?

H++HCO3��?�ĵ���ƽ�ⳣ��______��
��3���ܹ��ֿ�������������Ӱ�졢��������?pH�仯�������Һ����֮Ϊ������Һ����Ũ�Ⱦ�Ϊ0.1mol?L��1��NaHCO3��Na2CO3�����Һ����һ�ֻ�����Һ�����������������ƽ��HCO3��

H++CO32���ƶ�����Һ��H+Ũ�ȱ仯������������Ϣ��ȷ����ˮ���Ȼ�淋Ļ����Һ�ܲ����γɻ�����Һ______��
�ο��𰸣�������1����ӦCH4��g��+1/2O2?��g��=CO?��g��+2H2��g���ġ�H1=-35.6kJ?mol��1��0����S��0���ݷ�Ӧ�ܷ��Է����е��оݣ���H-T��S����֪����ֵһ����С��0���ʷ�Ӧ���Է����У��ܣ����ݷ�Ӧ�٢ڢۣ���ϸ�˹���ɣ���֪��ӦCH4��g��+H2O?��g��=CO?��g��+3H2��g����H=�١�2-�ڡ�12250.3-�ۡ�12=250.3kJ?mol-1���ʴ�Ϊ���ܣ�250.3��
��2�����ݷ�ӦN2 +3H2 ?2NH3
��ʼŨ�ȣ�0.5? 1.3? 0
�仯Ũ�ȣ�0.1?0.3?0.2
ƽ��Ũ�ȣ�0.4?1.0?0.2
���Դﵽƽ��ʱ������Ũ����1.0mol/L���ʴ�Ϊ��1.0mol/L��
��3���ڵ����У����������õ��ӵĻ�ԭ��Ӧ�������Խ����£������õ��ӵĹ���Ϊ��N2+6e-+6H+=2NH3���ʴ�Ϊ��N2+6e-+6H+=2NH3��
��4���ñ�����궨ij��ˮ��Ũ��ʱ��ѡ������ܽ��͵ζ����ʴ�Ϊ��A��
������1������ij�¶��£�H2CO3��Һ��pC-pH��ϵͼ�����Եó�pH=2��4ʱ��H2CO3��Һ����Ҫ���ڵ�����ΪH+��HCO3-���ʴ�Ϊ��H+��HCO3-��?
��2�����¶���H2CO3?

H++HCO3-�ĵ���ƽ�ⳣ��K=C(H+)?C(HCO3-)C(H2CO3)=10-6?mol/L���ʴ�Ϊ��10-6mol/L��
��3����ˮ�ĵ����ܲ���笠����ӣ�笠�����ˮ���ܲ���һˮ�ϰ����ӣ���ˮ���Ȼ�淋Ļ����Һ�ܹ��ֿ�������������Ӱ�죬��������pH�仯�������γɻ�����Һ���ʴ�Ϊ���ܣ�
���������
�����Ѷȣ���