1、填空题 13分)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示。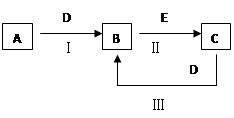
⑴若A是淡黄色化合物;D是CO2;C为NaOH。
①写出A的电子式?
②写出反应Ⅱ的化学方程式?
⑵若A是地壳中含量最多的金属元素的单质,B在火焰上灼烧时火焰呈黄色,E是一种无色无味的气体,遇澄清的石灰水变浑浊。
①写出B的化学式?②写出反应Ⅲ的离子方程式?
③用单线桥法表示反应Ⅰ电子转移的方向和数目?。
参考答案:

本题解析:略
本题难度:一般
2、选择题 将少量的金属钠放入盛有CuSO4溶液的烧杯中,剧烈反应,则烧杯中发生的反应是(?)
①2Na+CuSO4====Na2SO4+Cu ?②Cu+2H2O====Cu(OH)2↓+H2↑
③2Na+2H2O====2NaOH+H2↑?④2NaOH+CuSO4====Cu(OH)2↓+Na2SO4
A.①
B.①②
C.③④
D.①③
参考答案:C
本题解析:金属钠投到任何盐溶液中,首先是Na先与水反应生成H2和NaOH,而不可能是Na与金属阳离子间反应。
本题难度:简单
3、选择题 下列反应所得溶液中一定只含一种溶质的是
A.向AlCl3溶液中滴入NaOH溶液
B.向NaOH溶液中通入SO2气体
C.向稀硝酸中加入过量铁粉
D.向Na2CO3溶液中滴入盐酸
参考答案:C
本题解析:A、向AlCl3溶液中加入过量NaOH溶液反应生成偏铝酸钠和氯化钠,且有剩余的NaOH,溶液中的溶质有3种。B.向NaOH溶液中通入SO2气体,产物可能为Na2SO3或NaHSO3;C、稀硝酸与铁粉反应产物为硝酸铁,铁过量则只生成硝酸亚铁;D、向Na2CO3溶液中滴入盐酸,盐酸少时生成NaHCO3,过量则生成NaCl。
本题难度:一般
4、选择题 A、B、C、D、E五种中学常见物质均含有同一种元素,且A为单质,有如图2所示的转化关系。则下列分析中不正确的是
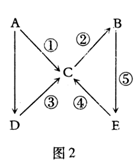
A.?若ABCDE中同一种元素的价态均不相同,则A为非金属单质
B.?若A为金属钠,则由1mol? D完全反应生成C时,一定有1mol电子转移
C.?若A为非金属硫,则④的反应类型既可能为氧化还原反应,也可能为非氧化还原反应
D.?若A为金属铁,则化合物C和D均可以由化合反应制得
参考答案:B
本题解析:A选项? A、 N2? B 、NO2? C、 NO? D 、NH3 ?E、 HNO3
B选项? A、 Na? B、 NaHCO3? C 、NaOH D、 Na2O? E、 Na2CO3;
C选项? A 、S? B、 SO3? C 、 SO2 D、H2S E、 H2SO4
D选项? A 、 Fe? B、 Fe(OH)2? C、FeCl2? D、FeCl3? E、Fe(OH) 3
所以错误的答案是B
点评:考查无机框图推断;
本题难度:一般
5、选择题 将等物质的量的①Na、②Na2O、③Na2O2、④NaOH投入到等体积且足量的水中,得到四种溶液,其中说法正确的是
[? ]
A.①、②、③、④溶质的质量分数相等
B.②、③溶质的物质的量浓度相等
C.①溶质质量分数最大,④溶质的质量分数最小
D.无法确定①、②、③、④四种溶液溶质的质量分数的大小
参考答案:B
本题解析:
本题难度:一般