1、填空题 氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为______________。
(2)混合①中使用冰水的目的是__________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是_______?、________。操作Ⅲ一般适用于分离____________混合物。(选填编号)
a.固体和液体?b.固体和固体?c.互不相溶的液体?d.互溶的液体
(4)混合②中加入Na2SO3的目的是___________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为__________,若假设成立可观察到的现象为_____________。乙同学假设工业氢溴酸呈淡黄色是因为________,其用于证明该假设所用的试剂_____________?。
2、填空题 新型电池在飞速发展的信息技术中发挥着越来越重要的作用。Li2MSiO4(M=Mn、Fe、Co等)是极具发展潜力的新型锂离子电池电极材料,在苹果的几款最新型的产品中已经有了一定程度的应用。下面列出了两种制备Li2FeSiO4的方法:

(1)固相法中制备Li2FeSiO4的过程必须在惰性气体氛围中进行,其原因是___________;根据已有信息,以下判断正确的是________________。
①该反应是氧化还原反应?
②该反应一定是吸热反应
③Li2SiO3?和Li2FeSiO4属于硅酸盐
(2)溶胶-凝胶法中,检验溶液中有胶体产生的方法是____________;实验中若制得1mol?Li2FeSiO4,整个反应过程中转移电子的物质的量为________________。
(3)以Li2FeSiO4、嵌有Li的石墨为电极,含Li+的导电固体为电解质的锂离子电池,充、放电的总反应式可表示为Li2FeSiO4 Li+LiFeSiO4,该电池放电时,负极是________,正极反应式为__________________。
Li+LiFeSiO4,该电池放电时,负极是________,正极反应式为__________________。
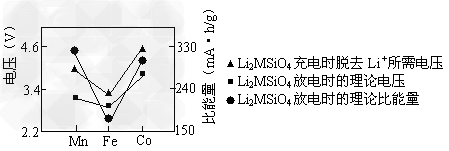
(4)三种Li2MSiO4的性能对比如下图所示。实际应用时,常用来源丰富的铁元素生产的
Li2FeSiO4作电极材料,使用该电极材料的另一个优点是___________________。
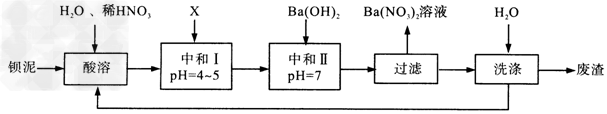
3、填空题 Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药、陶瓷釉药等。钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下:又已知:
①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ba(NO3)2晶体的分解温度:592℃;
③Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。试用离子方程式说明提纯原理:______________________________
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,反应的化学方程式为:______________________。 ?
(3)该厂结合本厂实际,选用的X为________(填序号);
A.BaCl2? B.BaCO3? C.Ba(NO3)2? D.Ba(OH)2 ?
(4)中和I使溶液的p?H为4~5目的是__________________;结合离子方程式简述原理_______________________。 ?
(5)从Ba(NO3)2溶液中获得其晶体的操作方法是___________________。 ?
(6)测定所得Ba(NO3)2晶体的纯度:准确称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为______________。
4、填空题 硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO、CuO等,生产工艺流程示意如下:
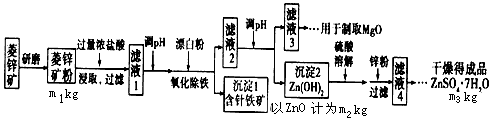
(1)将菱锌矿研磨成粉的目的是 ________________________ 。
(2)完成“氧化除铁”步骤中反应的离子方程式:
口Fe(OH)2+口________+口______=口Fe(OH)3+口Cl-
(3)针铁矿(Coethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O 和H,化学式量为89,化学式是________。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为___________。
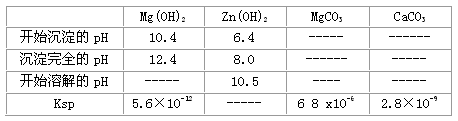
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是____(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为____、____、过滤、洗涤、干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于_______。
5、填空题 工业上用重晶石(主要成分BaSO4)为原料制备BaCl2和锌钡白,生产过程中会产生大量废气(主要成分为CO2、CO及少量SO2和硫蒸气等),为防止污染空气并提高原料利用率,生产中采用下述工艺流程
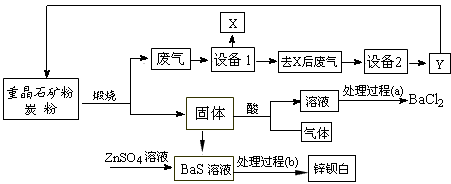
请根据上述流程回答下列问题
(1)假设煅烧时还原产物只有BaS,则反应的化学方程式为___________________________;
(2)设备2中所用的洗涤剂是碱液,则Y的化学式为________________________;
(3)溶解固体所用的酸为____________(写化学式),生成的气体用过量NaOH溶液吸收,其反应的离子方程式为_______________________________;
(4)处理过程(b)的具体步骤为______________________;
(5)锌钡白的成分是___________________(写化学式)。