1��ʵ���� ij�Ȼ�����Ʒ��������FeCl2���ʡ���Ҫ�ⶨ������Ԫ�ص�����������ʵ�鰴���²�����У�

��1�����������õ��IJ����������ձ����������⣬��������________��________(����������)��
��2��д��������ˮ������Ӧ�����ӷ���ʽ_____________________________________��
��3����������Ѿ�ϴ�Ӹɾ��IJ�����������_____________________��
��4����������ΪW1 g�����Ⱥ����������ɫ����������ΪW2 g������Ʒ����Ԫ�ص�����������________ (�г�ԭʼ��ʽ�����軯��)��������ȷ�����ղ����Ľ��ƫ�����������ԭ�������_____________________________________________________________
(д��һ��ԭ��)��
2������� �ɷ����Ʊ�FeCl2����Ҫ�������£�
����ͼ��ʾ�����Ʊ�FeCl3?6H2O

��1�����в�������ĵ���ʽ��?��
��2�������ӷ���ʽ��ʾ���̢���ϡ���������?���ڸù�����Ҫ��������Һ�в������ᣬĿ����?��
����FeCl3 ? 6H2O�Ƶø���FeCl2�Ĺ������£�
������ʢ��FeCl3 ? 6H2O�������м���SOCl2�����ȣ������ˮFeCl3?
��������ˮFeCl3���ڷ�Ӧ���У�ͨ����в���������һ��ʱ�����ȣ�����FeCl2
�����ռ�FeCl2�����汸��
��3�� SOCl2��ˮ�Ӵ���Ѹ�ٲ���������SO2�����ȷֽ�FeCl3 ? 6H2O���ܵõ���ˮFeCl3�������袡�пɵõ���ˮFeCl3����ϱ�Ҫ��ѧ����ʽ���͵õ���ˮFeCl3��ԭ��?��
��4�����̢��в���FeCl2�Ļ�ѧ����ʽ��?��
��FeCl2�İ�װ�����а�ȫע����������������£�
Ʒ ��
| �Ȼ�����
|
��������
| ��ɫ���������ױ�ɻ�ɫ������ˮ���и�ʴ�ԡ���
|
ע������
| ����Ӵ���������ȣ�����ϩ����Ͱ��װ����������
|
?
��5������˵����ȷ����?��
a���ܱձ��桢Զ���Դ
b��������ǿ��������ͬ��š�����
c������������������װ��Ҫ�þ���ϩ����Ͱ��װ
��6��FeCl2�ڿ��������ȿ������Ȼ������������ȣ���Ӧ�Ļ�ѧ����ʽ��?��
3������� ��14�֣����Ը������������Ĺ�ҵ��ҺΪԭ�������������Ĺ�������(���ֲ�����������)��
��.�ӷ�Һ���ᴿ���ᾧ��FeSO4��7 H2O��
H2O��
��.��FeSO4��7H2O���Ƴ���Һ��
��.FeSO4��Һ���Թ�����NH4HCO3��Һ��ϣ��õ���FeCO3����Һ��
��.����Һ���ˣ���90 ����ˮϴ�ӳ����������õ�FeCO3���塣
��.����FeCO3���õ�Fe2O3���塣
��֪��NH4HCO3����ˮ�зֽ⡣
(1)���У�����������м��ȥ��Һ�е�Fe3�����÷�Ӧ�����ӷ���ʽ��_________________��
(2)���У����һ�����ᣬ���������?�����û�ѧƽ��ԭ���������������________________________________________________________________________��
(3)���У�����FeCO3�����ӷ���ʽ��___________________________________________
��FeCO3��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ���ñ仯�Ļ�ѧ����ʽ��_______________________________________��
(4)���У�ͨ������SO���жϳ����Ƿ�ϴ�Ӹɾ�������SO�IJ�����__________
________________________________________________________________________��
(5)��֪����FeCO3�Ļ�ѧ����ʽ��4FeCO3��O22Fe2O3��4CO2��������464.0  kg��FeCO3���õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3��������________kg��(Ħ������/g��mol��1��FeCO3 116 Fe2O3 160 FeO 72)
kg��FeCO3���õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3��������________kg��(Ħ������/g��mol��1��FeCO3 116 Fe2O3 160 FeO 72)
4��ѡ���� ʹO.1 mol Fe203��CO�л�ԭ��������������ͨ�������ij���ʯ��ˮ�У���Ӧһ��ʱ���ֹͣ���õ���ɫ����0.24 mol����ԭ��Fe203�����ʵ���Ϊ
A��O.08 mol
B��0.1 mol
C��O.24 mol
D��O.12 mol
5��������
(һ)��ȡCuO
ʵ�鲽�裺�ٳ�ȡ5 g CuSO4��5H2O����ϸ�����ձ��У���30 mL����ˮ�ܽ⣻
��������CuSO4��Һ����μ���NaOH��Һ��ֱ�����ٲ�������Ϊֹ��Ȼ��
���û����ת�Ƶ��������У�����������ȫ����Ϊ��ɫ��
�۽���������û������ˡ�ϴ�ӣ����ɺ���ϸ���á�
�ش���������
(1)����ʵ�鲽������Ҫʹ�ò���������?(��ʵ�鲽�����)��
��ĥ��������������������?
(2)�������ϴ�ӳ����IJ���������?
(��)��Ч���Ƚ�
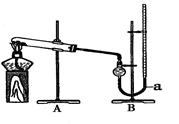
����ͼװ�ý���ʵ�飬ʵ��ʱ��������25 mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԣ�������ݼ��±���
ʵ��
| KClO3����
| �������ʵ���
| ��������
|
ʵ���
| 1.2g
| ����������
| ?
|
ʵ���
| 1.2g
| CuO ?0.5g
| ?
|
ʵ���
| 1.2g
| MnO2 0.5g
| ?
|
?�ش��������⣺
(3)�ϱ�����ʵ���еġ��������ݡ�ָ?
(4)����װ��B�ɸ���ܡ��齺�ܺ�50 mL�ζ��ܸ������װ���ɣ��˴����õζ�����
?(���ʽ����ʽ��)�ζ��ܡ�
(5)��Ҫ֤��ʵ����и�������ռ���������O2���ɴ������ռ��������õ��ɼм�סװ��B�е��齺��a����ȥ������ϵ�����Ƥ����?
(6)Ϊ̽��CuO��ʵ������Ƿ�Ϊ�������貹������ʵ��(����д���������)��
a��?��b������CuO�Ļ�ѧ������û�иı䡣