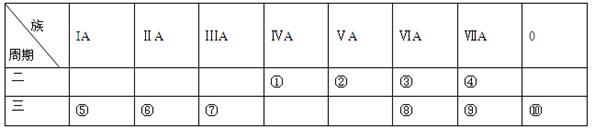
1、填空题 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
 ?
?
(1)非金属性最强的元素是______(填元素符号,下同),形成化合物种类最多的元素是___________。
(2)第三周期元素除⑩外原子半径最小的是______(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________(填化学式,下同),具有两性的是____________。
(3)⑤⑥⑦单质的活泼性顺序为______>______>______ (填元素符号),判断的实验依据是________________________________________________ (写出一种)。
2、填空题 氮可以形成多种离子,如N3-、N3-、NH2-、NH4+、N2H5+、N2H62+等,已知N2H5+与N2H62+是由中性分子X结合H+形成的,有类似于NH4+的性质。
⑴ 1个N3-离子含有?个电子;
⑵ 形成N2H5+离子的中性分子X的分子式是?;
X在氧气中可以燃烧,写出燃烧反应的化学方程式?;
⑶ 写出N2H62+离子在强碱溶液中反应的离子方程式?。
3、选择题 下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是?
元素代号
| L
| M
| R
| T
|
原子半径/nm
| 0.160
| 0.143
| 0.102
| 0.074
|
主要化合价
| +2
| +3
| +6、-2
| -2
|
A.L2+与R2-的核外电子数相等
B.M与T形成的化合物具有两性
C.气态氢化物的稳定性为H2T<H2R
D.L和M金属性强弱比较:L>M
4、选择题 短周期元素R、T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角。下列判断正确的是
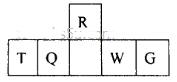
A.离子半径:T< W<G
B.等物质的量的W、G单质分别与足量铁粉反应,后者消耗的铁粉多
C.最简单气态氢化物的热稳定性:Q<R
D.T和G组成的化合物溶于水,其水溶液呈中性
5、填空题 有X、Y、Z、W四种含14个电子的粒子,其结构特点如下:
粒子代码
| X
| Y
| Z
| W
|
原子核数
| 单核
| 不同元素构成的两核
| 同元素构成的两核
| 同元素构成的两核
|
粒子的电荷数
| 0
| 0
| 两个负电荷
| 0
|
?
(1)A原子核外比X原子多3个电子,A的原子结构示意图是?。含lmolX的氧化物晶体中含有共价键数目为?。
(2)Z与钙离子组成的化合物的电子式为?。
(3)14gY完全燃烧放出的热量是141.5kJ,写出Y燃烧的热化学方程式?。
(4)组成W的元素最高价氧化物对应的水化物甲有下图所示转化关系(丁为金属单质,反应条件和其他物质已略)

①写出丁元素在周期表中的位置?。
②写出丁在高温下与水反应的化学方程式?。
③组成W的元素的简单氢化物极易溶于水的主要原因是?,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH,其负极的电极反应式为?。