1、填空题 阅读如下信息后完成问题:元素M是仅次于铁而在生物细胞中大量存在的金属元素,是人体必需元素之一;M用于制合金、白铁、干电池、烟火等;其粉末为强还原剂,可用于有机合成、染料制备以及金、银的冶炼;其氧化物是一种白色颜料。
(1)M的元素符号是_______________,核外电子数有_______________个。
(2)M的最重要的两种矿物的化学式是_______________和_______________。
(3)M的最重要的一种“矾”的名称是_______________,化学式是________________。
(4)M能否与强酸(HCl)或强碱(NaOH)反应。如果能,写出离子方程式。
参考答案:(1)Zn?29
(2)ZnS(闪锌矿)?ZnCO3(菱锌矿)
(3)皓矾?ZnSO4・7H2O
(4)Zn+2H+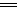 Zn2++H2↑?Zn+2OH-+2H2O
Zn2++H2↑?Zn+2OH-+2H2O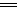 Zn(OH)42-+H2↑
Zn(OH)42-+H2↑
本题解析:M的判断有两处题眼:“仅次于铁而在生物细胞中大量存在的金属元素”“用于制合金、白铁、干电池、烟火等”。综合其他有关信息即可做出判断,M就是锌元素。
锌与酸反应学生是熟悉的,与碱反应则是学生所不熟悉的,但它在金属活动顺序表中与铝紧邻,同学们应该多一个心眼。加之锌与铝处于对角位置,所以同学们应该大胆做出判断,锌与铝的性质应是相似性为主,即它也可以与碱发生反应。
本题难度:简单
2、填空题 (3分)试用化合价升降法配平下列化学方程式。
?
?H2SO4+?H2S ――?SO2?+?S +?H2O
参考答案:1、1、1、1、2
本题解析:硫酸中S的化合价是+6价,H2S中S的个÷化合价是-2价,所以硫酸是氧化剂,硫化氢是还原剂。因为同一种元素之间发生氧化还原反应,生成物的化合价只能处于中间,而不能发生交叉,所以SO2是还原产物,单质S是氧化产物,即1mol硫酸得到2mol电子,1mol硫化氢失去2mol电子,所以方程式为H2SO4+H2S=SO2+S+2H2O。
本题难度:一般
3、选择题 铝可与硝酸钠发生反应(未配平):Al+NaNO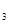 +H
+H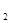 O
O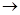 Al(OH)
Al(OH)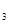 +N
+N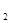 ↑+NaAlO
↑+NaAlO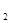 ,有关叙述正确的是(?)
,有关叙述正确的是(?)
A.上述反应中水是氧化剂
B.若反应过程中转移5 mol e 则生成标准状况下N
则生成标准状况下N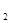 的体积为11.2L
的体积为11.2L
C.该反应的氧化产物是N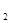
D.当消耗1 mol Al时,生成标况下N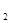 的体积为22.4L
的体积为22.4L
参考答案:B
本题解析:根据方程式可知,Al元素的化合价从0价升高到+3价,失去3个电子,做还原剂;硝酸钠中氮元素的化合价从+5价降低到0价,得到5个电子,做氧化剂,而水不是氧化剂,也不是还原剂,A不正确,B正确;氮气水还原产物,氢氧化铝和偏铝酸钠是氧化产物,C不正确;1mol失去3mol电子,生成0.3mol氮气,D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是准确标出有关元素的化合价变化情况,然后依据有关概念,终于一分析、判断即可。而有关氧化还原反应的计算,则是根据电子的得失进行。
本题难度:一般
4、选择题 新型无机非金属材料氮化硅是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特点,工业上可用下列方法制取:3SiO2+6C+2N2=Si3N4+6CO下列叙述正确的是(?)
A.Si3N4不与任何酸反应
B.Si3N4中硅元素显-4价,氮元素显+3价
C.Si3N4含有离子键
D.上述反应,每生成1mol Si3N4,电子转移12mol
参考答案:D
本题解析:略
本题难度:简单
5、填空题 请将5种物质:N2O、FeCl2、Fe(NO3)3、HNO3和FeCl3分别填入下面对应的横线上,组成一个未配平的化学方程式。
(1)?+?→?+?+?+H2O(不需配平)
(2)反应过程中,N2O与FeCl2的物质的量之比为?。
参考答案:(1)FeCl2? HNO3? Fe(NO3)3? FeCl3? N2O;(2)1:8
本题解析:利用氧化剂的氧化性强于氧化产物的氧化性。还原剂的还原性强于还原产物的还原性。在题目提供的物质中,HNO3、Fe(NO3)3和FeCl3都有氧化性,而且氧化性HNO3>Fe(NO3)3和FeCl3;N2O、FeCl2有还原性,还原性FeCl2>N2O。因此该反应的方程式为:FeCl2 + HNO3 Fe(NO3)3 + FeCl3 +N2O+ H2O;根据质量守恒定律及电子守恒可知在反应中每个FeCl2只能失去1个电子,而每产生1个N2O,要得到电子8个,所以N2O与FeCl2的物质的量之比为1:8.
Fe(NO3)3 + FeCl3 +N2O+ H2O;根据质量守恒定律及电子守恒可知在反应中每个FeCl2只能失去1个电子,而每产生1个N2O,要得到电子8个,所以N2O与FeCl2的物质的量之比为1:8.
本题难度:一般