1������� ��84����Һ������Чɱ�����H1N1�Ȳ�����ijͬѧ������һƿ����¶ʿ���ơ�84����Һ����������������Ϻ�����Һ��װ˵���õ�������Ϣ����84����Һ������25%NaClO��1000mL���ܶ�1.19g?cm-3��ϡ��100��������ȣ���ʹ�ã�
�����������Ϣ�����֪ʶ�ش��������⣺
��1���á�84����Һ�������ʵ���Ũ��Ϊ______mol?L-1��
��2����ͬѧȡ100mL����¶ʿ���ơ�84����Һ��ϡ�ͺ�����������ϡ�ͺ����Һ��c��Na+����______mol?L-1������ϡ�ͺ���Һ�ܶ�Ϊ1.0g?cm-3����
��3��һƿ����¶ʿ���ơ�84����Һ��������______L�����е�CO2����״���������ʣ�
��4����ͬѧ���ġ���¶ʿ���ơ�84����Һ�����䷽������NaClO��������480mL��25%NaClO������Һ������˵����ȷ����______�����ţ���
A������ͼ��ʾ�������У��������Dz���Ҫ�ģ�����һ�ֲ�������
B������ƿ������ˮϴ����Ӧ��ɲ���������Һ����
C�����ù������ƷNaClO�����ƿ��ܵ��½��ƫ��
D����Ҫ������NaClO��������Ϊ143g��
�ο��𰸣���1������c=1000��wM����c��NaClO��=1000mL��1.19g?cm-3��25%74.5g?mol-1��1L=4.0mol?L-1���ʴ�Ϊ��4.0��
��2������ϡ��ǰ�����ʵ����ʵ������䣬��100mL��4.0mol?L-1=100mL��1.19g?cm-3+10000g1g?cm-3��c��NaClO����
���ϡ�ͺ�c��NaClO����0.04mol?L-1��c��Na+��=c��NaClO����0.04mol?L-1���ʴ�Ϊ��0.04��
��3��һƿ��84����Һ������n��NaClO��=1L��4.0mol?L-1=4.0mol��
���ݷ�ӦCO2+2NaClO+H2O�TNa2CO3+2HClO������ҪCO2�����ʵ���Ϊn��NaClO����12=2.0mol��
����״����V��CO2��=2.0mol��22.4L?mol-1=44.8L���ʴ�Ϊ��44.8L��
��4��A������������ƽ����NaClO���壬�����ձ����ܽ�NaClO�����ò��������н������������������ƿ�ͽ�ͷ�ι������ݣ�ͼʾ��A��B��C��D����Ҫ�������貣�����ͽ�ͷ�ιܣ���A����
B�����ƹ�������Ҫ����ˮ�����Ծ�ϴ�Ӹɾ�������ƿ���غ�ɺ���ʹ�ã���B����
C������NaClO�����տ����е�H2O��CO2�����ʣ�������ƷNaClO���ܲ��ֱ��ʵ���NaClO���٣����Ƶ���Һ�����ʵ����ʵ�����С�����ƫ�ͣ���C��ȷ��
D��Ӧѡȡ500mL������ƿ�������ƣ�Ȼ��ȡ��480mL���ɣ�������ҪNaClO��������0.5L��4.0mol?L-1��74.5g?mol-1=149g����D����
�ʴ�Ϊ��C��
���������
�����Ѷȣ�һ��
2��ѡ���� �ڱ�״���£�����һ��������������������Ϊ74.6�ˣ����ij䵪����������Ϊ66�ˣ����������ݻ�Ϊ
[? ]
A��11.2L
B��5.6L
C��4.48L
D��2.24L
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� NAΪ�����ӵ�����������˵������ȷ����(? )
A��17 g 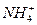 �к��еĵ�����Ϊ10NA
�к��еĵ�����Ϊ10NA
B��1 mol��L-1 Mg(NO3)2��Һ�к���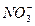 ����ĿΪ2NA
����ĿΪ2NA
C����״���£�22.4 L�ױ������ķ�����ΪNA
D�������£�28.0 g��ϩ�ͱ�ϩ�л�������к��е�̼ԭ����Ϊ2NA
�ο��𰸣�D
������������⿼������֮��İ�����ϵ��18 g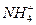 �к��еĵ�������Ϊ10NA��B��û����Һ������������ʵ���������������Ŀ��C��ױ�ΪҺ�壬�������壬����22.4 L�ױ�������1 mol����ϩ�ͱ�ϩ��ԭ�Ӹ���C��H=1��2�����Բ�����ϩ�ͱ�ϩ����Ӱ�죬ֻҪ����һ����28.0 g�У����е�̼ԭ����Ϊ2NA��
�к��еĵ�������Ϊ10NA��B��û����Һ������������ʵ���������������Ŀ��C��ױ�ΪҺ�壬�������壬����22.4 L�ױ�������1 mol����ϩ�ͱ�ϩ��ԭ�Ӹ���C��H=1��2�����Բ�����ϩ�ͱ�ϩ����Ӱ�죬ֻҪ����һ����28.0 g�У����е�̼ԭ����Ϊ2NA��
�����Ѷȣ���
4������� ��1��������л������㣺
��3.6 g H2O�����ʵ���Ϊ ������ mol��
�ڷ�����Ϊ3.01��1023��H2�����ʵ���Ϊ ������ mol��
�۱�״���£�8.96 L N2�����ʵ���Ϊ ������ mol��
��75 mL 2.0 mol��L��1 CaCl2��Һ�к�CaCl2 ������ mol��
��2��ѡ�����и�С�����ʷ�����ᴿ�����ݵ��������ʺͷ��뷽����
| ���ʲ���
| ���뷽��
|
�ٳ�ȥ�Ȼ�����Һ�е���ɳ
|
|
|
�������Ȼ�̼��ȡ��ˮ�е��嵥��
|
|
|
�۷������ᣨ�е�1180C���������������е�77.10C��
|
|
|
�ܷ������ͺ�ˮ
|
|
|
�ݴӺ�������NaCl��KNO3��Һ����ȡKNO3
|
|
|
���ʲ��죺A���ܽ�����¶ȱ仯���졡 B���ڲ�ͬ�ܼ��е��ܽ�Ȳ���
C���е���� ��D���������� E����ˮ�е��ܽ�Ȳ���
���뷽����a������ b������ c����Һ d����ȡ e���ᾧ
��3����ҵ���ʳ��ˮ��ȡ�����Ļ�ѧ����ʽ�� ��
�ο��𰸣���1����0.2��������0.5��������0.4��������0.15��
w.w.^w.k.&s.5*u.c.#om��.��.��.Դ.�� ��2��
���ʲ���
���뷽��
�ٳ�ȥ�Ȼ�����Һ�е���ɳ
E
b
�������Ȼ�̼��ȡ��ˮ�е��嵥��
B
d����dc��
�۷������ᣨ�е�1180C���������������е�77.10C��
C
a
�ܷ������ͺ�ˮ
D
c
�ݴӺ�������NaCl��KNO3��Һ����ȡKNO3
A
e
 ��3��2NaCl + 2H2O 2NaOH+H2�� + Cl2��
��3��2NaCl + 2H2O 2NaOH+H2�� + Cl2��
�����������
�����Ѷȣ�һ��
5��ѡ���� �谢���ӵ�����ΪNA��������˵����ȷ����(? )
A�����³�ѹ�£�11.2 L�����к��е���ԭ����Ϊ2NA
B����״���£�0.3 mol���������к�����ԭ����Ϊ0.3NA
C�������£�2.7 g�������������ᷴӦ��ʧȥ�ĵ�����Ϊ0.3NA
D�������£�1 L 0.1 mol��L-1 MgCl2��Һ�к�Mg2+��Ϊ0.2NA
�ο��𰸣�C
��������������ۺϿ������ʵ����������ӵ�������Ħ������������Ħ��������йؼ��㡣���³�ѹ�£�11.2 L CH4�����ʵ���С��0.5 mol�����к��е���ԭ����С��2NA��A����ȷ;1 mol SO2��2NA����ԭ�ӣ�0.3 mol SO2�к���0.6NA����ԭ�ӣ�B����ȷ��1 mol���������ᷴӦʧȥ��3 mol���ӣ���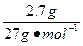 ="0.1" mol�������������ᷴӦʧ������Ϊ0.3 NA,C��ȷ����MgCl2====Mg2++2Cl-֪0.1 mol MgCl2��Һ�к�Mg2+��ĿΪ0.1 NA,D����ȷ��
="0.1" mol�������������ᷴӦʧ������Ϊ0.3 NA,C��ȷ����MgCl2====Mg2++2Cl-֪0.1 mol MgCl2��Һ�к�Mg2+��ĿΪ0.1 NA,D����ȷ��
�����Ѷȣ���