1、选择题 将下列反应所产生的气体,通入硅酸钠溶液中后不发生反应的是(?)
A.CO2与Na2O2
B.Cu与浓H2SO4共热
C.Cu与浓硝酸共热
D.食盐与浓H2SO4共热
参考答案:A
本题解析:A项中气体为O2,不反应,而B项中SO2、C项中NO2、D项中HCl均与Na2SiO3反应产生H2SiO3沉淀。
本题难度:简单
2、计算题 为测定某石灰石中CaCO3的质量分数,称取W g石灰石样品,加入过量的浓度为6 mol/L的盐酸,使它完全溶解,加热煮沸,除去溶解的CO2,再加入足量的草酸铵[(NH4)2C2O4]溶液后,慢慢加入氨水降低溶液的酸度,则析出草酸钙沉淀,离子方程式为:C2O2-4+Ca2+=CaC2O4↓,过滤出CaC2O4后,用稀硫酸溶解:CaC2O4+H2SO4=H2C2O4 +CaSO4,再用蒸馏水稀释溶液至V0 mL。取出V1 mL用a mol/L的KMnO4酸性溶液滴定,此时发生反应:
2MnO- 4+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
若滴定终点时消耗a mol/L的KMnO4 V2 mL,计算样品中CaCO3的质量分数。
参考答案: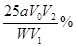
本题解析:分析:本题涉及到化学方程式或离子方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑? C2O2-4+Ca2+=CaC2O4↓
CaC2O4+H2SO4=H2C2O4+CaSO4?2MnO- 4+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
由方程式可以得出相应的关系式:
5CaCO3――5Ca2+――5CaC2O4――5H2C2O4――2MnO-4
5?2
n1(CaCO3)? aV2×10-3 mol
n1(CaCO3) =" 2.5" aV2×10-3 mol
样品中:n(CaCO3) =? 2.5 aV2×10-3×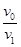 ?mol
?mol
则:ω(CaCO3) =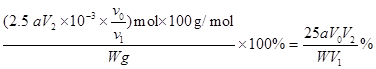
本题难度:一般
3、选择题 可以肯定溶液中大量存在CO32-的理由是?(?)
A.加入AgNO3溶液,有大量白色沉淀产生
B.加入酸,有无色无味气体产生
C.加入BaCl2溶液时有白色沉淀产生,再加稀盐酸沉淀溶解,产生可使澄清石灰水变浑浊的无色无味的气体







D.加入Ba(OH)2溶液有白色沉淀产生,再加稀盐酸如C所述
参考答案:C
本题解析:溶液中含有Cl-、SO32-时,可与AgNO3溶液反应产生白色沉淀,A不正确。HCO3-与酸反应会产生无色无味CO2气体,B不正确。向含有HCO3-的溶液中加入
Ba(OH)2时:HCO3-+OH-+Ba2+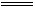 BaCO3↓+H2O,再加盐酸BaCO3+2H+
BaCO3↓+H2O,再加盐酸BaCO3+2H+ Ba2++CO2↑
Ba2++CO2↑
+H2O,其现象与CO32-反应现象相同,D选项不正确。
本题难度:简单
4、选择题 关于硅的叙法不正确的是
A.高纯硅是良好的半导体
B.硅是制造太阳能电池的常用材料
C.硅的化学性质不活泼,常温下不与任何物质反应
D.硅在地壳中含量居第二位,但在自然界中没有游离态的硅存在
参考答案:C
本题解析:A 正确,硅在元素周期表中位于金属元素和非金属元素的分界线处,是良好的半导体。
B 正确,太阳能电池中的常用材料是硅。
C 错误,虽然硅的化学性质不活泼,但是也能和氢氧化钠溶液反应。
D 正确,地壳中元素含量由多到少的顺序为:氧、硅、铝、铁等,硅处于第二位,且自然界中没有游离态的硅存在。
本题难度:一般
5、选择题 下列物质的主要成分不是二氧化硅的是
A.水玻璃
B.水晶
C.玛瑙
D.硅石
参考答案:A
本题解析:水玻璃的主要成分是硅酸钠,水晶、玛瑙、硅石主要成分是二氧化硅,故选A。
本题难度:一般