1、简答题 由1~20号元素组成的A、B、C、D、E、F有如图所示的相互转变,所有反应物和生成物均已给出,且已知A、C、D为单质,B、E、F为化合物.
(1)若A为气体单质,且当A与B质量比为19:12时,C和D恰好完全反应,则B的电子式______,E的水溶液与澄清石灰水反应的离子反应方程式______.
(2)若A?为固体单质,且当A与B质量相等时,C和?D恰好完全反应,则若将A加入到FeCl2溶液中,发生反应的化学反应方程式为______,如果反应生成的C与D反应正好生成1mol水,那么,同时生成的E、F与足量的金属铝反应产生气体的体积比为V(E):V(F)=______.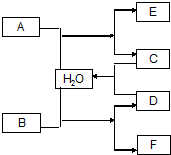
参考答案:本题一个很清晰的解题切入口是单质C与单质D反应生成水.显然,C、D是氢气和氧气.所以从归纳通过与水能生成氢气和氧气的入手就可以使问题得以解决.在由1-20元素组成的化合物及单质中,常见可生成H2的反应有,单质:Na(Li、K)+H2O→,化合物:NaH(KH)+H2O→;常见可生成O2的反应有,单质:F2+H2O→,化合物:Na2O2(K2O2、KO2、CaO2)+H2O→.结合题中所给出A、B的质量比可以得出:
(1)A为气体单质,且当A与B质量比为19:12时,C和D恰好完全反应,则A是F2,B是NaH.相应的E是HF,F是NaOH;B的电子式为
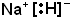
,E的水溶液与澄清石灰水反应的离子反应方程式为2HF+Ca2++2OH-=CaF2↓+2H2O,
故答案为:
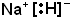
;2HF+Ca2++2OH-=CaF2↓+2H2O;
(2)若A?为固体单质,且当A与B质量相等时,C和?D恰好完全反应,则若将A加入到FeCl2溶液中,A是K,B是Na2O2,E是KOH,F是NaOH.C与D反应正好生成1mol水时,H2为1mol水,生成的KOH为2mol,O2为0.5mol,生成的NaOH也是2mol,所以V(E):V(F)=1:1,根据电子守恒规律能快速得出这一结论;
故答案为:4Na2O2+4FeCl2+6H2O=4Fe(OH)3↓+8NaCl+O2↑;1:1.
本题解析:
本题难度:一般
2、简答题 如图转化关系中所有物质均为中学常见物质,且反应中的部分产物已略去.A、F为银白色金属,D、X均为无色无味的气体单质,Z为黄绿色气体单质,其余物质均为化合物.Y为红棕色粉末,常用作红色油漆和涂料.
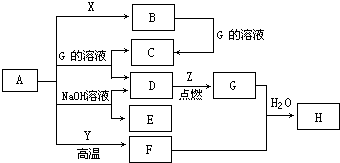
请按要求回答下列问题:
(1)Z的化学式为______.
(2)在实验室中,欲检验H溶液中的金属阳离子,先向溶液中滴加几滴______溶液,再加入几滴氯水,观察到溶液变为______色,证明原溶液中的金属阳离子为______.
(3)B与NaOH溶液反应的离子方程式为______.
(4)A与Y反应生成F的化学方程式为______.
(5)等质量的A分别与足量的G溶液、NaOH溶液充分反应后,相同条件下产生气体D的体积比为______.
参考答案:银白色金属A能与NaOH溶液反应得到E与无色无味的气体单质D,可推知A为Al、E为NaAlO2、D为H2,Z为黄绿色气体单质,则Z为Cl2,Z与D反应得到G为HCl,Y为红棕色粉末,常用作红色油漆和涂料,则Y为Fe2O3,A与Y在高温下反应得到金属单质F为Fe,Fe与G、水反应得到化合物H为FeCl2,Al与G溶液(盐酸)反应得到化合物C为
AlCl3,Al与无色无味气体单质X反应得到B,B溶于盐酸得到C,可推知X为O2、B为Al2O3,
(1)由上述分析可知,Z的化学式为Cl2,故答案为:Cl2;
(2)欲检验FeCl2溶液中的金属阳离子,先向溶液中滴加几滴KSCN溶液,再加入几滴氯水,观察到溶液变为红色,证明原溶液中的金属阳离子为Fe2+,故答案为:KSCN;红;Fe2+;
(3)B为Al2O3,与NaOH溶液反应的离子方程式为:Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(4)A与Y反应生成F的化学方程式为:2Al+Fe2O3高温.Al2O3+2Fe,故答案为:2Al+Fe2O3高温.Al2O3+2Fe;
(5)等质量的Al分别与足量的HCl溶液、NaOH溶液充分反应后,都生成氢气,反应中Al元素化合价都由0价升高为+3价,由于Al完全反应,故转移电子数目相等,故生成氢气的体积相等,即生成氢气体积之比为1:1,故答案为:1:1.
本题解析:
本题难度:一般
3、推断题 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示
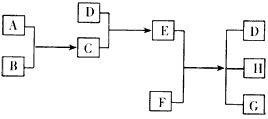
(1)D的化学式(分子式)是________________,E的化学式(分子式)是________________
(2)A和B反应生成C的化学方程式是___________________________
(3)E和F反应成D、H和G的化学方程式是________________________
参考答案:(1)NH3;NH4Cl
(2)H2+Cl2 2HCl
2HCl
(3)2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O
本题解析:
本题难度:一般
4、填空题 (1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
①通甲烷的铂丝为原电池的______极,发生的电极反应为______.
②该电池工作时(放电)反应的总化学方程式为______.
(2)X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式为______;
②向苛性钠溶液中通入过量的A所发生反应的离子方程式为______
③将B与氯气的水溶液充分反应可生成两种强酸,该反应的化学方程式为______.
参考答案:(1)①燃料燃烧时失电子发生氧化反应,原电池的负极上失电子发生氧化反应,所以通甲烷的铂丝为原电池的负极;甲烷燃烧生成二氧化碳和水,二氧化碳是酸性氧化物能和氢氧化钾反应生成碳酸钾和水,所以该电极上的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
故答案为:负;CH4+10OH--8e-=CO32-+7H2O;?
②甲烷失电子发生氧化反应,氧气得电子发生还原反应,氧气得电子和水反应生成氢氧根离子,所以该反应的电池反应式为:CH4+2O2+2OH-=CO32-+3H2O;
故答案为:CH4+2O2+2OH-=CO32-+3H2O;
(2)①Y是短周期非金属元素的单质且常温下为固体,和Z反应生成气体,所以Y只能是S;硫和非金属单质反应且生成的物质是气体,所以非金属单质为氢气、氧气,A在空气中充分燃烧可生成B,所以A硫和氢气反应的产物,B是硫和氧气反应的产物,从而确定X是氢气,Z是氧气,A是硫化氢,B是二氧化硫.
故答案为:SO2;
?②H2S是二元弱酸,能和氢氧化钠反应生成硫化钠和水,当硫化氢过量时硫化钠和硫化氢反应生成硫氢化钠.
故答案为:H2S+OH-=HS-+H2O;
③氯气有强氧化性,二氧化硫既有氧化性又有还原性,当遇到强氧化剂时,二氧化硫作还原剂被氧化,所以二氧化硫和氯气的水溶液反应生成盐酸和硫酸.
故答案为:SO2+Cl2+2H2O=H2SO4+2HCl.
本题解析:
本题难度:一般
5、推断题 下图涉及多种无机化工反应,所涉及物质都是由短周期元素组成的,其中R是一种新型无机材料,M是一种应用广泛的金属材料,F是人工合成的第一种有机物,且是一种常见的化肥,A、C、D、M均为常见元素的单质,“↑”表 示该物质常温下是气体,反应G+J→F+H2O中G与J的最佳配比为2:1,向Y溶液中通入足量的J气体时可得到一种白色胶状沉淀,将该白色胶状沉淀滤出,洗净后加热分解可以得到B。
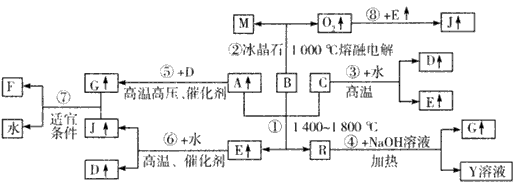
请回答下列问题:
(1)写出B的化学式:____ ,F的化学式:____ 。
(2)反应①的化学方程式为___。
(3)反应④的离子方程式为____ 。
(4)上述反应中属于非氧化还原反应的___(填写相应反应的序号)。
(5)Y溶液呈___性(填“酸”、“碱”或“中”),用离子方程式解释:____。
参考答案:(1) Al2O3?; CO( NH2)2
(2)N2 +Al2O3 +3C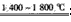 3CO +2AlN
3CO +2AlN
(3)AlN+OH- +H2O=AlO2-+NH3↑
(4)④⑦
(5)碱; AlO2-+2H2O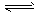 Al(OH) 3 +OH -
Al(OH) 3 +OH -
本题解析:
本题难度:一般