1、填空题 如图是部分元素的单质和化合物之间的相互转化关系,部分反应的生成物没有全部列出.已知原料A、M均属于金属氧化物,L是由两种沉淀组成的.F和Y反应能生成一种全部为非金属元素所组成的盐,C的焰色反应呈黄色,M有磁性,反应①中B和C的物质的量之比为3:4.
回答下列问题:
(1)反应②的主要用途是:______(答一点即可,2分),Y的空间构型为______.
(2)已知反应③中还有一种无色气体生成,写出反应③的离子方程式:______.
(3)L中两种沉淀为______(用化学式表示),A的化学式为______.
(4)若将M溶于稀硫酸中可形成溶液Z,请设计简单的实验,证明Z溶液中所含的金属阳离子:______.

参考答案:F和Y反应能生成一种全部为非金属元素所组成的盐,所以生成的盐为铵盐,故F和Y有一种是酸,一种是氨气;M有磁性,所以M是四氧化三铁;H和B 反应生成四氧化三铁,所以H和B有一种是氧气,一种是铁;四氧化三铁能和F反应,四氧化三铁和酸反应,和氨气不反应,所以F是酸,Y是氨气;B和Y反应生成D,氨气和铁不反应,和氧气反应,所以B 是氧气,H是铁;A是氧化物,A和X反应生成氧气,所以A是过氧化钠;氧气和氨气反应生成一氧化氮,所以D是一氧化氮;一氧化氮和氧气反应生成二氧化氮,所以E是二氧化氮;二氧化氮和水反应生成硝酸和一氧化氮,F是酸,所以F 是硝酸,X是水;过氧化钠和水反应生成氢氧化钠和氧气,所以C是氢氧化钠;四氧化三铁和N生成铁的反应是铝热反应,所以N是铝,G是氧化铝;氧化铝和氢氧化钠反应生成偏铝酸钠和氢气,I和硝酸铁反应生成L,L有两种沉淀,所以I是偏铝酸钠,L是氢氧化铝和氢氧化铁.
(1)铝热反应的用途是冶炼金属或焊接钢轨;氨气分子的空间构型为三角锥型,
故答案为:冶炼金属或焊接钢轨;三角锥型;
(2)四氧化三铁和硝酸反应生成硝酸铁、一氧化氮和水,故答案为:3Fe3O4+28H++NO3-=9Fe3++NO+14H2O;
(3)通过以上分析知,L为Fe(OH)3、Al(OH)3,A为Na2O2,故答案为:Fe(OH)3、Al(OH)3;Na2O2;
(4)四氧化三铁和稀硫酸反应生成硫酸铁和硫酸亚铁、水,三价铁离子用硫氰化钾溶液检验;二价铁离子用酸性高锰酸钾溶液检验,
故答案为:分别取少量乙溶液于两支洁净的试管中,向第一支试管中滴加硫氰化钾溶液,溶液变血红色,证明有Fe3+,向第二只试管中,滴加少量酸性高锰酸钾溶液,振荡,高锰酸钾紫色褪去,证明含有Fe2+.
本题解析:
本题难度:一般
2、填空题 某强酸性溶液X,含有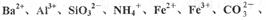
 中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
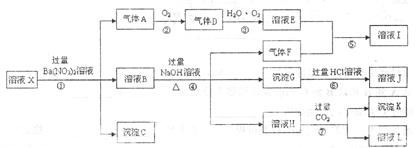
依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是: ____________________________不能肯定的是_____________________.对不能确定是否存在的离子,可以另取X溶液于一支试管中,选择下列试剂中的一种加入X溶液中 根据现象就可判般,则该试剂最好是:______________①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸⑤KSCN溶液,⑥KMnO4溶液。
根据现象就可判般,则该试剂最好是:______________①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸⑤KSCN溶液,⑥KMnO4溶液。
(2 )气体F的化学式为:______________,沉淀K的化学式为:_______,实验中,可以观察到反应②的现象是____________________________.
(3) 写出步骤①所有发生反应的离子方程式_____________________________ ;
(4) 要使步骤③中,D、H2O,O2三种物质恰好发生化合反应,则D、H2O, O2物质的量之比是____________________________。
参考答案:(1)SO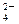 、Al3+、Fe2+、NH4+(各1分,共4分);Fe3+(1分);⑤(1分)
、Al3+、Fe2+、NH4+(各1分,共4分);Fe3+(1分);⑤(1分)
(2)NH3,Al(OH)3,气体由无色变红棕色 (各1分,共3分)
(3)Ba2++SO42-=BaSO4↓,3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O(各2分,共4分)
(4)4:2:1(2分)
本题解析:略
本题难度:一般
3、简答题 甲、乙、丙三种物质之间有如下转化关系:
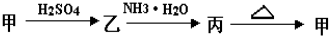
(1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是______?写出乙丙转化的化学方程式:______.
(2)若乙溶液中加入KSCN溶液,有血红色出现,则甲物质是______.写出?甲乙转化的离子方程式______.
参考答案:(1)通过题意知,甲是两性物质,我们学过的既能溶于酸又能溶于碱的物质有铝、氧化铝、氢氧化铝.通过转化方式得,甲、乙、丙有相同的元素.无论是哪种物质由甲生成乙,乙都是硫酸铝,硫酸铝和氨水反应生成氢氧化铝,氢氧化铝加热分解的氧化铝,所以甲是Al2O3,乙丙转化属于复分解反应,盐和碱反应生成另外的盐和碱,所以方程式为:
Al2(SO4)3+6NH3?H2O=2Al(OH)3+3(NH4)2SO4,故答案为:Al2O3;Al2(SO4)3+6NH3?H2O=2Al(OH)3+3(NH4)2SO4;
(2)通过转化方式得,甲、乙、丙有相同的元素,甲与硫酸反应生成乙,乙是硫酸盐,硫酸盐与氨水反应生成丙,丙是不溶性的碱,碱加热分解的氧化物,所以甲是氧化物.若乙溶液中加入KSCN溶液,有血红色出现,有血红色出现是Fe3+的特征反应所以甲是Fe2O3,氧化物和酸反应生成盐和水,所以其离子方程式为:Fe2O3+6H+=2Fe3++3H2O,
故答案为:Fe2O3;Fe2O3+6H+=2Fe3++3H2O.
本题解析:
本题难度:一般
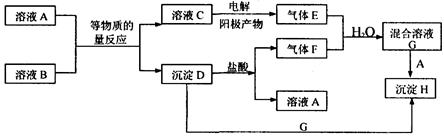
4、填空题 (8分)A、B均为无色盐溶液,B的焰色反应呈黄色,一定条件下A、B可以发生图所E和F均为有刺激性气味的气体, H不溶于酸,示的物质之间的一系列变化:
请填写下列空白。
(1)气体F的化学式为?,C中溶质的化学式为?。
(2)写出下列反应的离子方程式:
C→E?;? D+G→H?;
(3) 在混合溶液G中若滴入几滴石蕊溶液,可见现象为?,原因是_______________________________(用化学方程式表示G溶液的形成过程)
参考答案:(8分)(1)? SO2,? NaCl?(2分)
(2)①2Cl-+2H2O Cl2↑+H2↑+2OH-?(1分)
Cl2↑+H2↑+2OH-?(1分)
②BaSO3+2H++SO42-=BaSO4+SO2↑+H2O(2分)
(3)变红色(1分);SO2+Cl2+2H2O=2HCl+H2SO4(2分
本题解析:B的焰色反应呈黄色,说明含有钠离子。E和F均为有刺激性气味的气体,且E是阳极的电极产物,所以E应该是氯气,则C可能是氯化钠。D和盐酸反应生成F,所以F可能是二氧化硫,D可能是亚硫酸钡。氯气把二氧化硫氧化生成硫酸,则G是硫酸。G和A反应生成H沉淀,所以A是氯化钡,H是硫酸钡,则B是亚硫酸钠。
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。
本题难度:一般
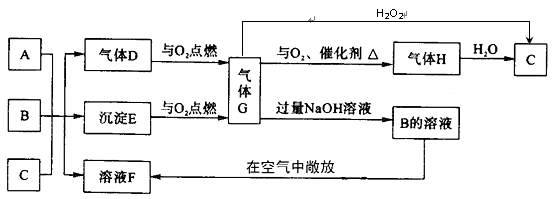
5、填空题 (12分) A、B是两种钠盐,且都是正盐,A中含有两种元素,B中含有三种元素,C是一种常?见的二元强酸,且A、B、C中皆含有同一元素,D有臭鸡蛋气味,它们在水溶液中有如下转化关系:
试回答:
(1)A、D、G的化学式分别为?、?、?
(2)A、B、C反应只生成E和F的离子方程式为?。
(3)要发生上述转化,A、B物质的量之比 应满足的关系是?。
应满足的关系是?。
(4)气体G可使高锰酸钾溶液褪色,发生反应的离子方程式为?。
参考答案:
(1)Na2S? H2S? SO2?(3分)?(2)2S2-+ SO32-+ 6H+=" 3S↓+" 3H2O(3分)
(3)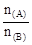 >
>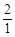 ?(3分)
?(3分)
(4)5SO2 + 2MnO4-+ 2H2O = 2Mn2++ 5SO42-+ 4H+(3分)
本题解析:略
本题难度:简单