1、填空题 在元素周期表中,最活泼的非金属元素是______,能稳定存在的最活泼的金属元素是______;最高价氧化物的水化物中酸性最强的酸是______,对应此元素的含氧酸中氧化性最强的是______;在室温下为液态的金属单质是______,在室温下为液态的非金属单质是______;+2价的阳离子与氖原子具有相同电子层结构的元素是______,-2价阴离子与氩原子具有相同电子层结构的元素是______.(写相应的元素符号或化学式)
2、推断题 Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态俗名叫___________。
(2)R的氢化物分子的空间构型是________,属于________(填“极性”或“非极性”)分子;它与X形 成的化合物可作为一种重要的陶瓷材料,其化学式是________________。
(3)X的常见氢化物的空间构型是____________。
(4)Q分别与Y、Z形成的共价化合物的化学式是___________、_________;Q与Y形成的分子属于
________(填“极性”或“非极性”)分子。
3、简答题 已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:
| 元素 | Al | B | Be | C | Cl | F | Li
X的数值
1.5
2.0
1.5
2.5
2.8
4.0
1.0
元素
Mg
Na
O
P
S
Si
X的数值
1.2
0.9
3.5
2.1
2.5
1.7
|
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是______.
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系______.
(3)请你预测Br与I元素的X数值的大小关系______.
(4)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于______原子(填元素符号).
4、选择题 已知a、b分别为同周期的ⅠA和ⅦA族的两种元素,它们的原子序数分别为m和n,则下列关系不可能成立的是( )
A.n=m+16
B.n=m+6
C.n=m+30
D.n=m+10
5、填空题 下表是元素周期表的一部分,回答下列问题:
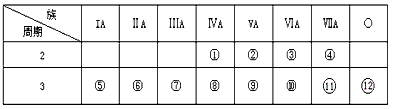
(1)写出①---⑿号元素的元素符号①___ ②___ ③____ ④____ ⑤____ ⑥____ ⑦___ ⑧____ ⑨____ ⑩___  _____
_____ ____
____
(2)写出①、③两种元素形成的化合物有两种,化学式:_______ ,____________ 。
(3)写出①元素最高价氧化物的电子式和结构式________ ,__________ 。
(4)这些元素的最高价氧化物的对应水化物中________酸性最强;________碱性最强;能形成两性氢氧化物的元素是________ ,形成两性氢氧化物化学式_____________ 。