1、填空题 (12分)从海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。

试回答下列问题:
(1)写出用海滩上的贝克制取Ca(OH)2的化学方程式:
?。
(2)写出电解熔融氯化 镁制取镁的化学方程式
镁制取镁的化学方程式 :?。
:?。
(3)将电解生成的氯气通入氢氧化钠溶液中可得到一种消毒液,写出反应的化学方程式:? ?。
?。
(4)粗盐中常含有Ca2+、Mg2+等杂质,可用Na2CO3、NaOH除去。精制过程发生反应的离子方程式为??、?。
(5)为有效除去Ca 2+、
2+、 Mg
Mg 2+、SO
2+、SO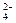 ,加入试剂的合理顺序为?
,加入试剂的合理顺序为? ?(选填a,b,c)
?(选填a,b,c)
a. 先加NaOH,后加Na2CO3,再加钡试剂
b. 先加NaOH,后加钡试剂 ,再加Na2CO3
,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3?
2、实验题 二氧化铈 是一种重要的稀土氧化物.。平板电视显示屏生产过程中产生大量的废玻璃粉末(含
是一种重要的稀土氧化物.。平板电视显示屏生产过程中产生大量的废玻璃粉末(含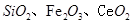 以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
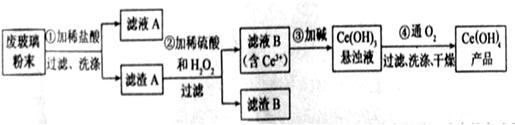
(1)洗涤滤渣A的目的是为了去除?(填离子符号),检验该离子是否洗净的方法是?。
(2)第②步反应的离子方程式是?,滤渣B的主要成分是?。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP?(填“能”或“不能”)与水互溶。实验室进行萃取操作是用到的主要玻璃仪器有?、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的
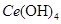 产品0.536g,加硫酸溶解后,用0.1000mol?
产品0.536g,加硫酸溶解后,用0.1000mol?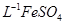 溶液(铈被还原为
溶液(铈被还原为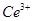 ),消耗25.00mL溶液,该产品中
),消耗25.00mL溶液,该产品中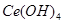 的质量分数为?。
的质量分数为?。
3、填空题 (8分)【化学?-化学与技术】
电解原理在工业有广泛的应用。利用相关知识回答下面的问题。
(1)铝的阳极氧化:在进行电解以前,要对铝电极进行表面处理,是将铝片浸入热的16%NaOH溶液中半分钟左右,目的是?,反应的离子方程式为?。铝的阳极氧化时,铝与电源的? ?极(填写正、负极)相连。
?极(填写正、负极)相连。
(2)电解原理的运用:在右图装置中,溶液的体积为100mL,开始时电解质溶液的浓度为0.1mol/L,工作一段时间后导线上通过0.001mol电子。若不考虑盐的水解和溶液体积的变化,则电解后溶液的pH值为____________。
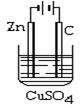
(3)电镀是运用电解原理,在金属表面形成一薄层有抗腐蚀、抗磨损能力的金属镀膜的过程。例如:在铜片上电镀银时,电解原理是:采用AgNO3溶液为电解质,用?作阳极。而在实际的电镀工艺中,要求金属在镀件上的析出速率得到控制,使析出的镀层厚度均匀、光滑致密、与底层金属的附着力强。所以在铁件上电镀铜时,实际使用的电镀液是?。
A.FeCl 2
2
B.CuCl2
C.K6[Cu(P2O7)2]
D.CuSO4
4、选择题 蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成.现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,得到沉淀X和滤液Y.下列叙述正确的是( )
A.沉淀X的成分是SiO2、Fe2O3
B.从蛇纹石组成看,其成分皆是碱性氧化物
C.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
D.在溶液Y中加入过量的氨水,过滤得到的沉淀的成分是Fe(OH)3和Mg(OH)2
5、选择题 所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的融合物或冷却后的固体,下表中难与其他金属形成二元合金的元素是
?
| Fe
| Cu
| Zn
| Ag
| Au
| W
|
熔点/ ℃
| 1 535
| 1 083
| 419.5
| 960.8
| 1 063
| 3 380
|
沸点/ ℃
| 3 000
| 2 595
| 907
| 2 212
| 2 707
| 5 627
A.Fe、Ag
B.Au、Ag
C.Ag、Zn
D.Zn、W
|
题型:单选题难度:偏易来源:不详 答案 根据合金的含义,两种金属要形成合金,必须在一定温度下共熔,而像题表中的Zn沸点是907 ℃,当Zn达到沸点并气化时,其他几种金属都还没熔化,故它很难与其他金属熔融形成合金;同样道理,金属W的熔点高达3 380 ℃,当W熔化时,温度已高于其他几种金属的沸点,而使其气化,故W也难以与其他金属熔融形成合金。故答案为D项。
马上分享给同学