1、选择题 已知A为中学化学中的常见金属,X、Y为常见非金属。X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图(部分反应的条件、生成物被略去):

请填写下列空白:
⑴金属A为?;操作a是将D溶液在HCl气流中蒸干,原因是?
⑵反应②的化学方程为:?;
反应⑤的化学方程:?。
⑶原电池反应①中,正极反应式为:?。
参考答案:⑴镁(Mg)?防止金属离子(Mg2+)水解?
⑵ 4NH3+5O2 4NO+6H2O? C+4HNO3(浓)
4NO+6H2O? C+4HNO3(浓) CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
⑶ 2NH4++2e-=2NH3↑+H2↑
本题解析:本题的突破口有两个:一是E→F→G→H,属于常温下气体E的连续氧化得到气体G,在中学阶段可推出E为NH3、F为NO、G为NO2,则H为HNO3;二是C为无色液体,由气体X(X由原电池反应得到,可能是H2)和氧气反应得到,故C应是H2O,X是H2,则Y是非金属C。再由反应⑤可知J是CO2,则进一步推出A为Mg。其余物质可以依次推出。
本题难度:一般
2、推断题 物质A~H有如下图所示的转化关系(其中部 分反应物及生成物没有列出)。A为富集某种离子的海 水,B为饱和溶液,且B的电解是一种典型的化工生产 工艺,G常温常压下为深红棕色液体。
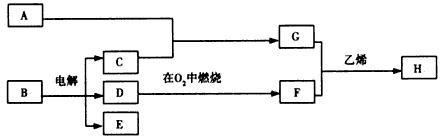
请回答下列问题:
(1)写出下列物质的化学式:B_________、F__________。
(2)电解A的浓溶液时,阳极反应式为______________,阴极生成物为__________。
(3)富集某种离子的海水与C反应的离子方程式为_______________________。
(4)H为一种有机化合物,该物质还存在一种同分异构体,请你写出H的同分异构体的结构简式__________________。
参考答案:(1) NaCl;H2O
(2)2Br--2e-=Br2;NaOH、H2
(3)2Br-+Cl2=2Cl-+Br2
(4)CH3CHBr2
本题解析:
本题难度:一般
3、简答题 我们已经学过了很多物质,如氧气、钠、硫酸、铁、碳酸钙、氢氧化钠、氢氧化铁、氯化铝、过氧化钠、氯化钠、氢氧化铝、碳酸钠、盐酸、碳酸氢钠、氧化铁、氧化钠、氧化铝、氯化铁、铝、二氧化碳、偏铝酸钠、二氧化硫等
(1)以上列举的物质中,属于两性氧化物的是______
(2)A、B、C、D是上述列举的物质中的四种物质,它们有如下的转化关系:
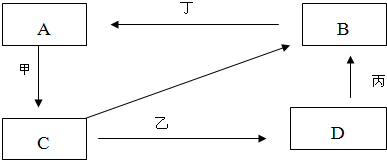
①写出A、B、C、D四种物质的化学式:A______B______C______D______
②写出甲、乙、丙、丁所表示的反应物的化学式或反应条件
甲______乙______丙______丁______
(3)从以上列举的物质中选择合适的物质,在溶液中分别发生如下的离子反应.写出其离子方程式.
①有一种难溶物质生成______
②有一种气体物质生成______
③有一种弱电解质生成______.
参考答案:(1)题中所给物质中,属于两性氧化物的为氧化铝,故答案为:氧化铝;
(2)由题中转化关系可知A、B、C、D应含有相同元素,题中只有氧化铝、氢氧化铝、氯化铝和偏铝酸钠符合,其中C能转化为B、D两种物质,应为NaAlO2,可与盐酸反应分别生成Al(OH)3、AlCl3,则D为Al(OH)3,B为AlCl3,A为Al2O3,
①由以上分析可知A为Al2O3,B为AlCl3,C为AlCl3,D为Al(OH)3,故答案为:Al2O3;AlCl3;NaAlO2;Al(OH)3;
②A为Al2O3,可与NaOH反应生成NaAlO2,NaAlO2可与过量二氧化碳反应生成Al(OH)3,Al(OH)3可与盐酸反应生成AlCl3,加热氯化铝溶液,促进铝离子的水解生成氢氧化铝,灼烧可生成氧化铝,
故答案为:NaOH;CO2;HCl;加热;
(3)①题中氢氧化钠和与氯化铝、氯化铁反应生成沉淀,如发生Fe3++3OH-=Fe(OH)3↓,故答案为:Fe3++3OH-=Fe(OH)3↓;
②所给物质中盐酸、硫酸可与碳酸钠、碳酸氢钠反应生成二氧化碳气体,可发生HCO3-+H+=CO2↑+H2O,故答案为:HCO3-+H+=CO2↑+H2O;
③对应的弱电解质为水,可为酸碱中和反应,金属氧化物与酸的反应,可发生Al2O3+6H+=2Al3++3H2O,故答案为:Al2O3+6H+=2Al3++3H2O.
本题解析:
本题难度:一般
4、填空题 (16分)已知:A、B、C、D、E五种物质间存在如下转化关系:A + B→C + D + E
(1)C溶液呈蓝色,D为红棕色气体,则该转化关系中涉及的离子方程式为?
?。
(2)若C为刺激性气味的气体且可使湿润的红色石蕊试纸变蓝,D为中性干燥剂。
① C的结构式为?;C是?(填“极性”或“非极性”)分子。
② A + B→C + D + E的化学方程式为?。
③工业上合成C的反应条件为?。
(3)若该转化关系中涉及的反应为氯碱工业的主要反应。
①以铁网和铂网作为电极,则铁网为?极,电极反应式为?。
②若反应后得到1L pH=13的E溶液,则两电极共产生气体?L(标准状况下)。
(4)若C、D均为无色气体,且C可以使品红溶液褪色。
①工业上利用黄铁矿生成C的设备是?。
②将2mol C和1mol O2充入2L密闭容器中,10min后达到平衡,此时C的转化率为75%。则10min内SO3的平均速率为?。
参考答案:(1)Cu + 4H+ + 2NO3- ="=" Cu2+ + 2NO2↑+ 2H2O
(2)①氨的结构式?(1分);极性(1分)
② Ca(OH)2 + 2NH4Cl 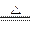 ?2NH3↑+ CaCl2 + 2H2O
?2NH3↑+ CaCl2 + 2H2O
③ 500℃,20MPa~50MPa,催化剂
(3)①阴(1分),2H+ + 2e? ="=" H2?② 2.24
(4)①沸腾炉(1分)?② 0.075mol・L?1・min?1
本题解析:略
本题难度:一般
5、填空题 由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如下图所示(某产物已略去):
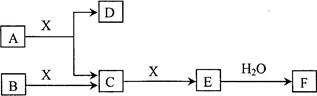
已知:B、X为单质,常温下D为无色液体,A、B含同一种元素。
请回答下列问题:
(1)若E气体是大气污染物,F是一元强酸。
①写出E→F反应的化学方程式:?。
②现有25℃时0.1 mol・L-1 A的水溶液,若向其中加入等体积0.1 mol・L-1的稀硫酸,则所得溶液中各离子的物质的量浓度由大到小的顺序是?。
③在常温下,向V1 L pH=a的A的水溶液中加入V2 L pH=b的盐酸,且a+b=14,若恰好完全反应,则V1和V2的关系为Vl?V2(填“>”、“<”、“=”或“无法确定”),等pH的所得溶液与盐酸比较,由水电离出的c(H+)前者为后者的108倍,则两种溶液的pH=?。
(2)若E气体不是大气污染物,F是二元弱酸。
①B所含元素在周期表中的位置?。
②写出氧化铁与C反应的化学方程式:?;将少量气体E通入氢氧化钙溶液中得不溶物F,F的Ksp=2.8×10-9。现将该沉淀放入0.1 mol・L-1的CaCl2溶液中,其Ksp?(填“增大”、“减小”或“不变”),此时,组成不溶物F的阴离子在溶液中的浓度为?。
参考答案:(1)① 3NO2+H2O=2HNO3+NO ?②c(H+)> c( SO42-) > c(NH4+) >c(OH-)?③ <? 3
(2)①第二周期ⅣA族?② Fe2O3+3CO 2 Fe +3CO2?不变?2.8×10-8 mol・L-1
2 Fe +3CO2?不变?2.8×10-8 mol・L-1
本题解析:(1)根据物质间的相互转化关系及已知条件可推知A是NH3,B是N2,C是NO,D是H2O,E是NO2。F是HNO3,X是O2。①写出E→F反应的化学方程式是3NO2+H2O=2HNO3+NO;②氨水与硫酸等体积等浓度混合得到的为NH4HSO4溶液。NH4HSO4= NH4++H++SO42-。由于发生:NH4++H2O  NH3・H2O+H+。H2O
NH3・H2O+H+。H2O OH-+H+。所以所得溶液中各离子的物质的量浓度由大到小的顺序是c(H+)> c( SO42-) > c(NH4+) >c(OH-)。③在常温下,对于NH3・H2O pH=a,C(H+)= 10-amol/L ,C(OH-)= 10(a-14)mol/L pH=b的盐酸,C(H+)=10-bmol/L 且a+b=14,所以C(H+)= C(OH-)。由于碱为弱碱C(NH3・H2O)>C(HCl).若恰好完全反应, V1和V2的关系是V1<V2。若NH4Cl与HCl的PH相等,假设它们的PH为X,则前者水电离产生的C(H+)=10-amol/L,后者由水电离出的c(H+)为10-(a+8)mol/L, C(OH-)= c(H+)=10-(a+8)mol/L,在整个溶液中C(OH-)・c(H+)=Kw=10-14. 10-(a+8) ・10-a=10-14.解得a="3." 则两种溶液的pH=3.(2) 根据物质间的相互转化关系及已知条件可推知A是CH4,B是C,C是CO,D是H2O,E是CO2。F是H2CO3,X是O2。①B所含元素在周期表中的位置第二周期ⅣA族,②写出氧化铁与CO反应的化学方程式:Fe2O3+3CO
OH-+H+。所以所得溶液中各离子的物质的量浓度由大到小的顺序是c(H+)> c( SO42-) > c(NH4+) >c(OH-)。③在常温下,对于NH3・H2O pH=a,C(H+)= 10-amol/L ,C(OH-)= 10(a-14)mol/L pH=b的盐酸,C(H+)=10-bmol/L 且a+b=14,所以C(H+)= C(OH-)。由于碱为弱碱C(NH3・H2O)>C(HCl).若恰好完全反应, V1和V2的关系是V1<V2。若NH4Cl与HCl的PH相等,假设它们的PH为X,则前者水电离产生的C(H+)=10-amol/L,后者由水电离出的c(H+)为10-(a+8)mol/L, C(OH-)= c(H+)=10-(a+8)mol/L,在整个溶液中C(OH-)・c(H+)=Kw=10-14. 10-(a+8) ・10-a=10-14.解得a="3." 则两种溶液的pH=3.(2) 根据物质间的相互转化关系及已知条件可推知A是CH4,B是C,C是CO,D是H2O,E是CO2。F是H2CO3,X是O2。①B所含元素在周期表中的位置第二周期ⅣA族,②写出氧化铁与CO反应的化学方程式:Fe2O3+3CO 2 Fe +3CO2。因为沉淀的溶度积常数KSp只与温度有关,与离子的浓度大小无关,所以将该沉淀放入0.1 mol・L-1的CaCl2溶液中,其Ksp不变。此时,组成不溶物F的阴离子在溶液中的浓度为2.8×10-9÷0.1=2.8×10-8 mol/L.
2 Fe +3CO2。因为沉淀的溶度积常数KSp只与温度有关,与离子的浓度大小无关,所以将该沉淀放入0.1 mol・L-1的CaCl2溶液中,其Ksp不变。此时,组成不溶物F的阴离子在溶液中的浓度为2.8×10-9÷0.1=2.8×10-8 mol/L.
本题难度:困难