1������� Q��R��X��Y��Z��ԭ������������������ֶ�����Ԫ�أ��ڶ����ڵ�����Ԫ����Q��ԭ�Ӱ뾶��Z��ԭ�Ӱ뾶֮����С(������ϡ������)��R��X��Y����Ԫ�ص�ԭ�Ӻ�����Ӳ�����ͬ��ͬһ������R��һ�ֵ��ʵ��۵���ߣ�Y��Q��R��X��Z�����γɶ��ֳ��������
��1��X�����ڱ��е�λ�ã�?����ԭ�Ӻ�����?�ֲ�ͬ��״�ĵ����ơ�������Ԫ���У������������δ�ɶԵ��ӵ�Ԫ����?����Ԫ�ط��ű�ʾ����
��2��������Һ̬�������ֻ������Ԫ���е����֣�������ԭ�Ӹ�����1�U1���ĵ���ʽ��_______________��
��3��Q�ֱ���X��Y�γɵ����������ȶ���______>______���÷���ʽ��ʾ��
��4��Q��R��Ԫ�ؿ���ɶ��ַ��ӣ���ռ乹�Ϳ�����?����д��ţ���
a��ֱ����? b��ƽ����? c��������? d����������
��5��X�����������γɹ⻯ѧ����ԭ��֮һ����ҵ�Ͽɲ����������⻯�ﷴӦ�����������ʶ���ȥ�����÷���ʽ��ʾ�÷�Ӧ?��
�ο��𰸣���1����2���ڵ�VA��? 2? C? O ��2��H2O2�ĵ���ʽ ��3��H2O>NH3��4��abd
��3��H2O>NH3��4��abd
��5��6NO2+8NH3=7N2+12H2O��6NO+4NH3=5N2+6H��6NOX+4XNH3=(3+2X)N2+6XH2O
�����������1�������������֪����Ԫ�طֱ���Q��H��R��C��X��N��Y��O��Z��Cl.����NԪ�������ڱ��е�λ���ǵڶ����ڵڢ����塣����ԭ�Ӻ�����S��P���ֲ�ͬ��״�ĵ����ơ�������Ԫ���У������������δ�ɶԵ��ӵ�Ԫ����C����2��������Һ̬�������ֻ������Ԫ���е����֣�������ԭ�Ӹ�����1�U1�Ļ�������H2O2�������ʽ�� ����3��Ԫ�صķǽ�����O>C��Ԫ�صķǽ�����Խǿ������ڵ��⻯��Խ�ȶ�����Q�ֱ���X��Y�γɵ����������ȶ���H2O>NH3����4��C2H2��ֱ���ͣ�C2H4��C6H6ƽ���Σ�CH4�������塣����ѡ��Ϊ��abd����5��NO��NO2���γɹ⻯ѧ����ԭ��֮һ����ҵ�ϲ����������⻯�ﷴӦ�����������ʶ���ȥ����ʽ�ǣ�6NO2+8NH3=7N2+12H2O��6NO+4NH3=5N2+6H��6NOX+4XNH3=(3+2X)N2+6XH2O��
����3��Ԫ�صķǽ�����O>C��Ԫ�صķǽ�����Խǿ������ڵ��⻯��Խ�ȶ�����Q�ֱ���X��Y�γɵ����������ȶ���H2O>NH3����4��C2H2��ֱ���ͣ�C2H4��C6H6ƽ���Σ�CH4�������塣����ѡ��Ϊ��abd����5��NO��NO2���γɹ⻯ѧ����ԭ��֮һ����ҵ�ϲ����������⻯�ﷴӦ�����������ʶ���ȥ����ʽ�ǣ�6NO2+8NH3=7N2+12H2O��6NO+4NH3=5N2+6H��6NOX+4XNH3=(3+2X)N2+6XH2O��
�����Ѷȣ�һ��
2��ѡ���� �裨81T1����Ԫ�����ڱ���A��Ԫ�أ����й��������������ȷ����
A��������Ľ����Ը�ǿ
B�����������ᷴӦ�ų�����
C�����ڻ������п�����+3��
D����������һ����������
�ο��𰸣�D
����������������ͬһ���壬���ϵ��£��뾶��������������ǿ���ǽ�������������A ��ȷ������������Ӧ��ˮ�����������ǿ���������������ԣ����������Ӧ���м��ԣ�D����ͬһ���廯ѧ�������ƣ�B��C ��ȷ��
�����Ѷȣ���
3������� (8��)ͬ��ͬѹ�£�������������H2��D2��T2���ܶ�֮��Ϊ________________��������֮��Ϊ__________��������֮��Ϊ__________�����֮��Ϊ___________________��
�ο��𰸣�.1��2��3 ��? 6��3��2 ��? 0��3��4��? 6��3��2 ��
���������ͬ��ͬѹ�£��ܶȱȵ���ʽ���ȣ������ߵ��ܶ�֮��Ϊ2��4��6��
H��D��T��ԭ�ӵ���������Ϊ1�����������ֱ�Ϊ0��1��2�����Ե�������H2��D2��T2��
���ʵ�����ʽ���ɷ��ȣ���6��3��2��
����ȵ������ʵ����ȣ�ҲΪ6��3��2
����������6��0��3��2��2��4����0��3��4
�����Ѷȣ�һ��
4��ѡ���� �ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��ǻ�ѧ�ͼ�������ᷢչ������ľ���֮һ������ȡ�ϳɰ�ԭ�����Ĺ����У�������һЩ���ʣ���CO��ʹ�����ж�����ȥCO�Ļ�ѧ��Ӧ����ʽ��HAc��ʾ���ᣩ��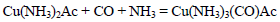
��ش��������⣺
��1��C��N��O�ĵ�һ�������ɴ�С��˳��Ϊ?��
��2��д����̬Cu+�ĺ�������Ų�ʽ?��
��3�������Cu��NH3��3��CO��Ac����ԭ�ӵ���λ��Ϊ?��
��4��д����CO��Ϊ�ȵ���������� ?������дһ����
��5����һ��������NH3��CO2�ܺϳɻ�������[CO��NH2��2]�������� Cԭ�Ӻ�Nԭ�ӹ�����ӻ����ͷֱ�Ϊ?��1 mol���ط����У��Ҽ�����ĿΪ ?��
�ο��𰸣���1��N��O��C ��2��[Ar]3d10��3��4 ��4��CN-��5��sp2�ӻ���sp3�ӻ���4.214��1024
�����������1��һ����˵�ǽ�����Խǿ����һ�����ܴ�����O��N��C��������Ϊp����������ϵ���к�ǿ���ȶ��ԣ�N��p����������ǰ�����ģ�O��p���ʧȥһ�����Ӳ��ǰ�����ģ�����O��N����ʧȥ���ӣ��ʴ�ΪN��O��C��2��ͭԭ�ӵĺ�������Ų�Ϊ1s22s22p63s23p63d104s1?��һ��ͭ���ӵĺ�������Ų�Ϊ1s22s22p63s23p63d10���ʴ�Ϊ[Ar]3d10��3��һ��ͭ�������������������һ���ʻ����壬��4�����壬�ʴ�Ϊ4��4���ȵ�����Ϊ�����������ͬ�����ӣ��ʻ�Ϊ14�����ӣ���CN-ҲΪ14�����ӣ��ʴ�ΪCN-��5������ԭ��Ϊ̼���۵�����Ϊ4������Ϊ����ԭ�ӣ����ṩ���ӣ�ÿ���ǰ����ṩһ�����ӣ����Ӷ���Ϊ��4+1��2����2=3�����ӻ����Ϊsp2������ԭ��Ϊ������ԭ�Ӻ���3�����ۼ���һ���µ��ӶԵ�ԭ�ӵļӳɵ��Ӷ�=3+1=4������һ���µ��Ӷԣ�Nԭ�ӹ�����ӻ�������sp3���Ҽ�����ĿΪ3��ÿ���ǰ����ЦҼ�����Ŀ2��һ���������к��Ҽ�����ĿΪ3+2��2=7����ÿĦ�������к��ЦҼ�����ĿΪ 7NA�ʴ�Ϊsp2��sp3��7NA��
�����Ѷȣ�һ��
5��ѡ���� ͬһ�����X �� Y �� Z����Ԫ��,��֪����������Ӧˮ���������ǿ����H3XO4��H3YO4��H3ZO4 ,�����ƶ���ȷ����
A��ԭ������: X��Y��Z
B����̬�⻯���ȶ���: XH3��YH3��ZH3
C��Ԫ�صķǽ���ǿ��: X��Y��Z
D�����Ӳ���: X��Y��Z
�ο��𰸣�D
���������ͬ�������϶��£�����ԭ�������ĵ������ǽ���������������������ˮ�����������������Ӧ�⻯����ȶ������������Ը��������֪�ǽ�������X��Y��Z�����ѡ��D�Ǵ���ģ��������ȷ�ģ���ѡD��
�����Ѷȣ���